

Тема: Круговорот воды в природе
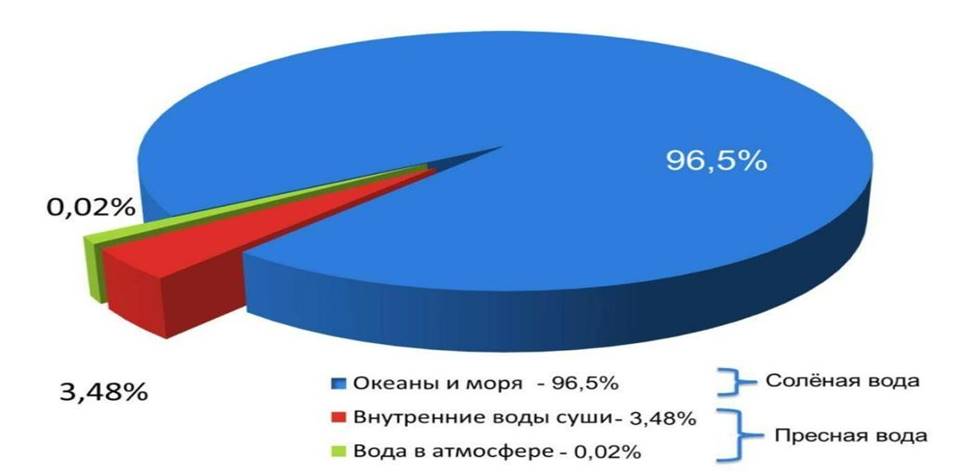
Запасы воды на земле огромны. Она находится в морях и океанах, в
материковых ледниках и полярных льдах, в пресных водах озер, рек и болот. Значительные
количества воды содержатся в атмосфере воздуха и горных породах, в живых
организмах.
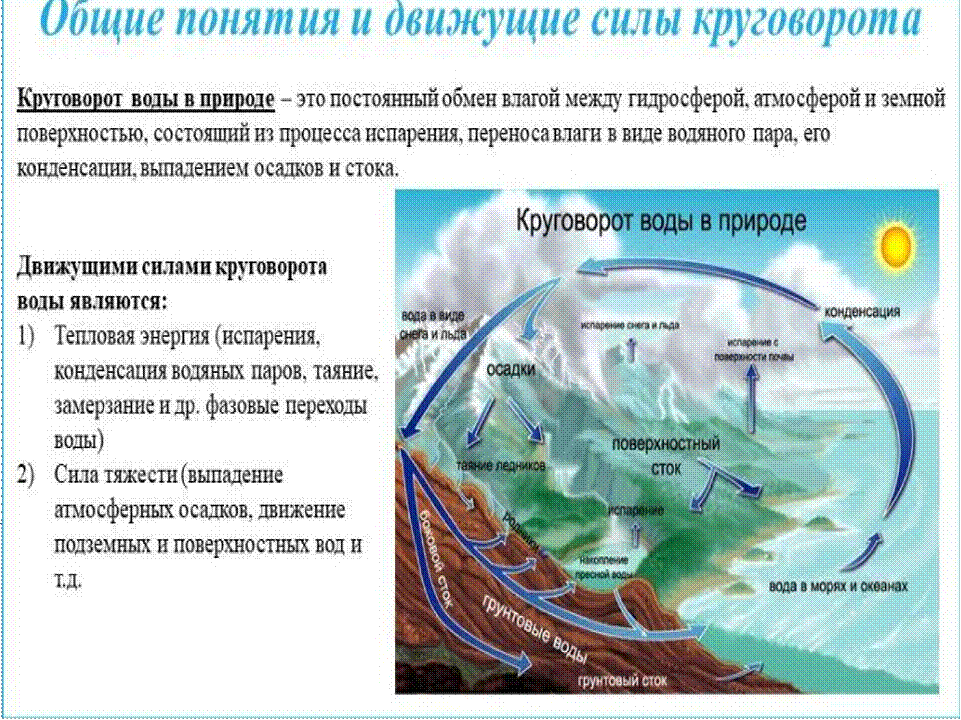
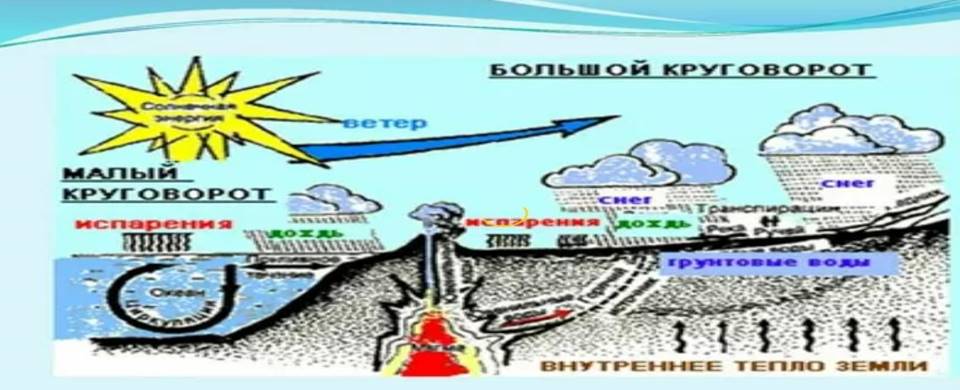
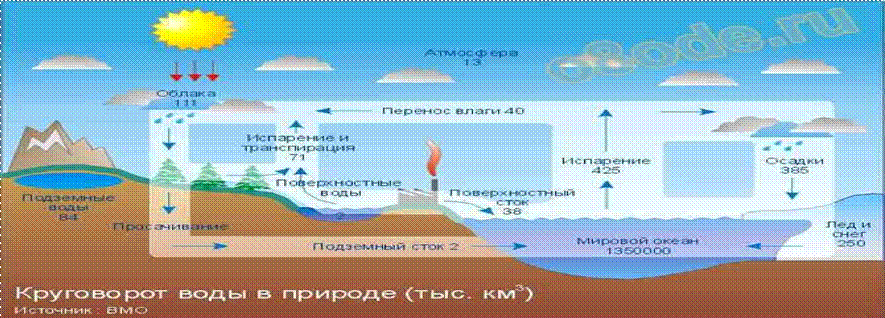
Большой, или мировой, круговорот —
водяной пар, образовавшийся над поверхностью океанов,
переносится ветрами на материки, выпадает там в виде атмосферных осадков и
возвращается в океан в виде стока. В этом процессе изменяется качество воды:
при испарении соленая морская вода превращается в пресную, а загрязненная —
очищается.
 |
 |
Геологический – процесс беспрерывного обмена водами между сушей и океаном.
 |
Глобальный – приток воды из глубин Земли через тектонические трещины (около 0,25 км3 в год) и устремление молекул водяного пара в космос.
Процесс имеет незамкнутый характер.

В теплое время года вода морей и океанов нагревается Солнцем. За счет этого она испаряется, то есть из жидкого состояния переходит в газообразное. При этом вода лишается солей. Таким образом, в атмосфере накапливается пресный водяной пар, который постепенно поднимается в ее верхние слои. С высотой температура понижается, а, значит, пар встречает на своем пути холодные воздушные потоки. Также имеет место процесс адвекции – перемещения воздушных масс горизонтально. Так водяной пар попадает в зону низких температур и конденсируется – превращается в капли воды, образуя облака. Из облаков впоследствии выпадают осадки, которые наполняют океан.
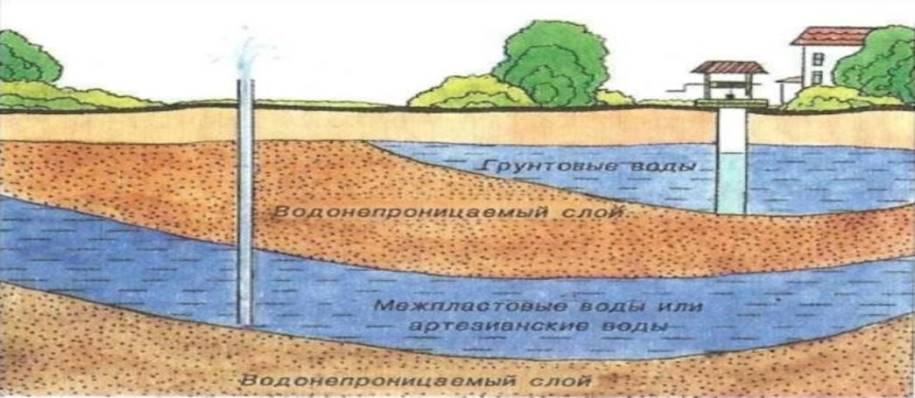 |
 |
 ПЕРЕХВАТ:
ПЕРЕХВАТ:
растительность перехватывает часть выпадающей в осадках воды до того, как она достигает почвы.
 ТРАНСПИРАЦИЯ: биологическое
ТРАНСПИРАЦИЯ: биологическое
испарение воды
растениями через устьица листовой пластинки, но не
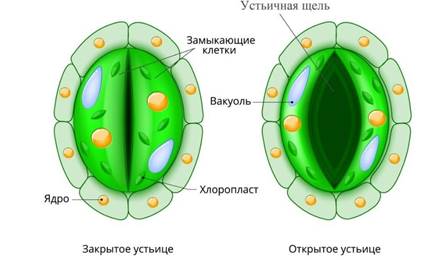 дождевая вода, а вода, заключенная в растении, т.е. экосистемная
дождевая вода, а вода, заключенная в растении, т.е. экосистемная
 |
СТОК: в этой фазе круговорота избыток выпавшей с осадками воды стекает в моря и океаны.
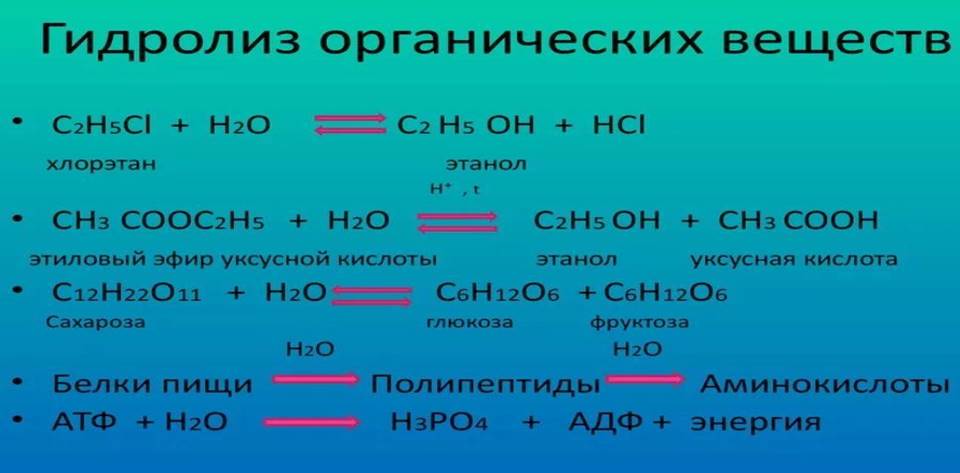
Без воды невозможен гидролиз — химическая реакция, которая
сопровождает усвоение белков, жиров, углеводов, а ведь именно они являются
обязательным компонентом нашей пищи, так, например, белок распадается на
аминокислоты, углевод на глюкозу, жиры
на глицерин. В результате сложные органические вещества распадаются до простых
веществ, которые, легко усваиваются организмом.
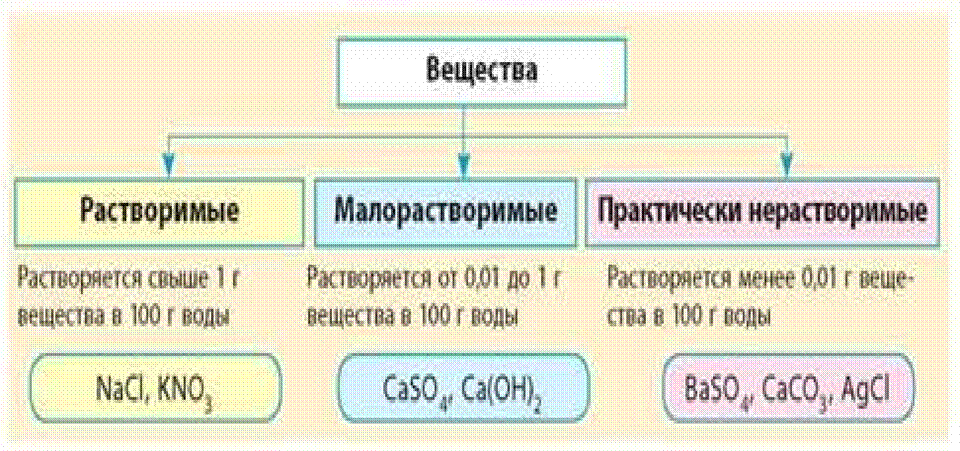
Вода является наиболее распространённым растворителем на нашей
планете. По растворимости в воде вещества делятся на три группы:
Вода образует многочисленные соединения, в которых ее молекула полностью сохраняется. Это так называемые гидраты. Если гидрат кристаллический, то он называется кристаллогидратом.
H2SO4 + H2O → H2SO4.H2O (гидрат серной кислоты)
NaOH + H2O → NaOH.H2O (гидрат едкого натра)
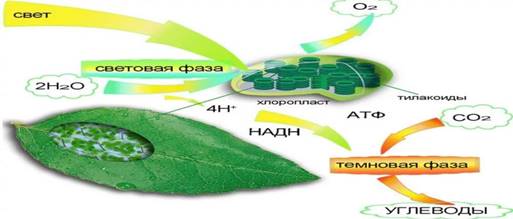
Фотосинтез — процесс, протекающий в зеленных листьях растений с использованием энергии света,
при котором из углекислого газа и воды образуются органические вещества и кислород.
6n CO2 + 5n H2O → (C6H10O5)n + 6n O2
(при действии света)
Минерализация — это показатель количества содержащихся в воде растворенных веществ (неорганические соли неорганические вещества). Как правило, это бикарбонаты, хлориды, сульфаты кальция, магния, калия, натрия и других веществ.
Свойство минерализации основано на дипольном моменте оксида водорода. Благодаря его наличию молекулы способны присоединять к себе множество других веществ ионов и удерживать их. Так формируются ассоциаты и прочие объединения.
С точки зрения бальнеологии по степени минерализации воду классифицируют на:
* столовую — минерализация до 1 г/л
*лечебно-столовую — минерализация от 1 г/л до 10 г/л
*лечебная — минерализация более 10 г/л или высокое содержание биологически активных элементов:
железо, брома, йода, сероводорода, фтора и т. д., при этом общая минерализация может быть невысокой.
Вода может взаимодействовать с металлами с выделением водорода:
− с активными
2Na + 2H2O → H2 + 2NaOH (бурно)
− со средней активностью до H
(только при нагревании)
− с малоактивными после H (не взаимодействуют)
Вода –активное химическое вещество
Вода может взаимодействовать с неметаллами:
из неметаллов с водой реагируют углерод и его водородное соединение (метан) при высокой температуре:
C + H2O → H2 + CO (при сильном нагревании)
CH4 + 2H2O → 4H2 + CO2 (при сильном нагревании)
Вода может взаимодействовать с газами: как уже говорилось ранее вода взаимодействует с оксидами неметаллов. В данном случае CO2 — это газ. Если струю газообразного оксида углерода (IV) CO2 направить в воду, то часть его раствориться в ней. В этом растворе произойдет химическая реакция соединения и образуется вещество — угольная кислота H2CO3.

Собирая углекислый газ над водой, ученый Джозеф Пристли обнаружил, что часть газа растворяется в воде и придает ей приятный терпкий вкус. По сути, Пристли впервые получил напиток газированный или содовой воды. Позже ученый Торберн Бергман создал аппарат, позволяющий насыщать жидкость углекислым газом под давлением и назвав его сатуратором.
Важное свойство круговорота
воды заключается в том, что он, взаимодействуя с литосферой, атмосферой и живым
веществом, связывает воедино все части гидросферы: океан, реки, почвенную
влагу, подземные воды и атмосферную влагу. Поэтому круговорот воды является
одним из наиболее важных явлений в природе. Без него трудно представить
существование жизни на нашей планете. Вместе с водой по всей биосфере
циркулируют разные органические вещества и минералы, а также она способствует
формированию оптимальных климатических условий. 
 Круговорот воды является одним из грандиозных процессов на
поверхности земного шара. Он играет главную роль в связывании геологического и
биотического круговоротов. Рассмотренная мною тема является очень актуальной в
свете современной экологической ситуаци
Круговорот воды является одним из грандиозных процессов на
поверхности земного шара. Он играет главную роль в связывании геологического и
биотического круговоротов. Рассмотренная мною тема является очень актуальной в
свете современной экологической ситуаци
и.
Вода – это источник жизни на земле, но, как выясняется не бесконечный. Дело в том, что загрязнение водных ресурсов земли имеет в настоящий момент глобальный характер. Очень важно обеспечить «природе» нормальное функционирование ее базовых циклов обмена веществ.
Благодарю за внимание!

Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.