
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «СРЕДНЯЯ ШКОЛА № 4 МО АХТУБИНСКИЙ РАЙОН» ГОРОД АХТУБИНСК
ВКЛАД ОТЕЧЕСТВЕННЫХ ХИМИКОВ В РАЗВИТИЕ ОРГАНИЧЕСКОЙ ХИМИИ
Автор проекта:
ученица 10 Б класса
Гулина Александра Сергеевна
Руководитель проекта:
учитель химии
Конькова Марина Николаевна
Ахтубинск – 2019
ПАСПОРТ
Тема проекта: «Вклад отечественных химиков в развитие органической химии»
Школа, класс: МБОУ «СОШ № 4 МО «Ахтубинский район» 10 «Б» класс
Автор проекта: Гулина Александра Сергеевна
Руководитель проекта: Конькова Марина Николаевна
Учитель химии.
Сроки реализации: сентябрь 2018 г – май 2019 г.
Аннотация:
В данном проект я попыталась обобщить полученную мной информацию о вкладе российских ученых в развитие органической химии. Данный вопрос встречается в школьной программе, но достаточно узко, поэтому я решила изучить этот вопрос глубже и с результатами своего исследования познакомить своих одноклассников.
Очень часто я слышу о
том, что Россия отстаёт от Запада по многим параметрам, но я с этим не согласна
и хочу рассказать о вкладе российских ученых, которые были оценены не только в
России, но и за рубежом. Так, 27 марта 1924 году президент Лондонского
химического общества У.П. Уинни на Годичном собрании Общества в своей речи
сказал: «…если мы, оценивая по заслугам музыкальную школу, связанную с именами
Балакирева, Бородина, Римского – Корсакова, Чайковского, или писателей Тургенева,
Достоевского, Льва Толстого и их современников, считаем, что без них свет был
бы неизмеримо беднее, то не будет преувеличением утверждение, что рост химии не
в меньшей степени был задержан, если бы работы Менделеева, Бутлерова, Вагнера и
их приемников по какой – либо причине были бы изъяты из общей сокровищницы
знаний». Мы должны гордиться нашей наукой, так как многие открытия впервые были
сделаны в России и являются весомым вкладом в развитии химии в целом.[1]
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ…………………………………………………………………3
ГЛАВА 1. ОСНОВНЫЕ ОТКРЫТИЯ РОССИЙСКИХ УЧЁНЫХ В ОБЛАСТИТЕОРЕТИЧЕКОЙ ОРГАНИЧЕСКОЙ ХИМИИ…………................5
1.2 Современное значение теории химического строения им. Бутлерова……………………………………………………………………………..7
1.3 Правило Марковникова…………………………………………………8
ГЛАВА 2. ОСНОВНЫЕ ОТКРЫТИЯ РОССИЙСКИХ УЧЁНЫХ В ОБЛАСТИ ОПЫТНОЙ ОРГАНИЧЕСКОЙ ХИМИИ……………………………10
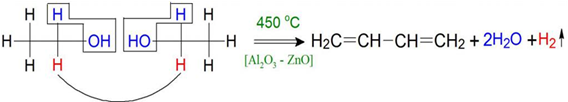
2.1 Реакция Лебедева………………………………………………………10
2.2 Реакция Коновалова ………………………………………...................11
2.3 Реакция Зинина…………………………………………………………12
2.4 Реакция Бородина………………………………………………………13
2.5 Реакция Зелинского – Казанского…………………………………….14
2.6 Реакция Кучерова………………………………………………………14
ГЛАВА 3. ОСНОВНЫЕ ОТКРЫТИЯ РОССИЙСКИХ УЧЁНЫХ В ОБЛАСТИ ПРИКЛАДНОЙ ОРГАНИЧЕСКОЙ ХИМИИ....................................16
ВЫВОД…………………………………………………………...................18
ГЛОССАРИЙ……………………………………………………………….19
СПИСОК ЛИТЕРАТУРЫ………………………………………………….26
ВВЕДЕНИЕ
Органическая химия известна с давних времён, но как наука сформировалась в начале 19 века. Химия лежит в основе большинства процессов в живой природе. Примеров тому очень много. Мы восхищаемся изменением окраски листьев в осенний период. Вначале они зелёные. Эту окраску растениям придаёт пигмент хлорофилл – сложное органическое вещество. С приближение осени и похолоданием, он разрушается и обесцвечивается. После его исчезновения проявляются необыкновенные красивые цвета каротинов, антоцианинов, флавонолов – органических пигментов устойчивых к холоду.
Любой живой организм представляет собой уникальную химическую лабораторию, в которой осуществляются тысячи химический реакций. Понятие органической химии впервые предложил шведский химик Берцелиус в 1807 году.
Из всех известных в науке веществ примерно 95% относятся к органическим. Они составляют основу пищевых продуктов, сырьё для производства тканей, входят в состав различных видов топлива, могут служить конструктивными материалами для создания медицинского оборудования, применятся в автомобилестроении и других производствах. Органические вещества основные компоненты лекарств, моющих средств, синтетических волокон и каучуков и так далее.
Очень многие открытия в органической химии были сделаны российскими учёными.
Органическая химия, а особенно органический синтез, лежат в самом сердце химии. Современное развитие органического синтеза жизненно необходимо. Достаточно посмотреть вокруг для того, чтобы понять и убедиться, что без органической химии не мог бы существовать современный мир. Человечеству нужны лекарства с самыми различными спектрами действия, также нужны ростовые вещества и средства борьбы с вредителями сельского хозяйства, материалы с различными свойствами, волокна, которые смогут заменять шерсть и шёлк, пластические массы, красители, взрывчатые вещества и средства для тушения пожаров, а для всего этого нужны мономеры, синтез которых основан на открытиях химиками – органиками реакций.
На сегодняшний день химики синтезировали более 88 миллионов соединений, и порядка 15000 новых химических соединений регистрируется ежедневно. Это количество значительно больше того, что создала природа, и такая безграничность структур поражает воображение самих исследователей. Практически ученые создали целый химический мир, где можно найти молекулы с ранее неизвестными свойствами. Многие соединения были синтезированы российскими учёными в XX веке и эти синтезы используются до сих пор, поэтому я считаю, что мы должны знать какие открытия были сделаны нашими учёными, какой вклад они внесли в развитие органической химии.
Цель работы: Изучение роли открытий отечественных учёных в органической химии.
Задачи:
1. Собрать и проанализировать имеющуюся литературу по данной теме.
2. Изучить вклад отечественных учёных в сфере теоретических знаний по органической химии.
3. Рассмотреть основные реакции химического синтеза, открытые нашими учёными.
4. Показать практическое применение открытий, сделанных нашими учёными.
Гипотеза: Можно ли сказать, что открытия, сделанные российскими учёными в области органической химии, вносят весомый вклад в развитие химии в целом.
«…Так как в своём развитии химия захватила и ряд прикладных областей, совершенно овладев некоторыми из них, то её изучение стало многообъемлющим в наше время и история нашей науки , в её теоретической, опытной и прикладной частях, даёт объяснение многому – иначе непонятному».
Менделеев Д.[2]
ГЛАВА 1. ОСНОВНЫЕ ОТКРЫТИЯ РОССИЙСКИХ УЧЁНЫХ В ОБЛАСТИ ТЕОРЕТИЧЕСКОЙ ОРГАНИЧЕСКОЙ ХИМИИ
1.1 Теория А.М. Бутлерова
Органическая химия как наука сформировалась в XIX веке, но с органическими веществами человек был знаком еще с древности и обширно применял их в своей жизни, так, например, древние люди путём брожения сахаристых веществ умели получать спирт. Был известен уксус, получаемый при скисания вина. В древнем Риме использовались различные растительные красители. Однако в древние времена люди имели дело только со смесями, а чистые органические вещества стали получать значительно позднее, так, например, ряд чистых органических веществ был выведен только в XVIII веке.
Когда органическая химия сформировалась как наука, то первые открытия в этой области были сделаны зарубежными учеными, а вклад отечественных ученых начался чуть позже.
Первый из отечественных химиков, кто внёс значительный вклад в развитие органической химии, был Александр Михайлович Бутлеров. Долгие годы А.М.Бутлеров работал над теорией химического строения органических веществ. Эта теория заключалось в том, что свойства органических соединений зависят не только от химических элементов и их количества, но и от структуры молекулы, то есть, говоря простым языком от того, как атомы связаны между собой. Теория А.М.Бутлерова так же объяснила и существование такого явления как изомерия – явления, при котором возможно существование веществ с одинаковым составом, но разным строением. Ознакомимся с теорией химического строения органических веществ ближе.
В 1858 году А.М.Бутлеров считал, что возможно определённое группирование атомов в сложные частицы и саму причину этой группировки он видел в химическом сходстве. Три года спустя А.М.Бутлеров в своем докладе «О химическом строении веществ» излагает идею химического строения в более развитой форме.
Основы этой теории сформулированы следующим образом:
1. «Полагая, что каждому химическому атому свойственно лишь определённое и ограниченное количество химической силы (сродства), с которой он принимает участие в образовании тела, я назвал бы химическим строением эту химическую связь, или способ взаимного соединения атомов в сложном теле»
2. «… химическая натура сложной частицы определяется натурой элементарных составных частей, количеством их и химическим строением»
С этими основами так или иначе связаны и все остальные положения теории химического строения. Бутлеров намечает путь для определения химического строения и формулирует правила, которыми можно будет при этом руководствоваться. За основу он берёт синтетические реакции, проводимые в таких условиях, когда радикалы , участвующие в них, сохраняли своё химическое строение, но он думает и о том, что возможны перегруппировки, и полагает, что в последствии «общие законы» будут открыты и для таких случаев. Александр Михайлович полагал, что не все реакции пригодны для определения строения и существуют такие, при проведении которых изменяется строение химического вещества, то есть реакции, сопровождающиеся изомеризацией скелета или переносом реакционного центра.
Бутлеров впервые объяснил явление изомерии тем, что изомеры – это соединения, которые обладают одинаковым составом, но различным химическим строением. В свою очередь зависимость свойств изомеров и органических соединений от их химического строения объясняется тем, что в них существует передающийся вдоль связей «взаимного влияния атомов», в результате которого атомы приобретают различное «химическое значение» в зависимости от их структурного окружения.
Большое значение для теории химического строения имело её экспериментальное подтверждение. Бутлеров сумел доказать существование позиционной и скелетной изомерии, также он получил третичный бутиловый спирт, расшифровал его строение и доказал наличие у него изомеров, а на основе своей теории Бутлеров впервые начал изучать полимеризацию.
1.2 Правило Марковникова
При присоединении простых кислот или воды к несимметричному алкену или алкину атом водорода будет присоединяться к более гидрированному атому углерода, например, это можно наблюдать в реакции гидратации пропилена:
CH3-CH=CH2 + H2O = CH3-CH-OH-CH3
Первоначально правило Марковникова было сформулировано, для того чтобы можно было предсказывать региоселективность присоединения простых кислот и воды, но затем оно было распространенно и на реакции присоединения любых полярных молекул.
Правило Маровникова в электронной интерпретации предполагает, что более электроположительная часть полярной молекулы будет присоседиться к кратной связи так, чтобы образовался более устойчивый карбониевый ион.
Ориентация по правилу Марковникова требует меньше энергии для активации процесса, чем при реакции присоединения, которая будет проходить против правила Маровникова. В газовой фазе для некоторых реакций такое различие достигает 25-30 кДж/моль.
При наличии заместителей, которые проявляют электронноакцепторный эффект, например присоединение галогеноводородов или воды к кислотам, то реакция будет идти против правила Марковниова. Также присоединение против правила Марковникова можно наблюдать при свободнорадикальном присоединении.
2.2 Реакция Коновалова
Реакция Коновалова или нитрование – это реакция, при которой в алифатических и алициклических соединениях происходит замещение атома водорода на нитрогруппу, при нитровании разбавленной азотной кислотой:
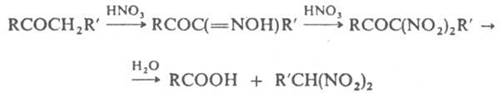
ArNO2 + 3H2S = ArNH2 + 2H2O + 3S
В ходе этой реакции происходит нагревание нитросоединений с их последующим восстановлением. Используя в этой реакции сульфиды в основном получают амины ряда антрахинона, также используя сульфиды можно частично восстановить ди- и полинитросоединения, при этом легче происходит восстановление нитрогруппы, которая находиться в пара- положении к другим заместителям.
Впервые реакция Зинина была применина для синтеза анилин, который до этого получали из индиго, а также для 2-нафтиламина, м-аминобензойной кислоты и м-фенилендиамина. Эти соединения стали доступны как промышленное сырьё, благодаря реакции Зинина.[3]
2.4 Реакция Бородина
Реакция заключается в разложении мочевины гипобромитом натрия. Для приготовления раствора гипобромита натрия в пробирку добавляют 1 – 2 миллилитра концентрированного раствора гидроксида натрия, затем при охлаждении добавляют 3 – 4 капли брома. Смесь встряхивают, пока бром не раствориться и не исчезнет его окраска (Рисунок 3).
![]()
Рисунок 3 – Взаимодействие брома с гидроксидом натрия
Дальше к 1 миллилитру 20% - ного раствора мочевины начинают по капли добавлять раствор гипобромита натрия, в результате чего в пробирке начинается бурное выделение азота и оксида углерода (IV) (Рисунок 4).
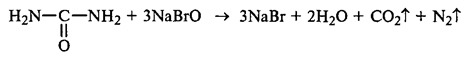
Рисунок 4 – Взаимодействие раствора мочевины с раствором гипобромита натрия
Эта реакция лежит в основе количественного определения мочевины. Масса мочевины рассчитывается по объёму выделившегося газа.
2.5 Реакция Зелинского – Казанского
Эта реакция представляет собой тримеризацию ацетилена над активированным углём и приводит к образованию бензола (Рисунок 5).
Тримеризация ацетилена была открыта ещё в 1866 году французским химиком М. Бертло. Он пропускал ацетилен через раскалённый трубку и получал бензол, но выход его был очень маленьким.
Позднее российские учёные Н.Д. Зелинский и Б.А. Казанский показали, что эта реакция проходит эффективней, если пропускать ацетилен через активированный уголь, нагретый до 600-650°С, при этом выход продукта будет составлять уже 70%.
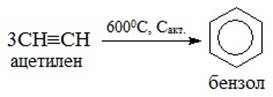
Рисунок 5 – Тримеризация ацетилена над активированным углём (реакция Зелинского – Казанского)
2.6 Реакция Кучерова
Реакцию проводят в воде или спиртовом растворе. В этой реакции используются катализаторы, такие как соли ртути (Hg2+) в кислой среде, например HgSO4 в H2SO4. Из ацетилена будет образовываться альдегид (Рисунок 6), а из алкинов, имеющих три и больше атомов углероды, будут образовываться кетоны (Рисунок 7).
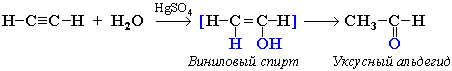
Рисунок 6 – Гидрирование ацетилена
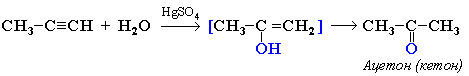
Рисунок 7 – Гидрирование пропина
Ион Hg2+ образует p – комплекс с молекулой алкина, к которой идёт присоединение молекулы воды с промежуточным образованием неустойчивого енола, который изомеризируется в карбонильное соединение. Присоединение воды к алкину происходит по правилу Марковинкова. Реакция протекает против правила Марковникова в том случае, если образуется семь продуктов.
Атом кислороды обычно присоединяется в том положении, которое будет наиболее удалено от электроотрицательной группы, но при небольшой разницы в полярности заместителей в молекуле алкина будет образовываться смесь продуктов.
ГЛАВА 3. ОСНОВНЫЕ ОТКРЫТИЯ РОССИЙСКИХ УЧЁНЫХ
В ОБЛАСТИ ПРИКЛАДНОЙ ОРГАНИЧЕСКОЙ ХИМИИ
Марковниковым помимо правила был открыт новый класс соединений – нафтены. Этот класс соединений нашёл широкое применение в промышленном органическом синтезе. Так, например, циклопропан используется в медицине в качестве ингаляционного анестезирующего средства; циклопентан используют в качестве добавки к моторному маслу для того, чтобы повысить его качество; циклогексан применяют для синтеза полупродуктов в производстве синтетического волокна, нейлона и капрона, также из циклогексана получают циклогексанол, циклогексанон и адипиновую кислоту, ещё он используется в качестве растворителя. Нефтехимическая промышленность использует нафтены для получения ароматических углеводородов путём каталитического крекинга.
Лебедевым, в его магистерской диссертации, был разработан метод синтеза бутадиенового каучука, на базе которого в дальнейшем был создан промышленный метод, который положил начало отечественной промышленности синтетического каучука. Благодаря работам Лебедева, в Советском Союзе в 1932 началось производство синтетического каучуку – впервые в мире.
Реакция Зинина позволила разработать промышленные способы получения анилина. В 1844 году, пользуясь восстановительным действием гидросульфида аммония на динитросоединения, Зининым был получен нафтилендиамин и фенилдиамин. В результате был открыт метод получения аминопроизводных из органических нитросоединений. Эти работы заложили научную основу для развития производства синтетических красителей, новых фармацевтических препаратов, душистых веществ.
Благодаря реакциям и опытам, описанным выше, в промышленности нашей страны произошло много поворотных моментов. Так, реакция, открытая М.Г. Кучеровым, превращение ацетилена в уксусный альдегид в присутствии ртутных солей положила начало техническому использованию ацетилена в качестве сырья для получения многочисленных химических продуктов. Также, получило развитие промышленного синтеза уксусной кислоты, благодаря, открытию М.Г.Кучерова. именно за это он в 1885 году был достоин премии Русского физико-химического общества. Наряду с химией, Михаил Григорьевич хорошо рисовать и его работы получили одобрение художника Александр Николаевич Бенуа. Также у него был красивый голос, прекрасная музыкальная память и слух, что позволяло ему почти в точности воспроизводить сольные партии ряда опер.
Развитие в этой области не стоит на месте, и наши учёные также продолжают делать вклад в дальнейшее её развитие. Так, например, химики из Российского химико-технологического университета имени Менделеева придумали, как перерабатывать смесь всевозможных пластмассовых бутылок, даже если они сделаны из разных полимеров.
Ещё одним важнейшим открытием российских учёных в наше время стало синтезированние нефти и газа. Это открытие было сделано учёными университета нефти и газ имени Губкина. Путём экспериментов и теоретических расчётов они доказали, что нефть и газ могут образовываться не только путём разложения органических веществ, но и абиогенным (небиологическим) путём. Учёные установили, что в верхней мантии Земли, на глубине 100 – 150 километров, существуют уловия для синтеза сложных систем углеводородных систем.
"Этот факт позволяет говорить о природном газе (по крайней мере) как о возобновляемом и неиссякаемом источнике энергии", — сказал РИА Новости профессор Владимир Кучеров из университета имени Губкина.
—
ВЫВОД
Российскими учёными был сделан огромный вклад в развитие органической химии, который был признан не только в нашей стране, но и за рубежом. В ходе работы я убедилась, что достижения российской науки в области органической химии действительно важны и играют весомую роль в её развитии. В моём проекте показана только малая часть всего того, что было сделано и открыто нашими учёными. Мы должны гордиться достижениями химиков – органиков, потому что благодаря им мы имеем в нашей жизни огромное количество различных веществ, без которых сложно прожить.
ГЛОССАРИЙ
Абсо́рбция — поглощение сорбата всем объёмом сорбента. Является частным случаем сорбции. В технике и химической технологии чаще всего встречается абсорбция газов жидкостями
Алкадиены (диеновые углеводороды) — класс углеводородов, содержащих две двойных связи углерод-углерод.
Алке́ны (олефины, этиленовые углеводороды) — ациклические непредельные углеводороды, содержащие одну двойную связь между атомами углерода, образующие гомологический ряд с общей формулой CnH2n. Атомы углерода при двойной связи находятся в состоянии sp² гибридизации и имеют валентный угол 120°.
Алки́ны (иначе ацетиленовые углеводороды) — углеводороды, содержащие тройную связь между атомами углерода, образующие гомологический ряд с общей формулой CnH2n-2. Атомы углерода при тройной связи находятся в состоянии sp-гибридизации.
Антоцианы — окрашенные растительные гликозиды, содержащие в качестве агликона антоцианидины — замещённые 2-фенилхромены, относящиеся к флавоноидам. Они находятся в растениях, обусловливая красную, фиолетовую и синюю окраски плодов и листьев.
Ароматические соединения (арены) — циклические органические соединения, которые имеют в своём составе ароматическую систему.
А́том — частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, являющаяся носителем его свойств.
Ацетальдеги́д (у́ксусный альдегид, этана́ль, метилформальдегид) — органическое соединение класса альдегидов с химической формулой CH3-CHO, является альдегидом этанола и уксусной кислоты.
Ацетиле́н (по ИЮПАК — этин) — органическое соединение, непредельный углеводород C2H2. Имеет тройную связь между атомами углерода, принадлежит к классу алкинов. При нормальных условиях — бесцветный, очень горючий газ.
Бутадие́н-1,3 (дивини́л, бу́та-1,3-дие́н) — ненасыщенный углеводород, простейший представитель сопряжённых диеновых углеводородов.
Вале́нтность —способность атомов химических элементов образовывать определённое число химических связей.
Валентный угол — угол, образованный направлениями химических (ковалентных) связей, исходящими из одного атома.
Галогеноводоро́ды — общее название соединений, образованных из водорода и галогенов (элементов подгруппы фтора)
Гидрата́ция — присоединение молекул воды к молекулам или ионам. Гидратация является частным случаем сольватации — присоединения к молекулам или ионам веществ молекул органического растворителя.
Двойная связь — ковалентная связь двух атомов в молекуле посредством двух общих электронных пар. Строение двойной связи отражено в теории валентных связей. В этой теории считалось, что двойная связь образуется комбинацией сигма- и пи-связей.
Изомерия — явление, заключающееся в существовании химических соединений — изомеров, — одинаковых по атомному составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам.
Кароти́н — жёлто-оранжевый пигмент, непредельный углеводород из группы каротиноидов. Эмпирическая формула С₄₀H₅₆. Нерастворим в воде, но растворяется в органических растворителях. Содержится в листьях всех растений, а также в корне моркови, плодах шиповника и др.
Каучу́ки — натуральные или синтетические эластомеры, характеризующиеся эластичностью, водонепроницаемостью и электроизоляционными свойствами, из которых путём вулканизации получают резины и эбониты.
Квазикриста́лл — твёрдое тело, характеризующееся симметрией, запрещённой в классической кристаллографии, и наличием дальнего порядка.
Конденса́ция — переход вещества в жидкое или твёрдое состояние из газообразного.
Моле́кула — электрически нейтральная частица, образованная из двух или более связанных ковалентными связями атомов.
Органи́ческая хи́мия — раздел химии, изучающий соединения углерода, их структуру, свойства и методы синтеза.
Органи́ческий си́нтез — раздел органической химии и технологии, изучающий различные аспекты получения органических соединений, материалов и изделий, а также сам процесс получения веществ.
Пиро́лиз — термическое разложение органических и многих неорганических соединений.
Полярность - это разделение электрического заряда, приводящее к тому, что молекула или ее химические группы имеют электрический дипольный момент с отрицательно заряженным концом и положительно заряженным концом.
Пропиле́н (пропен)— непредельный (ненасыщенный) углеводород ряда этилена, горючий газ. Вещество с наркотическим действием более сильным, чем у этилена. Класс опасности — четвертый.
Реакции присоединения — в органической химии так называются химические реакции, в которых одни химические соединения присоединяются к кратным (двойным или тройным) связям другого химического соединения.
Региоселективность — явление, при котором в химической реакции один путь разрыва и образования связей преобладает над остальными возможными путями. В зависимости от степени региоселективности реакции могут быть частично или полностью региоселективными.
Ректификация — это процесс разделения двойных или многокомпонентных смесей за счёт противоточного массо- и теплообмена между паром и жидкостью. Ректификация — разделение жидких смесей на практически чистые компоненты, отличающиеся температурами кипения, путём многократных испарений жидкости и конденсации паров.
Структурная формула — это разновидность химической формулы, графически описывающая расположение и порядок связи атомов в (ковалентном) соединении, выраженное на плоскости (2D-формулы) или в трёхмерном пространстве (3D-формулы) . Связи в структурных формулах обозначаются валентными черточками (штрихами).
Таутомери́я — явление обратимой изомерии, при которой два или более изомера легко переходят друг в друга. При этом устанавливается таутомерное равновесие, и вещество одновременно содержит молекулы всех изомеров (таутомеров) в определённом соотношении.
Тройная связь — ковалентная связь двух атомов в молекуле посредством трёх общих связывающих электронных пар.
Флавонолы - это класс флавоноидов, которые имеют 3-гидроксифлавоновую основу. Их разнообразие связано с различным положением фенольных групп -ОН. Они отличаются от флаванолов, таких как катехин, другой класс флавоноидов. Флавонолы присутствуют во многих фруктах и овощах.
Хлорофилл - зелёное красящее вещество листьев и др. органов растений, обусловливающее усвоение растениями углекислоты воздуха.
Этиле́н (по ИЮПАК: этен) — органическое химическое соединение, описываемое формулой С2H4. Является простейшим алкеном (олефином).
Organic synthesis - is a special branch of chemical synthesis and is concerned with the intentional construction of organic compounds. Organic molecules are often more complex than inorganic compounds, and their synthesis has developed into one of the most important branches of organic chemistry.
Flavonols - are a class of flavonoids that have the 3-hydroxyflavone backbone. Their diversity stems from the different positions of the phenolic -OH groups. They are distinct from flavanols (with "a") such as catechin, another class of flavonoids.
Isomers - are ions or molecules with identical formulas but distinct structures. Isomers do not necessarily share similar properties. Two main forms of isomerism are structural isomerism (or constitutional isomerism) and stereoisomerism (or spatial isomerism).
The valence or valency of an element is a measure of its combining power with other atoms when it forms chemical compounds or molecules. The concept of valence developed in the second half of the 19th century and helped successfully explain the molecular structure of inorganic and organic compounds.
A double bond in chemistry is a chemical bond between two chemical elements involving four bonding electrons instead of the usual two. The most common double bond, that is between two carbon atoms, can be found in alkenes.
A triple bond is a chemical bond between two atoms involving six bonding electrons instead of the usual two in a covalent single bond. The most common triple bond, that between two carbon atoms, can be found in alkynes.
An atom is the smallest constituent unit of ordinary matter that has the properties of a chemical element.
A molecule is an electrically neutral group of two or more atoms held together by chemical bonds. Molecules are distinguished from ions by their lack of electrical charge.
Tautomers are constitutional isomers of organic compounds that readily interconvert. This reaction commonly results in the relocation of a proton. Tautomerism is for example relevant to the behavior of amino acids and nucleic acids, two of the fundamental building blocks of life.
The structural formula of a chemical compound is a graphic representation of the molecular structure, showing how the atoms are arranged. The chemical bondingwithin the molecule is also shown, either explicitly or implicitly.
Acetaldehyde (systematic name ethanal) is an organic chemical compound with the formula CH3CHO, sometimes abbreviated by chemists as MeCHO (Me = methyl). It is one of the most important aldehydes, occurring widely in nature and being produced on a large scale in industry.
Propene, also known as propylene or methyl ethylene, is an unsaturated organic compound. It has one double bond, and is the second simplest member of the alkene class of hydrocarbons. It is a colorless gas with a faint petroleum-like odor.
Ethylene (IUPAC name: ethene) is a hydrocarbon which has the formula C2H4 or H2C=CH2. It is a colorless flammable gas with a faint "sweet and musky" odour when pure. It is the simplest alkene (a hydrocarbon with carbon-carbon double bonds).
In organic chemistry, the term aromaticity is used to describe a cyclic (ring-shaped), planar (flat) molecule with a ring of resonance bonds that exhibits more stability than other geometric or connective arrangements with the same set of atoms.
1,3-Butadiene is the organic compound with the formula (CH2=CH)2. It is a colorless gas that is easily condensed to a liquid. It is important industrially as a monomer in the production of synthetic rubber. The molecule can be viewed as the union of two vinyl groups. It is the simplest conjugated diene.
Pyrolysis is the thermal decomposition of materials at elevated temperatures in an inert atmosphere. It involves the change of chemical composition and is irreversible.
In organic chemistry a diene is a covalent compound that contains two double bonds, usually among carbon atoms.
In chemistry, polarity is a separation of electric charge leading to a molecule or its chemical groups having an electric dipole moment, with a negatively charged end and a positively charged end.
An addition reaction, in organic chemistry, is in its simplest terms an organic reaction where two or more molecules combine to form a larger one.
In chemistry, regioselectivity is the preference of one direction of chemical bond making or breaking over all other possible directions.
Acetylene (systematic name: ethyne) is the chemical compound with the formula C2H2. It is a hydrocarbon and the simplest alkyne. This colorless gas is widely used as a fuel and a chemical building block. It is unstable in its pure form and thus is usually handled as a solution. Pure acetylene is odorless, but commercial grades usually have a marked odor due to impurities.
In chemistry, a hydration reaction is a chemical reaction in which a substance combines with water. In organic chemistry, water is added to an unsaturated substrate, which is usually an alkene or an alkyne. This type of reaction is employed industrially to produce ethanol, isopropanol, and 2-butanol.
Propene, also known as propylene or methyl ethylene, is an unsaturated organic compound. It has one double bond, and is the second simplest member of the alkene class of hydrocarbons. It is a colorless gas with a faint petroleum-like odor.
СПИСОК ЛИТЕРАТУРЫ
Справочная литература:
1. Русский биографический словарь : в 25 томах. — СПб., 1908. — Т. 3: Бетанкур — Бякстер. — С. 528—533.
2. Книга для чтения по органической химии. Пособие для учащихся [Текст]. — М.: «Просвещение», 1975.
3. Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.) — СПб., 1891. — Т. V. — С. 79—82.
4. Московская речь о Бутлерове - Труды института истории естествознания и техники — 1956. — Т. 12. — С. 135—181.
5. Письма русских химиков к А. М. Бутлерову / Научное наследство. — Т. 4. — М., 1961.
Электронные ресурсы:
6. http://him.1september.ru/2000/38/no38_1.htm
7. http://himija-online.ru/imennye-reakcii/reakciya-zelinskogo.html
8. http://himija-online.ru/organicheskaya-ximiya/cikloalkany/primenenie-cikloalkanov.html
9. http://www.xumuk.ru/organika/01.html
10. https://kopilkaurokov.ru/himiya/presentacii/vklad_uchienykh_vrazvitiie_orghanichieskoi_khimii
11. https://pcgroup.ru/blog/vklad-aleksandra-mihajlovicha-butlerova-v-mirovuyu-i-rossijskuyu-nauku/
12. https://studfiles.net/preview/2983468/page:5/
Скачано с www.znanio.ru
[1] Уинни У.П. О значении работ русских химиков для мировой химии: Речь президента Английского химического общества, произнесенная на Годовом собрании Общества 27 марта 1924 г./ Пер. В.Г. Хлопина. Л.: Научн. хим. – техн. изд – во НТО ВСНХ, 1924, с. 7 – 8.
[2] Менделеев Д. [Предисловие] В кн.: Мейэр Э. История химии от древнейших времён до настоящих дней. СПб., 1899, с, 8
[3] Фигуровский Н. А., Соловьев Ю. М., Н. Н. Зинин, М., 1957; Эфрос Л. С, Горелик М. В., Химия и технология промежуточных продуктов, Л., 1980, с. 466-73; Porter Н. К., "Organic Reactions". 1973, v. 20, p. 455-81. Н. Э. Нифантьев.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.