
Электрический ток в растворах и расплавах электролитов.
Электролитическая диссоциация
 Как и другие тела, жидкости
могут являться проводниками, полупроводниками и диэлектриками.
Например, дистиллированная вода является диэлектриком. Это легко подтверждается
с помощью опыта. Поместим два электрода в ванну с водой. Эти электроды мы
подсоединим к источнику тока, а также включим в цепь лампочку и выключатель.
Как и всегда, с помощью выключателя мы можем замыкать и размыкать цепь, ну а
лампочка будет служить индикатором того, что по цепи протекает электрический
ток.
Как и другие тела, жидкости
могут являться проводниками, полупроводниками и диэлектриками.
Например, дистиллированная вода является диэлектриком. Это легко подтверждается
с помощью опыта. Поместим два электрода в ванну с водой. Эти электроды мы
подсоединим к источнику тока, а также включим в цепь лампочку и выключатель.
Как и всегда, с помощью выключателя мы можем замыкать и размыкать цепь, ну а
лампочка будет служить индикатором того, что по цепи протекает электрический
ток.
Итак, если мы замкнем цепь, то никакого электрического тока мы не получим: ведь дистиллированная вода является диэлектриком. Разомкнем цепь и насыплем в ванну некоторое количество самой обычной поваренной соли. Подождав, пока соль растворится, снова замкнем цепь. В этом случае, лампочка загорится, что будет означать протекание электрического тока по всей цепи. Давайте разберемся, как же соль могла повлиять на проводимость воды.
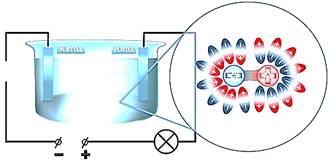 После того, как мы
насыпали соль в ванну, там образовался солевой раствор. Как вы знаете из курса
химии, молекулы воды являются полярными, так же, как и молекулы поваренной
соли. Центр распределения положительного заряда в поваренной соли приходится на
ион натрия, а центр распределения отрицательного заряда приходится на ион
хлора. В результате, молекулы воды ориентируются таким образом, что вокруг иона
натрия скапливаются отрицательные полюса молекул воды, а вокруг иона хлора —
скапливаются положительные полюса молекул воды.
После того, как мы
насыпали соль в ванну, там образовался солевой раствор. Как вы знаете из курса
химии, молекулы воды являются полярными, так же, как и молекулы поваренной
соли. Центр распределения положительного заряда в поваренной соли приходится на
ион натрия, а центр распределения отрицательного заряда приходится на ион
хлора. В результате, молекулы воды ориентируются таким образом, что вокруг иона
натрия скапливаются отрицательные полюса молекул воды, а вокруг иона хлора —
скапливаются положительные полюса молекул воды.
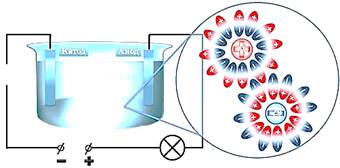 В этом случае, действие
кулоновских сил достаточно велико, чтобы расщепить молекулу поваренной соли. То
есть, молекула распадается на ион натрия и ион хлора.
В этом случае, действие
кулоновских сил достаточно велико, чтобы расщепить молекулу поваренной соли. То
есть, молекула распадается на ион натрия и ион хлора.
Таким образом, в растворе возникают заряженные частицы — ионы. В результате, отрицательные ионы (в данном случае ионы хлора), начинают двигаться к аноду, а положительные ионы (в данном случае ионы натрия) начинают двигаться к катоду. Это есть не что иное, как упорядоченное движение заряженных частиц, то есть электрический ток.
Существует класс веществ, молекулы которых состоят из двух или более частей, таких, что одна часть притягивает один или несколько электронов другой части и приобретает отрицательный заряд, вторая часть при этом заряжается положительно. Почему так происходит – этот вопрос подробно рассматривает химия, нам же важны последствия этого явления.
 Такие вещества называются электролитами. Электролитами являются все растворимые соли, кислоты и
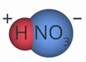
основания. Из курса химии вы знаете, что молекула кислоты состоит из
кислотного остатка и одного или нескольких атомов водорода. Кислотный остаток
является той частью, которая притягивает электроны, атом водорода – частью,
которая отдает электрон (он в атоме водорода всего один), например,
Такие вещества называются электролитами. Электролитами являются все растворимые соли, кислоты и
основания. Из курса химии вы знаете, что молекула кислоты состоит из
кислотного остатка и одного или нескольких атомов водорода. Кислотный остаток
является той частью, которая притягивает электроны, атом водорода – частью,
которая отдает электрон (он в атоме водорода всего один), например, ![]() .
.
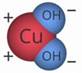
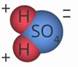
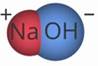 Молекула основания состоит из атома металла и одной
или нескольких гидроксогрупп, состоящих из одного атома кислорода и одного
атома водорода (-ОН). В такой молекуле атом металла отдает электроны,
гидроксогруппа принимает один электрон. Например,
Молекула основания состоит из атома металла и одной
или нескольких гидроксогрупп, состоящих из одного атома кислорода и одного
атома водорода (-ОН). В такой молекуле атом металла отдает электроны,
гидроксогруппа принимает один электрон. Например, ![]() .
.
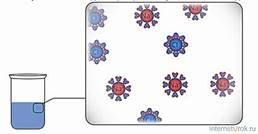 Молекула соли состоит из атома металла и кислотного
остатка. Свойства принимать или отдавать электроны при этом у атома
металла и кислотного остатка сохраняются. Количество электронов, которое
принимает или отдает та или иная группа, соответствует валентности группы
Молекула соли состоит из атома металла и кислотного
остатка. Свойства принимать или отдавать электроны при этом у атома
металла и кислотного остатка сохраняются. Количество электронов, которое
принимает или отдает та или иная группа, соответствует валентности группы
Рассмотрим сказанное на
примере поваренной соли ![]() .
Атом хлора притягивает один электрон атома натрия и заряжается отрицательно,
атом натрия заряжается положительно. В таком состоянии кристалл не проводит
электрический ток, поскольку нет свободных носителей заряда: частицы
зафиксированы в кристаллической решетке.
.
Атом хлора притягивает один электрон атома натрия и заряжается отрицательно,
атом натрия заряжается положительно. В таком состоянии кристалл не проводит
электрический ток, поскольку нет свободных носителей заряда: частицы
зафиксированы в кристаллической решетке.
Что произойдет, если такое вещество поместить в воду? Молекула воды полярна, электроны в ней смещены в сторону атома кислорода, поэтому эта сторона имеет отрицательный заряд, а противоположная – положительный. Противоположные заряды притягиваются, поэтому понятно, что молекулы воды притянутся своей положительно заряженной стороной к атомам хлора, а отрицательно заряженной стороной – к атомам натрия. В некоторый момент сила, с которой молекулы будут притягивать атом, станет достаточной, чтобы атом покинул кристаллическую решетку.
Этот процесс называется электролитическая диссоциация, соль растворяется в воде. Что мы получаем в итоге? Мы получаем множество ионов натрия, заряженных положительно, и ионов хлора, заряженных отрицательно, свободно перемещающихся в воде. Ион – это электрически заряженная частица, представляющая собой атом или группу атомов. Т.е. мы получили свободные носители заряда, а это значит, что при наличии электрического поля раствор может проводить ток.
Чистая вода является диэлектриком, а проводящие свойства она приобретает в процессе электролитической диссоциации. А т.к. дистиллированная вода в природе встречается редко и в ней всегда растворено некоторое количество солей, то мы привыкли считать, что вода проводит электричество. Теперь мы знаем, что, чем более соленая вода, тем лучшим проводником она является.
Подводные лодки и соленая вода
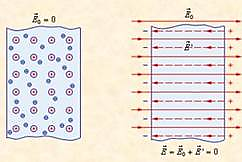
Морская вода содержит большое количество солей, растворенных в ней. Мы уже знаем, что это делает воду хорошим проводником. Проводник является экраном для внешнего электрического поля, он его не пропускает внутрь. Внутри проводника напряженность электрического поля равна нулю.
Какое преимущество это дает подводной лодке? Подводная лодка в морской воде невидима для радаров. Принцип радиолокации состоит в следующем: локатор излучает электромагнитную волну, она отражается от объекта. Локатор принимает отраженное излучение и по его наличию и параметрам устанавливает расположение объекта.
Когда мы говорили о воде как экране электрического поля, мы рассматривали постоянное поле. Распространение электромагнитной волны – более сложный процесс, но и ее морская вода, как хороший проводник, практически не пропускает, таким образом, лодка оказывается невидимой для радаров.
Чтобы узнать, растворимо ли вещество, какие ионы образуются при электролитической диссоциации, какова величина их зарядов, удобно пользоваться таблицей растворимости веществ.
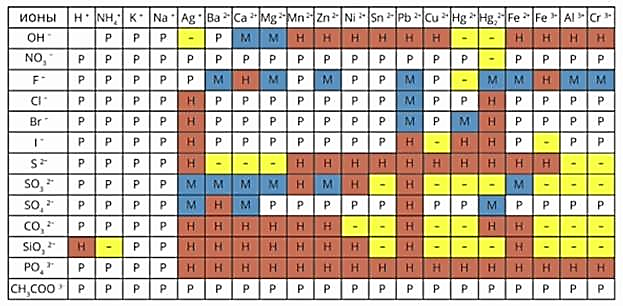
То же происходит в расплавах электролитов с тем различием, что ионы покидают кристаллическую решетку и становятся свободными носителями заряда не вследствие взаимодействия с водой, а вследствие разрушения кристаллической решетки при переходе в жидкое агрегатное состояние.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.