
Лабораторная работа №9. «Измерение заряда одновалентного иона»
Цель работы – определение числа фарадея и заряда электрона.
Приборы и принадлежности: источник тока, секундомер электрическая ванна.
Закон электролиза
Если заряд одновалентного иона равен Ze, где е – элементарный заряд, Z – валентность иона или число электронов. Заряд сообщенный электроду
q = n∙Z∙e, (1)
где n – число атомов.
Масса вещества выделившегося на электроде:
М = n∙m, (2)
где m – масса одного иона.
Используя уровнения (1) и (2) получаем
М= ![]() ∙q. (3)
∙q. (3)
У любых атомов имеющих одинаковое количество вещества количество атомов будет соответсвенно тоже равны N = NA,
NА = 6,023· 10![]() моль
моль![]() (число Авогадро).
(число Авогадро).
Тогда масса иона:
m=![]() , (4)
, (4)
где μ – молярная масса.
Используя уранения (4) и (3) получаем:
М = ![]() (5)
(5)
Величина
![]() , (6)
, (6)
Заряд одновалентного иона будет равен абсолютному значению заряду электрона. Поэтому заряд электрона можно высчитать используя уравнение ниже.
е = ![]() . (7)
. (7)
Ход работы:
1. Медную пластину, используемую в качестве катода нужно в течение 10 минут выдержать в электрической печи и взвесить на весах. Полученную массу М1 нужно записать в таблицу.
2. Катод и анод нужно расположить в электрическую ванну. На отрицательную клемму источника питания нужно подсоединить катод, а на положительную анод.
3. Включите источник тока и секуондомер одномоментно. Пропустите электрический ток через электролит в течение 30 минут.
4. Выключите источник тока и секундомер. Высушите катод в электрической печи и путем взвешивания определите массу М2. Определите разницу масс М1–М2 и запишите в таблицу.
5. Используя уравнение (7) определите заряд электрона. (m =63,5×10-3 кг/моль)
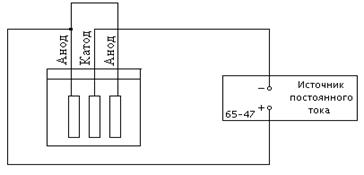
![]() Рис. 1
Рис. 1
Запишите значения в таблицу ниже.
|
М1, кг |
М2, кг |
М, кг |
I, А |
t, c |
К, кг/Кл |
F, Кл/моль |
е, |
|
|
|
|
|
|
|
|
|
Теоретические вопросы
1. Какие проводники называются проводниками первого и второго рода?
................................................................................................................................................................. .................................................................................................................................................................
2. Сформулируйте закон электролиза.
................................................................................................................................................................. .................................................................................................................................................................
3. Объясните связь между числом Фарадея и электрохимической валентностью веществ? В чем заключается физический смысл числа Фарадея.
................................................................................................................................................................. ................................................................................................................................................................. .................................................................................................................................................................
4. Можно ли определить электрохимическую валентность вещества пропуская через электрическую ванну переменный ток?
................................................................................................................................................................ .................................................................................................................................................................
5. Укажите причины возникновения погрешностей в этой работе.
.................................................................................................................................................................
.................................................................................................................................................................
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.