
Технологическая карта урока
Тема урока: Одноатомные спирты
Тип урока: Изучение нового материала
Цель урока: формирование понятия о спиртах, их физических и химических свойствах и влияние на организм.
Задачи урока.
Материалы и оборудование: КОЗы, ситуационные задачи
|
№ п/п |
Этап урока |
Деятельность учителя |
Деятельность учащихся |
Формируемые УУД |
|
I. |
Организационно-мотивационный
|
Приветствие, проверка готовности к уроку, создание позитивного настроя. |
Приветствуют учителя, контролируют свою готовность к уроку.
|
Личностные: самоорганизация. Регулятивные: способность регулировать свои действия, прогнозировать деятельность на уроке. |
|
II |
Актуализация опорных знаний учащихся
|
Напишите структурную формулу метана, этана и один атом водорода замените на -ОН группу. Какие вещества получились?
Чем отличаются полученные вещества от других классов органических соединений? Как можно назвать класс получившихся веществ? Какое определение спиртов вы можете предложить?
|
Отвечают на вопросы и записывают в тетради
А)СН3 – ОН Б)СН3 – СН2 – ОН
Наличием –ОН группы
Спирты
Спирты – органические вещества, в молекулах которых содержится одна или несколько гидроксогрупп (ОН).
|
Личностные: осознание своих возможностей.
Регулятивные: умение регулировать свои действия, взаимодействовать в группе. Познавательные: Умение анализировать, выделять и формулировать задачу; умение осознанно строить речевое высказывание. |
|
III |
Осмысление новых знаний
|
Спирты, в молекулах которых содержится одна гидроксогруппа (ОН), называют одноатомными спиртами. На сегодняшнем уроке мы с вами должны познакомиться и выяснить отличительные особенности, а также некоторые химические свойства одного из важнейших классов органических веществ – спиртов. Тема урока: Одноатомные спирты. Все связывают спирты как алкоголь, справедливо ли такое утверждение? Какую цель мы можем поставить сегодня на уроке? Чем отличаются полученные формулы спиртов друг от друга? Можно вывести общую формулу одноатомных спиртов? Для дальнейшего изучения спиртов вам необходимо поделиться на группы. Раздаются ситуационные задачи и КОЗы. (Приложение 1-3) В группе определите аналитиков, теоретиков, докладчиков. Результатом работы будет опорный конспект. На работу отводится 15 минут. |
Узнать строение, химические и физические свойства.
Количеством СН2- групп
R-OH
Учащиеся делятся на группы и определяют роли аналитиков, теоретиков, докладчиков.
Решают ситуационные задачи и КОЗы, составляют конспект.
|
Личностные: проявление интереса и активности в выборе решения; установление личностного смысла знания. Регулятивные: умение составлять последовательность действий, осуществлять контроль по результату. Познавательные: умение выделять необходимую информацию |
|
|
||||
|
IV |
Закрепление знаний
|
Затем учитель проходит, оценивает опорные конспекты. Организуется выступление групп. Учитель побуждает учащихся других групп участвовать в обсуждении вопросов, задает вопросы, поправляет или сам дает ответы в случае затруднения, дает пояснения.
Тестирование с взаимопроверкой
|
Модельный ответ, см. Приложение 4.
Приложение 5 Модельный ответ- Приложение 6 |
Регулятивные: умение составлять план и последовательность действий, осуществлять контроль по результату. Познавательные: Умение сформулировать алгоритм действия; выявлять допущенные ошибки и обосновывать способы их исправления обосновывать показатели качества конечных результатов. |
|
V |
Рефлексия.
|
Задает вопросы: Разрешили ли вы проблему, поставленную в начале урока? Что на уроке было главным? Что было интересным? Что нового сегодня узнали? Чему научились? Как вы можете использовать полученные знания? |
Учащиеся отвечают на поставленные вопросы. |
Личностные: умение провести самооценку и организовать взаимооценку (прогнозирование и контроль). Регулятивные: построение логической цепочки рассуждений и доказательство.
|
|
VI |
Домашнее задание |
Приготовить сообщение или презентацию: «Влияние спиртов на организм человека» |
Учащиеся записывают домашнее задание. |
|
Приложение 1
КОЗ 1 Одноатомные спирты
|
Во многих зарубежных странах бензин заменяют спиртосодержащим топливом. Возможно, в будущем и вам придется делать выбор между видами топлива для автомобиля. Ответив на вопросы задания, вы сможете сделать правильный выбор. |
Стимул |
|
Используя информационный лист, установите взаимосвязь описанных в тексте явлений с помощью уравнений реакции: 1. реакции горения метанола 2. реакции горения этанола. 3. Определите, к какому типу термохимических реакций относится процесс горения спиртов? 4. Объясните причины использования метилового и этилового спирта, как альтернативу традиционному бензиновому топливу? Приведите не менее двух доказательств. Время – 5 минут |
Задачная формулировка |
|
1. __________________________________________________
2.__________________________________________________
3.__________________________________________________ 4. А) _________________________________________________
Б) _________________________________________________
|
Бланк выполнения задания |
|
Информационный лист Таблица №1, №2.
|
Источник информации |
|
1) 2СН3ОН + 3О2 = 2СО2 + 8Н2О 2) С2Н5ОН + 3О2 = 2СО2 + 3Н2О 3). Так как при горении теплота выделяется – это экзотермическая реакция 4) а) метанол и этанол полностью сгорают без копоти, что предотвращает загрязнение атмосферы; б) теплота сгорания спиртов выше, чем теплота сгорания нефтепродуктов |
Модельный ответ (инструмент проверки)
|
Правильные ответы на 1- 3 задание по 1 баллуПравильно выполненное 5 задание - 2 баллаМаксимальное количество 5 балловОценка соответствует количеству набранных баллов |
Аналитическая шкала (шкала оценивания)
|
Информационный лист
Метанол (метиловый спирт, древесный спирт) СН3ОН
Бесцветная жидкость с характерным запахом, tкип. – 64,7 С0, хороший растворитель, даже в небольших дозах сильный органический яд.
Этанол (этиловый спирт, винный спирт) С2Н5ОН
Бесцветная жидкость с характерным запахом, tкип. – 78,3 С0, смешивается с водой в любых соотношениях, хороший растворитель,в больших дозах сильный органический яд.
Как и большинство органических веществ, спирты в кислороде воздуха горят с образованием углекислого газа и воды. При их горении выделяется много теплоты. Метиловый и этиловый спирты горят почти бесцветным пламенем, так как происходит их полное сгорание.
Таблица № 1
|
Сжигаемое топливо |
Теплота сгорания, кДж/кг |
Сжигаемое топливо |
Теплота сгорания, кДж/кг |
|
Дерево сухое |
4 500 |
Древестный уголь |
8 080 |
|
Торф сухой |
23 000 |
Природный газ |
29 000 |
|
Каменный уголь |
35 000 |
Нефтепродукты |
34 000 |
|
Бурый уголь |
28 000 |
Метиловый спирт |
38000 |
|
Антрацит |
34 000 |
Этиловый спирт |
41 000 |
Таблица №2
|
Сжигаемое топливо
|
Выбросы в атмосферу вредных веществ при сжигании разных видов топлива (т/год) |
||||||
|
Диоксид азота |
Оксид углерода |
Диоксид серы |
Бенз(а)пирен |
Твердые частицы |
Формальдегид, ацетальдегид |
Всего |
|
|
Природный газ |
277762,9 |
29361,2 |
- |
0,0017 |
3,0 |
- |
57127,1 |
|
Мазут (топочный) |
23241,6 |
27974,9 |
153785,5 |
0,018 |
1089,7 |
1200,0 |
209441,7 |
|
Уголь (бурый) |
45114,1 |
530405,3 |
269864,1 |
0,13 |
134365,5 |
2850,0 |
982599,1 |
|
Метиловый спирт |
- |
161,7 |
- |
- |
- |
57,7 |
219,4 |
|
Этиловый спирт |
- |
361,2 |
- |
- |
- |
85,2 |
446,4 |
Приложение 2
КОЗ 2 Одноатомные спирты
|
На просьбу жителей поселка Корфовский уменьшить производство спирта, руководство ответило отказом. С чем это могло быть связано? |
Стимул |
|
В нашей стране идет борьба с алкоголизмом, вводятся ограничения на продажу алкогольных напитков, но производство спирта растет. Объясните данный парадокс. Для этого исследуйте диаграммы на информационном листе и составьте список применения спиртов (не менее пяти) в порядке возрастания значимости.
Время – 5 минут |
Задачная формулировка |
|
Список областей применения спиртов: 1. __________________________________________________ 2.__________________________________________________ 3.__________________________________________________ 4._________________________________________________ Вывод: _________________________________________________
|
Бланк выполнения задания |
|
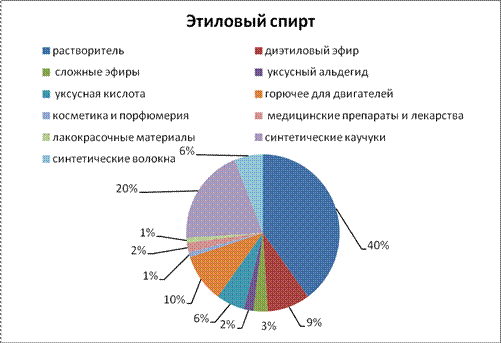
Информационный лист Диаграмма №1, №2.
|
Источник информации |
|
1) растворитель 2). синтетический каучук 3).топливо 4). эфиры 5). медицинские препараты и лекарства Вывод: спирты ценное химическое сырье, доля алкогольной продукции в общем производстве не является основным направлением. |
Модельный ответ (инструмент проверки)
|
Указано 5 областей применения 3 баллаСделан правильно вывод - 2 баллаМаксимальное количество 5 балловОценка соответствует количеству набранных баллов |
Аналитическая шкала (шкала оценивания)
|
Информационный лист
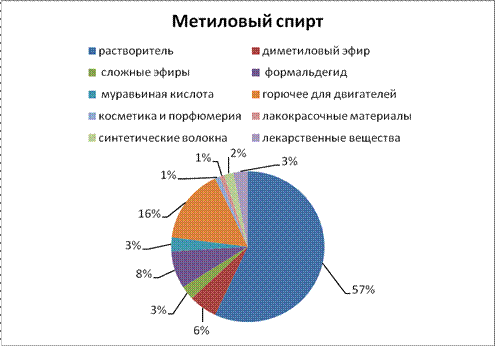 Диаграмма №1
Диаграмма №1
Диаграмма №2
Приложение 3
Ситуационная задача.
Спирты завораживают. Они многообразны. Способны приносить, подобно ядам, пользу и вред.
Имеют загадочную этимологию: слово пришло в наш язык благодаря заимствованию английского spirit (от spiritus — лат. «душа, дух, дыхание»). Применение спиртов во многих сферах деятельности — медицине, косметологии, промышленности — делают эти органические соединения незаменимым продуктом для человека.
Повсеместное использование спиртов в сельском хозяйстве, промышленности, военном деле, транспортной сфере.
Этанол является сырьем для натурального уксуса. Продукт получается при окислении уксуснокислыми бактериями. Аэрирование (принудительное насыщение воздухом) — необходимое условие процесса.
Этанол в пищевой промышленности не единственный спирт. Распространено использование спиртов как сахарозаменителей. Для этого по свойствам подходят маннит, ксилит, сорбит.
Вода, спирт, парфюмерная композиция (концентрат) — основные компоненты парфюмерных продуктов. Они используются в разных пропорциях.
В производстве парфюмерной продукции этанол высшей очистки выступает растворителем душистых веществ. При реакции с водой образуются соли, которые выпадают в осадок. Раствор несколько дней отстаивается и фильтруется.
Опасным ядом является метанол. Он токсично воздействует на сердце, нервную систему. Прием внутрь 30 г метанола приводит к смерти. Попадание меньшего количества вещества — причина тяжелых отравлений с необратимыми последствиями (слепотой).
Предельно допустимая его концентрация в воздухе на производстве — 5 мг/м³. Опасны жидкости, содержащие даже минимальное количество метанола.
Этанол — основа алкогольных напитков. Его получают из сахарной свеклы, картофеля, винограда, злаковых культур — ржи, пшеницы, ячменя, другого сырья, содержащего сахар или крахмал. В процессе производства применяются современные технологии очистки от сивушных масел.
Содержание этилового спирта — основа классификации алкогольных напитков.
1. Составьте список областей применения спиртов.
2. Постройте прогноз развития отравления метанолом.
3. Составьте кластер применения спиртов.
4. Найдите в тексте объяснение процесса аэрирования.
5. Придумайте игру-пантомиму о применении спиртов.
6. Выскажите критическое суждение «Спирты способны приносить, подобно ядам, пользу и вред».
Приложение 4
Модельный ответ
![]()
![]() Физические
Спирты Химические
Физические
Спирты Химические
свойства. свойства.
Среди спиртов нет газов, 1) Горят в кислороде и на воздухе:
это бесцветные жидкости, 2С2Н5ОН + 6О2→ 4СО2↑ + 6Н2О
хорошо растворимы в воде. 2)Взаимодействие с Na
Одноатомные спирты имеют 2С2Н5ОН + 2Na→ 2С2Н5ОNa+ Н2
резкий запах, летучи. Метанол- яд
для человека, вызывает слепоту
или смерть. Этанол- ядовитое нар-
котическое вещество.
Применение.
Одноатомные спирты используют в качестве растворителей, для производства пластмасс, уксусной кислоты, лаков, медикаментов,
Душистых веществ и алкогольных напитков.
Приложение 5
Тест « Спирты» 9 класс
1. Функциональная группа спиртов:
1) –ОН
2) –СОН
3) –СООН
4)–С=О
![]() О
О
2. Какое органическое соединение является гомологом этанола?
1) СН4 2)СН3ОН
3)С6Н5ОН 4)С2Н4(ОН)2
3. В результате горения этанола в кислороде образуется
1) С и Н2О 2)СО и Н2О
3)СО2 и Н2О 4)С2Н2 и Н2О
4.Общая формула предельных одноатомных спиртов:
1) R-О- R![]()
![]() 2) R-
2) R-![]() СООН
СООН
3) R-СООR 4) R-ОН
5. Количество коэффициентов в уравнении реакции горения метанола равно:
1) 4 2) 5
3) 6 4) 7
Приложение 6
Модельный ответ
|
1 |
1 |
|
2 |
2 |
|
3 |
3 |
|
4 |
4 |
|
5 |
3 |
Оцените работу.
«5»- 5 правильных ответов
«4»-4 правильных ответов
«3»-3 правильных ответа
«2»- меньше двух правильных ответов.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.