
План урока
|
Раздел: Газовые законы Long-term plan unit: Gas laws |
Школа: ГУ «Карабалыкская средняя школа имени Абая Кунанбаева отдела образования акимата Карабалыкского района» School: № 2
|
||||||||||||||||
|
Дата: Date: 13.11.2019 |
ФИО учителя: Уразбаева С.У. Teacher name: Syrkul Urazbaeva |
||||||||||||||||
|
Класс: Grade:10
|
Количество учащихся: |
|
|
||||||||||||||
|
Тема урока |
Основное уравнение идеального газа. Ideal gas laws |
|
|
||||||||||||||
|
Цели Learning objectives обучения |
10.3.2.1 - применять уравнение состояния идеального газа при решении задач To apply the ideal gas law in problem solving |
||||||||||||||||
|
Цели урока Lesson objectives |
степень усвоения знаний по теме «Уравнение состояния идеального газа» и формирование практических умений по их применению. |
||||||||||||||||
|
Критерии оценивания Success criteria |
Записывают уравнение состояния газа и характеризуют все параметры уравнения. Решают задачи, в которых нужно использовать уравнения состояния газа. |
||||||||||||||||
|
Языковые цели Language objectives |
Вовлечение учащихся в диалог-дискуссию. Полезные фразы для построения диалога: при переходе газа из одного состояния в другое меняются следующие макроскопические параметры… Учащиеся могут… В устном или письменном виде объяснить причинно-следственную взаимосвязь и описать зависимость Предметная лексика и терминология: взаимодействие, движение, идеальный газ, давление, объем, температура, interaction, motion, Ideal gas, pressure, volume, temperature Серия полезных фраз для диалога/письма: нормальному состоянию газа соответствует давление 105 Па(760 мм.рт.ст); температура 273 К. Нагревание... повышает кинетическую энергию частиц. |
||||||||||||||||
|
Привитие ценностей Cross-curricular links
|
-Проявлять уважение к одноклассникам при совместной работе. -Развивать самостоятельность в работе, выработать необходимые навыки для обучения на протяжении всей жизни. |
||||||||||||||||
|
Межпредметные связи |
С химией – повторение ранее изученного материала. |
||||||||||||||||
|
Навыки ИКТ ICT skills |
Использование презентаций на интерактивной доске. |
||||||||||||||||
|
Предварительные знания Previous learning
|
Учащиеся знакомы со строением тел, умеют работать с таблицей Менделеева. |
||||||||||||||||
|
Ход урока |
|||||||||||||||||
|
Этапы урока Stages of the lesson |
Запланированная деятельность на уроке Planned activities at the lesson
|
Ресурсы Resources |
|||||||||||||||
|
Начало Beginning
0-2 мин
3-15 мин |
1. Приветствие учащихся. Organizational moment to reacquaint students with the lesson objectives, success criteria, and answer any questions from the previous lesson. Презентация 2. Активизация мыслительной деятельности: В начале урока: Проверим усвоение изученной темы с использованием дидактической игры «Домино». Ученикам предлагается комплект физического «домино» по теме урока. Они отыскивают карточку №1 (в данном случае с вопросом «Что называют молярной массой?» и ищут на ее вопрос в общей массе карточек домино карточку с ответом; найдя, приставляют ее к первой карточке. На правой стороне приложенной карточки написан следующий вопрос, к которому учащимся опять нужно найти карточку с ответом, и т. д. Получается «цепочка» |
Приложение 1
|
|||||||||||||||
|
Середина урока Middle
16-25 мин
26-38 мин
|
Презентация Первоначальная проверка понимания Решение задач на доске.
1. Определить массу водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если температура газа равна 17 °С. Дано: V = 20 л, р = 830 кПа, t = 17 °C, М = 2·10-3 кг/моль, R = 8,31 Дж/(моль·К). Найти: m -? Решение
Дополнительно. В баллоне находится газ под давлением 40 Па и при температуре 27 °С. Когда из баллона выпустили 3/5 газа, содержавшегося в нем, его температура понизилась до -33 °С. Определить давление газа, оставшегося в сосуде.
Задачи решаются самостоятельно учениками
|
Приложение 2
|
|||||||||||||||
|
Конец урока End
1 мин |
Подведение итогов урока. Рефлексия. Стр.181 Домашнее задание прочитать параграф 31, выучить формулы Homework: solving problems |
|
|||||||||||||||
|
Дифференциация |
Оценивание |
Здоровье и
соблюдение техники безопасности |
|||||||||||||||
|
Все учащиеся будут: Знать, как связаны основные параметры газа, будут уметь использовать основную формулу
Некоторые учащиеся будут: Связывать полученные знания с реальными жизненными ситуациями и умело использовать правила сложения для конкретных физических величин.
|
Самооценивание Оценивание учителем |
При обсуждении результатов работы в группах и коллективной, развивается уважение к чужому мнению, умение выражать свои мысли и общаться должным образом со сверстниками и одноклассниками. |
|||||||||||||||
|
Рефлексия по уроку Были ли цели урока/цели обучения реалистичными? Все ли учащиеся достигли ЦО? Если нет, то почему? Правильно ли проведена дифференциация на уроке? Выдержаны ли были временные этапы урока? Какие отступления были от плана урока и почему? |
|
||||||||||||||||
|
|
|||||||||||||||||
|
Общая оценка Какие два аспекта урока прошли хорошо (подумайте как о преподавании, так и об обучении)? 1:
2:
Что могло бы способствовать улучшению урока (подумайте как о преподавании, так и об обучении)? 1:
2:
Что я выявил(а) за время урока о классе или достижениях/трудностях отдельных учеников, на что необходимо обратить внимание на последующих уроках?
|
|||||||||||||||||
|
|
Что называют молярной массой? |
|
Молярной массой называют массу одного моля вещества |
Чему равно нормальное атмосферное давление? |
|
Нормальное атмосферное давление равно 105 Па |
Перечислить макроскопические параметры состояния идеального газа |
|
Макроскопические параметры: р – давление, V – объем, Т - температура |
Перечислите единицы измерения давления, объема и температуры в СИ |
|
Давление измеряют в Па, объем в м3, температуру в К. |
Какое уравнение называют уравнением состояния? |
|
Уравнение, выражающее связь между макроскопическими параметрами состояния вещества, называется уравнением состояния этого вещества |
В чем заключается основная задача МКТ вещества? |
|
Основной задачей МКТ является нахождение уравнения состояния того или иного тел |
Какой вид имеет уравнение Менделеева-Клапейрона? |
|
|
Как формулируется закон Авогадро?
|
|
При одинаковых температурах и давлениях в равных объемах любых идеальных газов содержится одинаковое число молекул |
Сформулируйте закон Дальтона |
|
Давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений этих газов
|
Какое давление называют парциальным? |
|
Это давление, которое имел бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуре. |
В чем заключается объединенный газовый закон? |
|
Отношение произведения давления и объема идеального газа к его абсолютной температуре есть величина постоянная для данной массы данного газа. |
В каком виде объединенный газовый закон представил Клапейрон? |
|
|
Чему равна температура таяния льда и кипения воды при нормальном давлении по термодинамической шкале? |
|
Т л = 273 К Т в = 373 К |
Какой прибор служит для измерения давления газа? |
|
Манометр |
|
Решить задачи:
1. 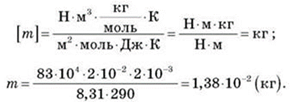 Определить массу
водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если
температура газа равна 17 °С.
Определить массу
водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если
температура газа равна 17 °С.
2.
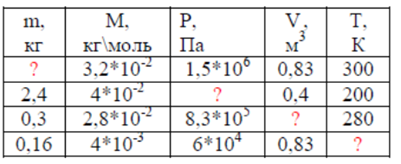
Определить m, P,V, T(Ответы: m=16 кг; Р=249300 Па;
V=0,03 м3; Т=150К )
3.
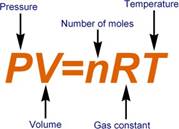
p – pressure (Pa)
• T – absolute temperature (K)
• V – Volume (m3)
• v – velocity (m/s) (can be written as c)
• <v> - average velocity (m/s)
• Na – Avogadro constant (6.02 x 1023)
• Mr – relative molecular mass (mass in grams of a mole of the molecule)
• n – amount of substance in moles
• N – number of molecules
• m0 – mass of one molecule
• R – universal gas constant (8.31 J K-1 mol-1)
• k – the Boltzmann constant (1.38 x 10-23 J K-1)
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.