
Тақырыбы: Резерфорд тәжірибесі. Атомның планетарлық моделі.
Сыныбы: 9
Түрі: Жаңа сабақ.
Әдісі: Сұрақ -жауап, ЛТС, интеграция, ақпараттық технология, тест, есептер шығару.
Сабақтас үш бағытты МАҚСАТ:
а) білімділік - танымдық: Оқушыларға Резерфорд тәжірибесінің мағынасын, атомның планетарлық моделі мен атом ядросының құрамы туралы жаңа тақырыпты ақпараттық, интеграциялық, инновациялық технология көмегімен меңгерту.
ә) дамытушылық: Берілген тапсырмадағы ситуациядан шығу әрекеті арқылы оқушылардың оқу-танымдық құзыреттіліктерін дамыту. Пән негізіндегі ғылыми тұжырымдарды көре білу, сезіну, түйсіну дағдыларын дамыту.
б) тәрбиелік: Әрекет барысында бір-бірінің пікірін тыңдауға, сыйлауға, тіл тазалығын сақтауға тәрбиелеу.
Мақсаттан нәтижеге жету жолындағы МІНДЕТТЕР:
Сабақтың көрнекіліктері: Ақпараттық технология, Менделеев кестесі, үлестірмелер, ғалым А.Эйнштейн суреті, электронды оқулықтар.
Сабақтың барысы:
7. Үйге тапсырма 1 мин
8. Қорытындылау 3 мин
1. Сыныпқа кіріп оқушылармен амандасып, түгендеймін. Оқушылардың қызығушылығын ояту.
2. «Ой шақыру»- үй тапсырмасын сұрақтар арқылы сұрау
1. 1896 жылы француз ғалымы Беккерель нені анықтады?
2. 1898 жылы қандай жаңалық ашылды ?
3. Радиоактивті элементтер деген не?
4. Радиоактивті сәулелер дегеніміз не?
5. Альфа, бета, гамма сәуле деген не?
6. Менделеев кестесінде радиоактивті элементтер қай реттен басталады?
7.Рентгендік сәулелер қайда қолданылады?
Сабақта жауап іздейтін сұрағымыз:
Атом күрделі болса, құрамы қандай?
Атом қандай бөлшектерден тұрады және олар қалай орналасқан ?
3. ЛТС
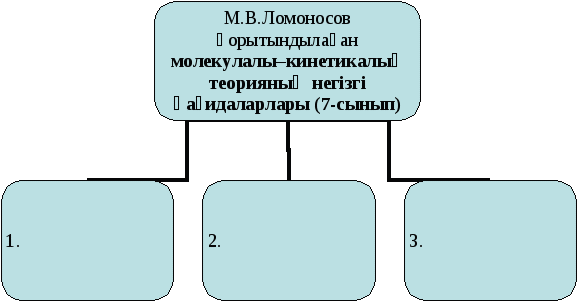
4. Заттар қалай құралған ЛТС құру
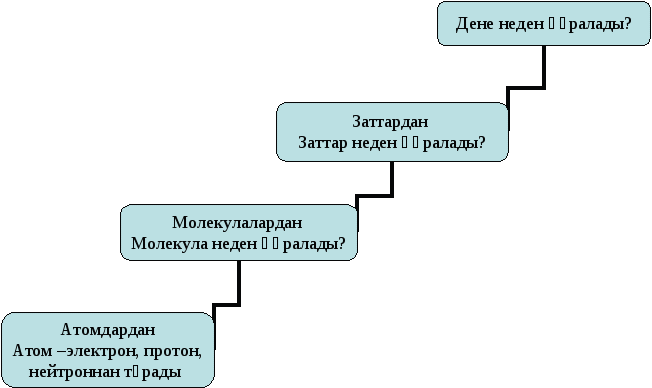
Орыс ғалымы А.Ф.Иоффе мен американдық ғалым Р.Милликеннің бір-біріне тәуелсіз жүргізген, электр зарядтарын бөлудегі іргелі тәжірибелеренің негізінде келесі нәтижелер алынды.
Электр зарядының бөліну шегі бар. Әрі қарай бөлінбейтін ең аз теріс заряды бар бөлшек электрон деп аталады. Осы бөлшек атомның қабықшасын құрайды.
ХХ ғасырдың басында ғалымдардың алдына мынадай мәселе қойылды: Атом күрделі болса, ол қалай құралған ? Атом қандай бөлшектерден тұрады және олар қалай орналасқан ?
1911 жылы Эрнест Резерфорд және оның шәкірттері альфа бөлшектерінің өте жұқа алтын және платина пластинкаларынан өтуін зерттеді. 9-сынып оқулығынан тәжірибе көрсетіледі.
Көптеген тәжірибе нәтижесін талдай келіп, 1911 жылы Резерфорд Күн жүйесіне ұқсас атомның планетарлық моделін ұсынды. 7-сынып оқулығынан көрсетілім.
Ядро атом көлемінің өте кішкене орталық бөлігін алып тұрады. Ядроның диаметрі 10-12-10-13см, ал атомның диаметрі 10-8см шамасында. Егер атомның көлемін футбол алаңының аумағындай үлкейтетін болсақ, атом ядросының көлемі футбол алаңына түсіп қалған шие дәніндей ғана болар еді.
Схема түсіндіріледі.

 электрон
электрон
![]() ядро
ядро
![]()
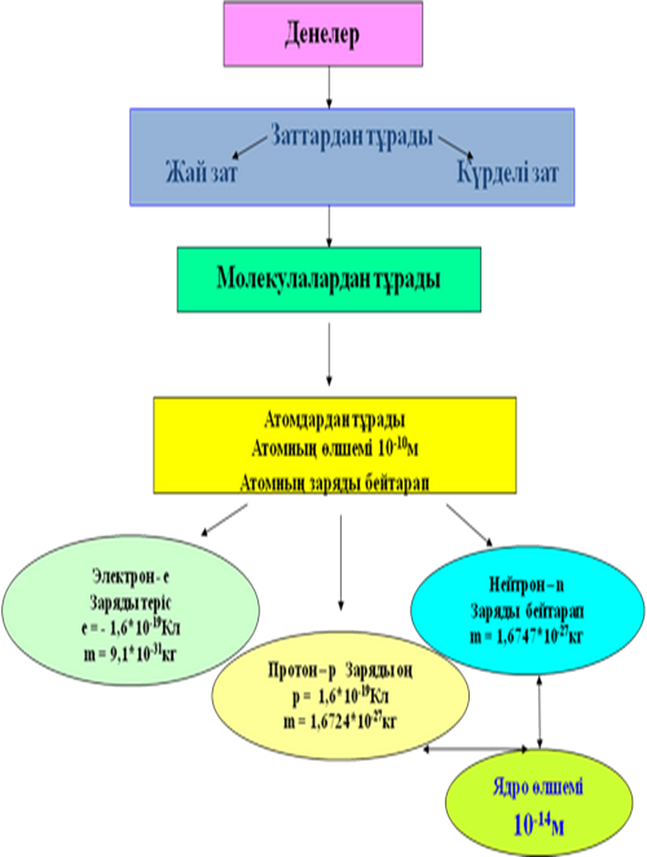
Атомдар қалыпты жағдайда бейтарап болғандықтан, электрондардың заряды мен ядроның заряды бірін-бірі теңгеріп тұрады.
Атом ядроларының заряды qя=+Z*e
Z - элементтің Менделеев кестесіндегі реттік саны
е- элементар заряд
Ядро құрамына кіретін оң зарядталған бөлшектерді протондар деп атайды.
Қалыпты жағдайда атом ядросының оң зарядын орбиталдық электрондардың теріс заряды теңгеріп тұрады. Сондықтан электрондық қабықшадағы теріс зарядтардың саны кері таңбамен алынған ядро зарядына тең. q=-Z*e
Қорытынды:
1. Әрбір электронның немесе протонның заряды бір элементар зарядқа тең
(е=1,6*10-19Кл );
2. Кез-келген элемент атомының ядросындағы протондар саны сол элементтің Менделеев кестесіндегі Z реттік санына тең.
1932 жылы Резерфорд шәкірті Д.Чэдвик ядро құрамына кіретін жаңа бөлшек нейтронды ашты. Сөйтіп, кез-келген элемент атомының ядросы екі түрлі бөлшектен: протондар мен нейтрондардан тұрады. Оларды жалпылап нуклондар деп атайды, ал тұтас ядроны нуклид дейді.
Ядродағы протондар мен нейтрондардың жалпы санын А әрпімен белгілейді. А санын массалық сан деп атайды.
zХA : Х- химиялық элемент; Z-реттік номері(заряд саны); А-массалық сан
N=A-Z
N-нейтрондар саны
Бір-бірінен тек ядросындағы нейтрондар санына қарай ажыратылатын элемент түрлерін изотоптар деп атаймыз.
Мысалы: сутектің 3 түрлі изотопы бар. 1Н1-жеңіл сутек, 1Н-ауыр сутек дейтерий, сирек кездеседі , 1Н3-тритий кездеспейді.
Элемент изотоптарының химиялық қасиеттері бірдей, сондықтан оларды химиялық тәсілмен ажыратуға болмайды. Изотоптарды тек массалық сандарына қарай ажыратып, сезімтал құралдардың жәрдемімен бөліп алады.
1р1-протон; 0n1-нейтрон; -1е0-электрон
Жаңа сабақты бекіту:
№1. 2 Х4-Не гелий p=2, A=4, N=2
79Х197-Аu алтын p=79, A=197, N=197-79=118
6Х56-Ғе темір p=6, A=56, N= 56-6=50
№2. Тақырыптық тест
І нұсқа
1.Заттың бөлінбейтін ең ұсақ бөлшегі атомдар деп атаған ғалым?
А.Ломоносов Б.Демокрит
В. Аристотель Г.Резерфорд
2. Атом қанша элементар бөлшектен тұрады ?
А.1 Б.2 В.3 Г.4
3. Ең жеңіл элемент ?
А. Сутегі Б.Уран В.Оттегі Г. Гелий
4.Электронның заряды қандай ?
А. оң Б.теріс В.Бейтарап Г.оң,теріс
5.Атомдар қай кезде пайда болады ?
А.Молекулалардан Б.Атомдардың бірігуінен
В.Заттардың бірігуінен Г.Молекулалар ыдырағанда
ІІ нұсқа
1. Табиғи қанша атом бар ?
А. 95 Б.92 В.93 Г.94
2. Ядрода қандай бөлшектер орналасады ?
А. e,p Б. e,n В. p,n Г. e,p,n
3. Протонның заряды қандай ?
А. оң Б.теріс В.Бейтарап Г.оң,теріс
4. Нейтронның заряды қандай ?
А. оң Б. Бейтарап В. теріс Г.оң,теріс
5. Денелер қалай құралады ?
А.Молекулалардан Б.Атомдардың бірігуінен
В. Молекулалар ыдырағанда Г. Заттардың бірігуінен
Қорытындылау
Үйге тапсырма: §53 ЛТС құру
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.