
КГУ « Опорная школа (ресурсный центр) на базе гимназии № 9 »
Краткосрочный (поурочный)
план
«Типы гибридизации: sp-, sp2-, sp3-.
«Лабораторная работа №1
«Составление моделей веществ с ковалентной связью (N2, О2,
алмаз)»
|
Раздел |
|
|
|
Ф.И.О (при его наличии) педагога |
Кондратова Тамара Сергеевна |
|
|
Дата |
|
|
|
Класс 10 |
Количество присутствующих |
Количество отсутствующих |
|
Тема урока |
Типы гибридизации: sp-, sp2-, sp3-. Лабораторная работа №1 «Составление моделей веществ с ковалентной связью (N2, О2, алмаз)» |
|
|
Цели обучения в соответствии с учебной программой |
10.1.4.4 объяснять различие видов гибридизации; 10.1.4.5 объяснять взаимосвязь строения и свойств веществ. |
|
|
Цели урока |
-уметь объяснять образование π –связи и Ϭ –связи в гибридных в атомных орбиталях при sp, sp2, sp3 гибридизации. - называть типы гибридизации и их основные характеристики. -прогнозировать свойства вещества, зная его строение. |
|
|
Критерии |
-объясняет образование π –связи и Ϭ –связи в гибридных в атомных орбиталях при sp, sp2, sp3 гибридизации. -называет типы гибридизации и их основные характеристики. -прогнозирует свойства вещества, зная его строение.
|
|
Ход урока
|
Этап урока/ время |
Действия педагога |
Действия ученика |
Оценивание |
Ресурсы |
|
Начало урока/3 мин
Стадия вызова 7 минут |
Организационные дейстия Приветствие учителя. Дарит каждой группе связку шаров ( 3 шара) Создание спокойной, деловой обстановки.
Актуализация знаний (Прием Deja vu – уже знакомое ранее+ новое, незнакомое) Приложение №1 Учащимся предлагается ответить на вопросы опираясь на схему (фронтальный опрос) Вопросы дифференцированы ( для всех учеников и ООП) Ученикам предлагает сформулировать тему и цель урока ( для всех учеников и ООП)
|
Рассаживаются рабочим группам получают воздушные шары.
Отвечают на вопросы |
Жетон правильного ответа
|
http://ae01.alicdn.com/kf/HTB1XhdWsb9YBuNjy0Fgq6AxcXXaH/25-50.jpg
http://img.likeness.ru/36/98/3698/1454218209.jpg
https://slide-share.ru/khimiyaprepodavateldocent-kafedri-organicheskoj-i-ehkologicheskoj-150386
https://www.medius.ru/catalog/uchebnye_klassy/kabinet_khimii/posobiya_na_pechatnoy_osnove/khimiya_10_11_klass_20_tabl_98kh68_sm.html |
|
Середина урока/
Стадия осмысления 7 мин выполнение + 5 мин представление + 4 мин оценивание
10 мин
5 мин
|
Изучение нового материала: Предлагает ученикам работу в группах по информационным листам с просмотром видеоресурсов с использованием приема Денотантный граф
|
Рисуют постер, готовят выступление, моделируют типы гибридизации с воздушными шарами
|
Чек –лист Приложение 8 взаимооценивание
|
https://www.youtube.com/watch?v=z1VB_Y4BbtA Материал учебника параграф 12, стр 68-71 Информационные листы Презентация к уроку. 1 группа -0-3 мин sp3-гибридизация 2 группа – 3.05 -5.59 мин sp2-гибридизация 3 группа – 6-9 мин sp-гибридизация |
|
Выполнение задания на закрепление Учитель контролирует работу каждой группы, особое внимание и помощь – детям с ООП Приложение №5 Задания уровня А В С Приложение№ 6 Задания на ФГ Приложение № 7 Задния для учеников с ООП
|
Учащиеся выполняют задания АВС, на ФГ (повышенная мотивация) Учащийся с ООП
работает с индивидуальным заданием. |
«КАРУСЕЛЬ» взаимооценивание |
|
|
|
Цель работы: прогнозирует свойства вещества, зная его строение.
|
Работают в группах каждый со своим заданием, делают вывод по цели Лабораторной работы |
Самооценивание, словесно |
https://sitekid.ru/imgn/215/1/23.jpg http://cohifi.com/img/9913-almaznyie-kowalientnaia-kristallitchieskaia-struktura-model-kit-d.jpg набор объемных моделей |
|
|
Окончание урока /4 мин |
Подведение итогов урока. Рефлексия 1. Три важных открытия для вас на уроке 2. Сократите до двух важных 3. Сократите до 1 слова Д/З параграф 12 стр. 64 упражнения №7, 8( письменно) стр.71 вопросы 1-6 (устно) |
Пишут ответы на стикерах «3+2+1» |
самооценивание |
|
Приложения к уроку
Приложение 1 Вопросы на актуализацию знаний Deja vu по таблице
1. В чем отличие двойных и тройных связей?
2. Покажите практически ( при помощи воздушных шаров) перекрывание орбителей в разных плоскостях ( вдоль линии и вне линии, соединяющие центры атомов.)
3. Назовите основные характеристики одинарной, двойной и тройной связи.
Приложение 2 ИНФОРМАЦИОННЫЙ ЛИСТ к уроку
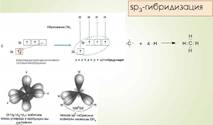 sр3-гибридизация -
это смешение одной 2s- и трех 2р-орбиталей и образование из них
четырех новых одинаковых орбиталей, каждая из которых на одну четверть
сохраняет свойства s-орбитали и на три четверти — свойства р-орбиталей.
sр3-гибридизация -
это смешение одной 2s- и трех 2р-орбиталей и образование из них
четырех новых одинаковых орбиталей, каждая из которых на одну четверть
сохраняет свойства s-орбитали и на три четверти — свойства р-орбиталей.
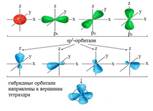
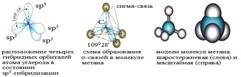
В результате sр3-гибридизации возникает четыре одинаковых гибридных облака, которые направлены к вершинам тетраэдра, в центре которого находится атом углерода.
Электронные облака взаимно отталкиваются и располагаются в пространстве максимально далеко друг от друга. Углы между этими орбиталями – тетраэдрические, равные 109°28'.
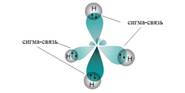
Вершины электронных орбиталей могут перекрываться с орбиталями других атомов. Если электронные облака перекрываются по линии, соединяющий центры атомов, то такую ковалентную связь называют (сигма) σ-связью. При образовании простейшей органической молекулы метана sр3-гибридные облака атома углерода перекрываются с 1s-облаками четырех атомов водорода. На каждой sр3-гибридной орбитали находится по одному электрону. Эти электроны и участвуют в образовании σ-связей с атомами водорода.
Рисунки с сайта https://himija-online.ru/wp-content/uploads/2015/11/%D0%BC%D0%B5%D1%82%D0%B0%D0%BD5.jpg
Информация с сайта https://himija-online.ru/organicheskaya-ximiya/gibridizaciya/tipy-gibridizacii-atoma-ugleroda.html
Приложение 3 ИНФОРМАЦИОННЫЙ ЛИСТ к уроку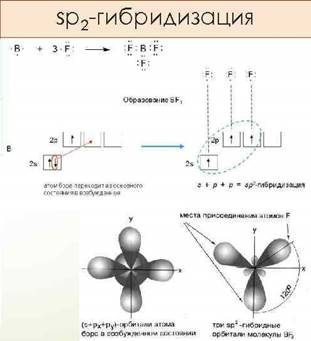
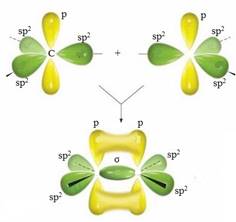 sр2-гибридизация При sр2-гибридизациии участвуют одна 2s- и две 2р-орбитали, образуя три sр2-гибридных облака. Эти sр2-орбитали расположены в
одной плоскости под углом 1200 друг к другу и направлены к вершинам
треугольника. Образование трех sр2-гибридных орбиталей В непредельных
углеводородах ряда этилена два атома углерода, находящиеся в состоянии
sр2-гибридизации стоят всегда рядом. Между ними за счет обычного линейного
перекрывания sр2-гибридных орбиталей возникает ковалентная связь
(σ-связь). Одна p-орбиталь остается негибридизованной и располагается
перпендикулярно плоскости sр–гибридных орбиталей. Верхняя половина р-орбитали
находится над плоскостью, нижняя половина – под плоскостью. Вторая связь также
образуется между двумя углеродными атомами. Связь образуется в результате
бокового перекрывания краев негибридизованных 2рорбиталей и называется
π-связью.Оставшиеся две sр2-орбитали
у каждого углеродного атома используются для образования σ–связей с атомами водорода.
sр2-гибридизация При sр2-гибридизациии участвуют одна 2s- и две 2р-орбитали, образуя три sр2-гибридных облака. Эти sр2-орбитали расположены в
одной плоскости под углом 1200 друг к другу и направлены к вершинам
треугольника. Образование трех sр2-гибридных орбиталей В непредельных
углеводородах ряда этилена два атома углерода, находящиеся в состоянии
sр2-гибридизации стоят всегда рядом. Между ними за счет обычного линейного
перекрывания sр2-гибридных орбиталей возникает ковалентная связь
(σ-связь). Одна p-орбиталь остается негибридизованной и располагается
перпендикулярно плоскости sр–гибридных орбиталей. Верхняя половина р-орбитали
находится над плоскостью, нижняя половина – под плоскостью. Вторая связь также
образуется между двумя углеродными атомами. Связь образуется в результате
бокового перекрывания краев негибридизованных 2рорбиталей и называется
π-связью.Оставшиеся две sр2-орбитали
у каждого углеродного атома используются для образования σ–связей с атомами водорода.
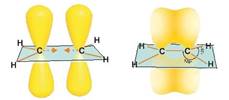
Рисунки с сайта https://himija-online.ru/wp-content/uploads/2015/11/%D0%BC%D0%B5%D1%82%D0%B0%D0%BD5.jpg
Информация с сайта https://himija-online.ru/organicheskaya-ximiya/gibridizaciya/tipy-gibridizacii-atoma-ugleroda.html
 Приложение
4 ИНФОРМАЦИОННЫЙ ЛИСТ к уроку
Приложение
4 ИНФОРМАЦИОННЫЙ ЛИСТ к уроку
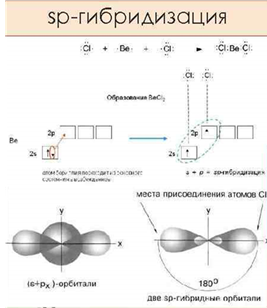
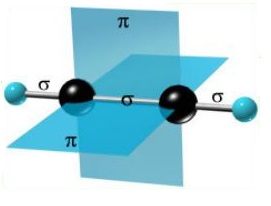
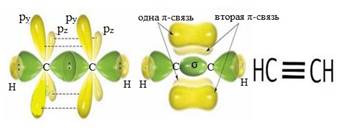
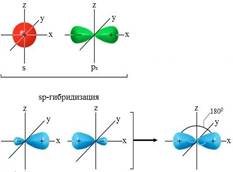
sр-гибридизация
Sр-гибридизацию рассмотрим на примере простейшей молекулы, содержащей тройную связь — молекуле ацетилена. В этом случае происходит гибридизация одной 2s- и одной 2р-орбиталей с образованием двух sp-гибридных орбиталей, которые располагаются под углом 1800. Оставшиеся негибридизированными р-орбитали располагаются перпендикулярно к этой прямой и друг к другу. Эти р-орбитали участвуют в образовании π-связей.
Рисунки с сайта https://himija-online.ru/wp-content/uploads/2015/11/%D0%BC%D0%B5%D1%82%D0%B0%D0%BD5.jpg
Информация с сайта https://himija-online.ru/organicheskaya-ximiya/gibridizaciya/tipy-gibridizacii-atoma-ugleroda.html
Приложение 5 Задания формативного оценивания уровня А В С
|
Раздел/тема |
10.1 С Химическая связь |
|
Цель обучения |
10.1.4.4 объяснять различие видов гибридизации; 10.1.4.5 объяснять взаимосвязь строения и свойств веществ |
|
Критерий оценивания |
Обучающийся умеет объяснять образование π –связи и Ϭ –связи в гибридных в атомных орбиталях при sp, sp2, sp3 гибридизации. - называет типы и основные характеристики sp, sp2, sp3 гибридизации. -прогнозирует свойства вещества, зная его строение |
|
Уровень мыслительных навыков |
понимание, анализ, оценка |
Уровень А Задание 1 Подберите характеристику типа гибридизации из предложенных определений и впишите в пустые колонки таблицы
|
|
Тип гибридизации |
Характеристика |
|
1 |
sp |
|
|
2 |
sp3 |
|
|
3 |
sp2 |
|
Определения:
образованы из одной s орбитали и трех p орбиталей,
образованы из одной s орбитали и двух p орбиталей,
образованы из одной s орбитали и одной p орбитали,
образованы из двух s орбиталей и трех p орбиталей.
3 балла
Уровень В Задание 2
Дано органическое вещество:
5 4 3 2 1
СН=- С –СН2 СН = СН СН2 ОН.
а) Опираясь на органическое вещество ,заполните таблицу:
|
№ |
Порядковый атом углерода |
С1 |
С3 |
С5 |
|
1 |
Типы гибридизации |
|
|
|
|
2 |
Количество π-связей |
|
|
|
|
3 |
Количество Ϭ –связей |
|
|
|
|
4 |
Атомы, участвующие в процессе гибридизации (укажите номер ) |
|
|
|
|
5 |
Пространственное строение атома углерода |
|
|
|
3 балла
Задание 3 В данной таблице показаны основные характеристики разных видов гибридизации по четырем важным параметрам – расположение электронных облаков в пространстве, тип гибридизации, длина связи и геометрия молекулы в хаотичном порядке. Выберите правильный вариант для каждого для каждого типа гибридизации:
|
|
тип гибридизации |
|
Расположение электронных облаков в пространстве |
|
Длина связи |
|
Геометрия молекулы |
|
1 |
sp |
1 |
|
1
|
0,154 нм |
1
|
Линейная |
|
2 |
sp3 |
2 |
|
2 |
0,120 нм |
2
|
Тетраэдр |
|
3 |
sp2
|
3 |
|
3
|
0,134 нм |
3
|
Плоская |
A) 1331 B) 1312 C) 2112 D) 2233 E) 1323 F) 3223
sp______________ sp2___________________ sp3______________________
3 балла
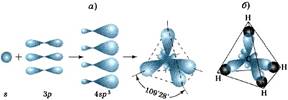

Уровень С задание 4
При образовании химической связи электронные облака атома углерода претерпевают изменения, которые вы можете увидеть на рисунках снизу.
а)Предположите, почему происходят такие изменения? Аргументируйте свое предположение. ________________________________________________________________________________________________________
2 балла
б) От чего зависит пространственная геометрия молекул? Можно ли по пространственному строению молекулы предсказать его химические свойства?
________________________________________________________________________________________________________
1 балл

 Приложение 6 Задание на
Функциональную Грамотность
Приложение 6 Задание на
Функциональную Грамотность
Реализуемые цели: объясняют образование π –связи и Ϭ –связи в гибридных в атомных орбиталях при sp, sp2, sp3 гибридизации; называют основные типы гибридизации и их основные характеристики
|
Задание Школьники наряжали школу к празднику воздушными шарами. Юные химики Дамир и Коля помогали классу. Мальчики заметили, что связанные шарики стараются как можно сильнее равноудалиться один от другого, особенно, если связывать их по три или четыре шара. Причем это положение связанных шаров было очень устойчивое и напоминало мальчикам гибридизованные орбитали атома углерода, о которых они уже знали из курса химии. «Теперь стало ясно, для нужна гибридизация атомных орбиталей» - подумал Коля. А)Опираясь на рисунки и схемы, выполните задания ниже: |
|
||
|
1.Объясните понятие гибридизации атомных орбиталей. |
|
||
|
2.Применяя знания о гибридизации, нарисуйте молекулу этана. |
|
||
|
3.Сравните типы гибридизации и назовите параметры, по которым они отличаются. |
|
||
|
4.Докажите выгодность гибридизованных облаков по отношению к негибридизованным. |
|
||
|
В) При образовании химической связи электронные облака атома углерода претерпевают изменения, которые вы можете увидеть на рисунке справа. |
|
||
|
Предположите, почему происходят такие изменения? |
|
||
|
Аргументируйте свое предположение |
|
||
|
Критерий оценивания |
|
Дескриптор |
балл |
|
объясняют образование π –связи и Ϭ –связи в гибридных в атомных орбиталях при sp, sp2, sp3 гибридизации; называют основные типы гибридизации и их основные характеристики
|
-объясняет понятие гибридизации -зарисовывает молекулу метана -сравнивает типы гибридизации -называет основные параметры гибридизации -доказывает выгодность гибридизованных облаков -выдвигает гипотезу причины гибрдизациии подтверждает ее аргументами |
2 б 1б 1б 1б 2б 3б |
|
.
Пример предполагаемого открытого ответа: Изменения происходят для выравнивания энергии разных электронных облаков. Такое состояние наиболее энергетически устойчивое Сигма – связи образуются при перекрывании облаков вдоль линии, проходящей через ядра атомов. Пи – связи возникают при перекрывании облаков по обе стороны от линии, соединяющей ядра атомов.
Приложение 7 Задание для детей с ООП
Реализуемые цели: называют основные типы гибридизации и их основные характеристики
• индивидуальное
• один шаг выполнения
• дополнительное время
• помощь учителя
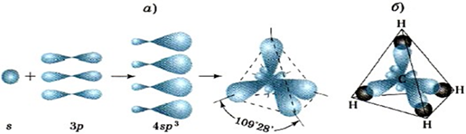
Задание 1 Рассмотрите внимательно рисунок и ответьте на вопросы теста:
1)Какой тип гибридизации показан на рисунке?
а)sp- б)sp2- в) sp3- 2 балла
2)Молекула какого вещества показана на рисунке под буквой б)?
а) метан б) вода с) углекислый газ 1 балл
3)Сколько s –электронных облаков показано на рисунке?
а) 1 б) 2 с)3 1 балл
4)Сколько всего гибридизованных облаков образовалось?
а) 4 б) 2 с)3 2 балла
|
Критерий оценивания |
Дескриптор |
балл |
|
называют основные типы гибридизации и их основные характеристики
|
-правильно указывает тип гибридизации - называет молекулу вещества по рисунку -указывает число s –электронных облаков -указывает число гибридных облаков
|
2 1 1 2 |
Приложение 8 Чек – лист для оценки выступления в группе
|
Чек –лист |
Выставленный балл |
|
(оцените от 1 до 5) |
|
|
Материал на постере представлен ясно и доступно |
|
|
Презентация содержит схемы, чертежи |
|
|
Материал учениками излагается четко и ясно |
|
|
Даются ответы на вопросы других групп |
|
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.