
№______САБАҚТЫҢ ЖОСПАРЫ
ПЛАН ЗАНЯТИЯ №_______
Топ
Группа________________________________________
Күні
Дата____________________________________
Пәні
Дисциплина: Химия
Сабақтың тақырыбы:
Тема занятия: Алкены. Этилен, его получение.
Цель урока: дать уч-ся представление о непредельных углеводородах, о ненасыщенной (кратной) связи; о строении молекулы этилена – первого представителя ряда алкенов, о физических свойствах веществ этого ряда, их номенклатуре и изомерии.
Задачи урока:
1. дать уч-ся представление о гомологическом ряде алкенов.
2. дать представление о строении молекул алкенов на примере первого представителя этого ряда – этилене, о физических свойствах веществ ряда этилена.
3. дать уч-ся представление о видах изомерии, присущих для алкенов: структурной и пространственной.
4. научить уч-ся составлять формулы изомеров алкенов, используя знания о видах изомерии алкенов.
5. научить уч-ся составлять названия изомеров алкенов.
Оборудование: ball - rod models of alkene molecules, tab. "The structure of the ethylene molecule."
Ход урока: I. Анализ контрольной работы.
II. Новый материал.
1. Дать уч-ся понятие ненасыщенной связи, кратной связи. Дать понятие «непредельные углеводороды».
Использовать шаро – стержневые модели молекул этилена и пропилена, табл. № 2. Вспомнить с уч-ся уравнение реакции дегидрирования этана:
СН3 – СН3 à CH2 = CH2 + H2 |
Дать определение алкенов (стр. 33 учебника).
Alkenes, or olefins (from Latin olefiant - oil is an old name, but widely used in the chemical literature. Ethylene chloride, obtained in the 18th century, is a liquid oily substance.) Are aliphatic unsaturated hydrocarbons in whose molecules between carbon atoms have one double bond.
Alkenes contain in their molecule fewer hydrogen atoms than their corresponding alkanes (with the same number of carbon atoms), therefore such hydrocarbons are called unsaturated or unsaturated.
Ethylene. Ethene.
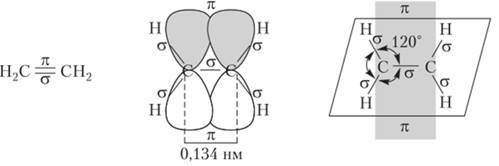
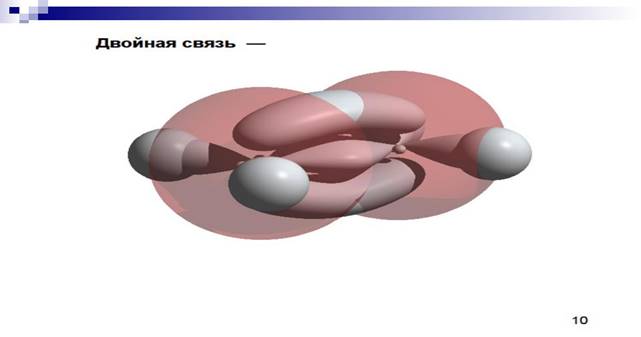
Н2С=СН2 молекула плоская , валентный угол 1200
II валентное состояние
1.SP2-
гибридизация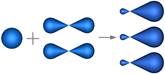
2. π , ϭ –связь3.валентный угол=1200
4.Есвязи (С=С)=620 кДж
Есвязи (С-С)=620-350=270 кДж
5.межъядерное расстояние 1,34 А0(или нм)
2. Строение молекул алкенов:
CnH2n – общая формула, где n больше или равно 2.
Задание классу: составить формулы алкенов, если n = 2,3,4,5,6
3. Гомологический ряд этилена и номанклатура алкено:
Принадлежность углеводорода к классу алкенов отражают родовым суффиксом - ен (или - илен) в его названии.
С2Н4 СН2=СН2 этен, этилен (-СН2=СН2 винил - радикал)
С3Н6 СН2=СН-СН3 пропен, пропилен
С4Н8 СН2=СН-СН2-СН3 бутен, бутилен
С5Н10 СН2=СН-СН2-СН2-СН 3 пентен, амилен
Features of the construction of the names of alkenes are that the main chain of carbon atoms must necessarily include a double bond C = C, and its numbering is carried out from the end of the main chain to which this bond is closer. In the name of the hydrocarbon ending in - en, the number indicates the number of the carbon atom from which the double carbon - carbon bond begins:
1 2 3 4 1 2 3 4
![]()
4. Изомерия алкенов.
Структурная изомерия
1.изомерия углеродного скелета
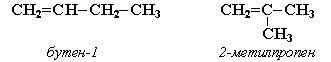
2.изомерия положения двойной связи
![]()
3.межклассовая изомерия с циклоалканами
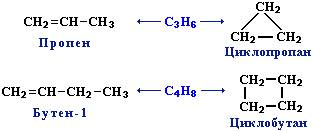
Пространственная изомерия алкенов
цис-транс-изомерия
Причина-неподвижность атома углерода при двойной связи
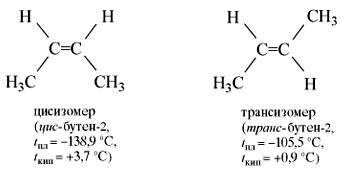
ВНИМАНИЕ! Цис-транс- изомерия не проявляется, если хотя бы один из атомов С при двойной связи имеет 2 одинаковых заместителя. Например,
бутен-1 СН2=СН–СН2–СН3 не имеет цис- и транс-изомеров, т.к. 1-й атом углерода связан с двумя одинаковыми атомами водорода.
Изомеры цис- и транс- отличаются не только физическими, но и химическими свойствами, т.к. сближение или удаление частей молекулы друг от друга в пространстве способствует или препятствует химическому взаимодействию. Иногда цис-транс-изомерию не совсем точно называют геометрической изомерией. Неточность состоит в том, что все пространственные изомеры различаются своей геометрией, а не только цис- и транс-изомеры.
4. Физические свойства алкенов
Первые три представителя гомологического ряда алкенов (этилен, пропилен и бутилен) — газы, начиная с C5H10 (амилен, или пентен-1) — жидкости, а с С18Н36 — твердые вещества. С увеличением молекулярной массы повышаются температуры плавления и кипения. Алкены нормального строения кипят при более высокой температуре, чем их изомеры, имеющие изостроение. Температуры кипения цис-изомеров выше, чем транс-изомеров, а температуры плавления — наоборот.
Алкены плохо растворимы в воде (однако лучше, чем соответствующие алканы), но хорошо — в органических растворителях. Этилен и пропилен горят коптящим пламенем.
5. Получение алкенов
1. Крекинг алканов: Основным промышленным источником получения первых четырех членов ряда алкенов (этилена, пропилена, бутиленов и пентиленов) являются газы крекинга и пиролиза нефтепродуктов, а также газы коксования угля (этилен, пропилен). Газы крекинга и пиролиза нефтепродуктов содержат от 15 до 30% олефинов. Так, крекинг бутана при 600°С приводит к смеси водорода, метана, этана и олефинов – этилена, пропилена, псевдобутилена (бутена-2) с соотношением олефинов ≈ 3,5 : 5 : 1,5 соответственно.
CnH2n+2 ---t, (400-700) → CnH2n+2 + CnH2n
алканалкен
2. Дегидрирование алканов:
CnH2n+2 --- t, kat-Ni или (Cr2O3)→ CnH2n +H2
3. Гидрирование алкинов:
CnH2n-2 + H2 --- t, kat-(Pt или Pd, Ni) → CnH2n
Получение в лаборатории
1. Дегидратация* спиртов:
R-CH2-CH2-OH ---t>140°C, H2SO4(конц.)→ R-CH=CH2 + H2O
*Правило А. М. Зайцева:
Отрыв атома водорода происходит от наименее гидрогенизированного атома углерода.
2. Дегидрогенирование* моногалогеналканов (по правилу Зайцева)
R-CH2-CH2-Г +NaOH ---спиртовой раствор, t→R-CH=CH2+NaГ+H2O
3. Дегалогенированиедигалогеналканов:
R-CH(Г)-CH2(Г) + Zn--- t, NaOH спирт.раствор → R-CH=CH2 + ZnГ2

Закрепление:
1. Фронтальный опрос:
1) Что такое алкены?
2) Какова общая формула алкенов, чему равна min n в этой формуле?
3) Дать сравнительную характеристику строения молекул алканов и алкенов.
4) Каковы физические свойства алкенов?
5) Какие виды изомерии характерны для алкенов?
6) Как получают этилен в промышленности?
2. Индивидуальные задания:
1) из списка веществ выбрать алкены: C2H2, C3H6, C2H4, C6H6, C8H16, C5H12, C4H8
2) составить молекулярные и свёрнутые структурные формулы гомологов этилена, если n= 3,4,5,6.
3) решить задачу: определить молекулярную и составить структурную формулы алкена, если известно, что массовая доля углерода в нём составляет 85,7%, относительная плотность вещества по водороду равна 21. (пропен)
4) составить и назвать все возможные изомеры для вещества состава С4Н8.
Самостоятельная работа по теме.
1 Вариант
1. Из предложенного ряда веществ выбрать алкены, назвать их:
C2H2 , C2H6 , C4H10, C6H6, C2H4, C6H12, C3H4, C4H8.
2. Что такое реакция:
1) гидратации;
2) галогенирования;
3) полимеризации?
2 Вариант
1. Составить и назвать алкены, если n = 3; 5; 6; 8; 2.
2. Что такое реакция:
1) гидрирования;
2) гидрогалогенирования;
3) окисления? Какие виды окисления органических веществ вы знаете?
Домашнее задание:
пар. 4 стр. 33 – 35, записи в тетради, стр. 41 вопр. 1,2,3, упр. 4; упражнение в тетради: составить и назвать все возможные изомеры для вещества состава С5Н10.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.