
Предмет: химия
|
Раздел долгосрочного планирования: |
Школа: КГУ «Опорная школа (ресурсный центр) на базе гимназии №9 п. Осакаровка» |
|||||
|
Дата:
|
ФИО учителя: Кондратова Тамара Сергеевна |
|||||
|
Класс: 9 |
Участвовали: |
Не участвовали: |
||||
|
Тема урока |
Аммиак. Лабораторный опыт «Модель молекулы аммиака» |
|||||
|
Цели обучения (ЦО) Цели обучения, достигаемые на этом уроке (Ссылка на учебный план) |
9.1.4.6.Объясняет молекулярную, электронную, структурную формулу аммиака. |
|||||
|
Цель урока |
Все ученики: Смогут объяснять молекулярную, электронную, структурную формулу аммиака. Большинство учеников: Умеют записывать электронную формулу аммиака, выявлять аналогию между молекулярной и структурной формулой. Некоторые ученики: Могут устанавливать причинно-следственные связи между строением молекулы аммиака и его свойствами, объяснить образование структурной и механизм образования электронной формул аммиака. |
|||||
|
Критерии оценивания
|
Обучающийся: 1.Может: записывать молекулярную формулу аммиака, объяснить образование структурной и электронной формул аммиака. 2.Находит сходство и отличие между молекулой азота и аммиака для объяснения активности молекулы последнего. 3. Устанавливает причинно – следственные связи между строением молекулы аммиака и его химической активностью и химическими свойствами. |
|||||
|
Языковые цели |
|
|||||
|
Воспитание ценностей |
Сотрудничество, взаимоуважение, умение работать в группе. |
|||||
|
Межпредметная связь |
Геометрия. Черчение. Строение пирамиды: основание, вершина. |
|||||
|
Предыдущие знания |
Азот. Лабораторный опыт «Строение молекулы азота». |
|||||
Сабақ барысы/ Ход урока
|
Время / этапы урока 3 мин |
Деятельность учителя
Учитель приветствует учащихся, и предлагает игру: все становятся в круг и передают из рук в руки чашу с водой.
Для реализации теперь уже целей урока учитель делит класс на три группы случайным образом по выбору картинок фасоли, гороха и бобов из «общей корзинки». Пока дети выбирают и делятся на три группы учитель может задать им вопрос: почему именно эти растения взяты для деления на группы и как они связаны с темой урока? |
Деятельность учащихся
Учащиеся осторожно, чтобы не пролить воду, передают чашу по кругу, не проливая ее. Чаша проходит круг. |
Оценивание
Учитель задает вопрос детям: Как вам удалось не пролить воду? Почему? Далее учитель желает ученикам также поддерживать и помогать друг другу, чтобы достичь общей цели. |
Способы дифференциации
Таким образом, в каждой группе будут находиться ученики с разными образовательными способностями. |
|
Начало урока 7 мин изучение + 6 мин презентация + 3 мин оценивание
|
Для изучения нового материала по теме урока учитель ставит проблемный вопрос: Молекула аммиака такая же инертная как и молекула азота? Исходя из чего мы можем высказать свое предположение?
Учитель показывает ОПЫТ «Дым без огня». (https://go.mail.ru/search_video?src=go&sbmt=1562685326455&fm=1&q=%D0%B2%D0%B8%D0%B4%D0%B5%D0%BE++%D0%BF%D0%BE+%D1%85%D0%B8%D0%BC%D0%B8%D0%B8++%D0%B4%D1%8B%D0%BC+%D0%B1%D0%B5%D0%B7+%D0%BE%D0%B3%D0%BD%D1%8F&d=3424758093&sig=66f295b2a2&s=Youtube)
Ученики предлагают сравнить строение молекул. После ответов на вопросы учитель помогает ученикам сформулировать тему урока и его цель, предлагает выработать соответствующие критерии успеха: К концу урока учащиеся смогут: 1.Может записывать молекулярную формулу аммиака, объяснить образование структурной и механизм образования электронной формул аммиака. 2.Находит сходство и отличие между молекулой азота и аммиака для объяснения активности молекулы последнего. 3. Устанавливает причинно – следственные связи между строением молекулы аммиака и его химической активностью, а поэтому может объяснить механизм образования электронной формулы аммиака. На этом этапе урока учитель использует подходы самообучения и взаимообучения, организуя индивидуальную и групповую самостоятельную работу Новый материал содержит текстовую информацию, рисунки, схемы.
. |
Ученики высказывают предположение, какая молекула активнее: азота или аммиака. Ответы могут быть разные.
Ученики видят, что аммиак – активное химическое вещество, и им предстоит это объяснить.
Каждая группа изучает материал учебника стр. 35-37, а также получает раздаточный материал с дополнительной информацией по теме урока (Приложение 1). Работа организуется по стратегии «Окно Джохари» (шаблон для работы групп подготовлен заранее на ватмане) - учащиеся сначала знакомятся с новым материалом индивидуально, затем обсуждают результаты своей работы в парах и в группе и заполняют таблицу. Важные окна – Белое пятно и Скрытая зона. Таблицы вывешиваются на доску, их представляет учащийся с каждой группы и проверяется совпадение квадратов в каждой группе. Таким образом, слепые пятна и скрытые зоны открываются в ходе поочередного общего представления своего выступления каждой группой. Неизвестное( черный ящик) - это и есть сумма этих квадратов.
SMS пишет каждый участник, крепит на общую доску, каждая группа подходит и выбирает SMS, которые, как он считает, адресованы именно их группе. Обсуждение проходить должно довольно быстро, лаконично. Почему каждый выбрал именно этот стикер? |
Формативное Оценивание выступления групп проводится методом SMS на стикере. |
|
|
|
|
|
|
|
|
|
. |
|
|
|
|
Основная часть 7 мин выполнение + 5 мин представление + 4 мин оценивание
|
Учитель помогает и поддерживает учеников, если последние затрудняются в формулировке выводов по теме, при необходимости он задает наводящие вопросы.
|
Для успешного усвоения нового материала урока ученики продолжают работать в группах, созданных в начале урока и получают задания. Задания составлены с учетом диффиренцированного подхода к обучению: от простого к сложному и, соответственно, подразумевают развитие мыслительных навыков высокого порядка: применение, синтез, оценивание. Каждая группа получает раздаточный материал с заданиями. Групповая работа «Делаем вместе» сначала индивидуально, затем в парах и в группе и заполняют приготовленную таблицу на ватмане, презентуют свою работу. Первой выступает группа, которая справилась с заданием быстрее остальных, другие группы дополняют, дают более полные и развернутые ответы. Другие группы оценивают выступление по критериям, приведенным в начале урока. В ходе активной работы учащиеся объясняют молекулярную, электронную и структурную формулу аммиака, показывают собранные молекулы аммиака. При выполнении данного вида деятельности у учеников формируются навыки обработки и анализа информации о механизме образования электронной формулы аммиака, оценки активности молекулы аммиака по сравнению с молекулой азота.
В заключение данного этапа урока ученики делают вывод о том, достигнута ли цель урока в соответствии с критериями успеха.
Задание –Приложение 2 |
Формативное оценивание учащихся проводится по методу «Горячий микрофон», где ребята высказывают свое мнение о выступлении первой группы и о том, что у них получилось в работе или нет, где были затруднения и что нужно сделать для того, чтобы их преодолеть. |
|
|
Конец урока 5 мин
|
Учитель обобщает урок закрытыми вопросами применяя прием Тrue/ False 1.Аммик – активное химическое вещество. 2.Молекула аммиака имеет форму пирамиды. 3. В вершине пирамиды находится свободная электронная пара. 4.Причина активности молекулы кроется в наличии свободной электронной пары атома азота. 5.Количество общих электронных пар между азотом и водородом равно двум. 6.Электронная плотность в молекуле сдвинута в сторону азота. Обобщив урок, учитель нацеливает учеников на самостоятельное углубленное изучение уже полученных знаний. Домашнее задание учитель задает по учебнику – упр. 8-10 стр. 34
|
Ученики показывают ответы большим пальцем руки |
По ответам учеников учитель делает вывод о том, что учащиеся усвоили материал урока и цели урока достигнуты. |
Рефлексия урока проводится по методу критического мышления «3+3+1» (в соответствии с темой урока): •1.написать 3 предложения по теме урока •2.сократить до 3 слов • 3.сократить до 1 слова Ученики после рефлексии зачитывают свои варианты рефлексии. Учитель благодарит учеников за работу. |
Приложение 1 АММИАК
Название соединения "аммиак" предположительно произошло от нескольких источников. Предположительно, свое название аммиак получил в честь бога Аммона, культ которого был распространен в Северной Африке. Аммиак может образовываться в результате быстрого разложения мочевины в очень жарком климате, что и связало запах соединения с культом божества.
По некоторым другим сведениям, аммиак мог получить свое современное название от древнеегипетского слова "амониан", как называли последователей египетского бога Амона. В качестве атрибута в некоторых элементах ритуальных обрядов использовался хлорид аммония, который при нагревании разлагается с образованием аммиака.
В 1801 году русский ученый-химик, академик Яков Дмитриевич Захаров ввел сокращенное название "аммиак", которое используется в настоящее время.
В чистом виде аммиак был получен в 1774 г. английским химиком Джозефом Луи Пристли. Он нагревал "аммониак" (хлорид аммония) с гашеной известью (гидроксидом кальция). Эту реакцию до сих пор используют в лабораториях, если требуется получить небольшие количества этого газа. Выделявшийся аммиак Пристли собирал над ртутью. Он назвал его «щелочным воздухом», так как водный раствор аммиака имел все признаки щелочи.
https://foxford.ru/wiki/himiya/ammiak
Молекула NH3 имеет форму трехгранной пирамиды с атомом азота в вершине.
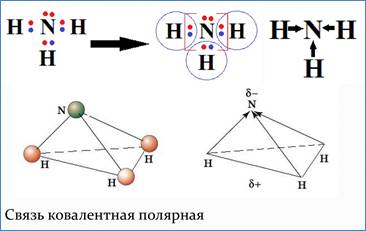
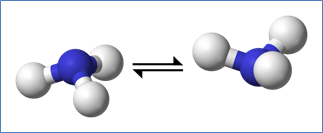
Однако, в отличие от пирамиды, склеенной, к примеру, из бумаги, молекула NH3 с легкостью «вывертывается наизнанку», наподобие зонтика, и при комнатной температуре она проделывает такое превращение с огромной частотой – почти 24 млрд. раз в секунду! Такой процесс называется инверсией; Если бы не было инверсии, существовали бы два пространственных изомера этого вещества, которые отличались бы друг от друга как предмет и его зеркальное изображение; роль четвертого заместителя играет неподеленная пара электронов у атома азота.

Между молекулами аммиака существуют водородные связи. Хотя они и не такие прочные, как между молекулами воды, эти связи способствуют сильному притяжению между молекулами. Поэтому физические свойства аммиака во многом аномальны по сравнению со свойствами других гидридов элементов той же подгруппы (PH3, SbH3, AsH3).

В твердом аммиаке каждый атом азота связан с шестью атомами водорода тремя ковалентными и тремя водородными связями. При плавлении аммиака рвутся только 26% всех водородных связей, еще 7% разрываются при нагреве жидкости до температуры кипения. И лишь выше этой температуры исчезают почти все оставшиеся между молекулами связи.
Среди прочих газов аммиак выделяется своей огромной растворимостью в воде: при нормальных условиях 1 мл воды способен поглотить больше литра газообразного аммиака (точнее, 1170 мл) с образованием 42,8%-ного раствора. Если рассчитать соотношение NH3 и H2O в насыщенном при нормальных условиях растворе, то получится, что одна молекула аммиака приходится на одну молекулу воды. При сильном охлаждении такого раствора (примерно до –80° C) образуются кристаллы гидрата аммиака NH3·H2O Известен также гидрат состава 2NH3·H2O.
Аммиак благодаря неподеленной паре электронов образует огромное количество комплексных соединений с ионами металлов – так называемых амминокомплексов или аммиакатов. В отличие от органических аминов, в этих комплексах с атомом азота всегда связаны три атома водорода.
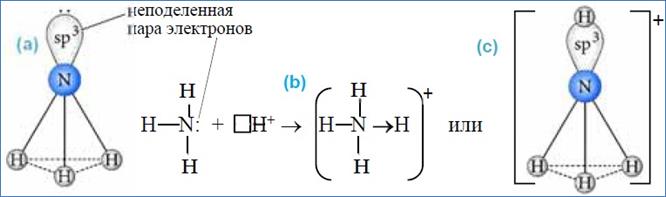
Как и в случае воды, комплексообразование с аммиаком часто сопровождается изменением окраски вещества.
Сильные водородные связи приводят к сравнительно высокой (по сравнению с другими газами) теплоте испарения аммиака – 23,3 кДж/моль. Это в 4 раза больше теплоты испарения жидкого азота и в 280 раз больше, чем у жидкого гелия. Поэтому жидкий гелий вообще невозможно налить в обычный стакан – он немедленно испарится. С жидким азотом такой опыт провести можно, но значительная его
http://znakka4estva.ru/dokumenty/himiya/ammiak/#vtab1
Приложение 2
Раздел 9.1.4.
Тема Аммиак. Лабораторный опыт «Модель молекулы аммиака»
Учебная цель 9.1.4.6. Объясняет молекулярную, электронную, структурную формулу аммиака.
Уровень навыков мышления Применение, синтез, оценивание
Критерии оценивания
1.Может: записывать молекулярную формулу аммиака, объяснить образование структурной и механизм образования электронной формул аммиака.
2.Находит сходство и отличие между молекулой азота и аммиака для объяснения активности молекулы последнего.
3. Устанавливает причинно – следственные связи между строением молекулы аммиака и его химической активностью, а поэтому может объяснить механизм образования электронной формулы аммиака.
Заполните таблицу:
|
Химическая формула аммиака |
Структурная формула аммиака |
Тип химической связи |
Молекулярная модель (рисунок) |
Схема образования электронной формулы аммиака |
Количество общих электронных пар |
Количество свободных электронных пар |
|
|
|
|
|
|
|
|
Лабораторный опыт №1 « Моделирование молекулы аммиака»
1. Соберите шаростержневую модель молекулы аммиака, используя химический конструктор.
2. Ответьте на вопросы: Почему молекула аммиака имеет форму пирамиды?
3. Как свободная электронная пара атома азота влияет на активность молекулы?
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.