
Публикация является частью публикации:


1. Дайте характеристику химическому элементу водороду с точки зрения строения атома и положения в периодической системе(состав, строение, степень окисления-свойства). Для характеристики распространения этого элемента в природе выберите необходимую информацию из приложения.
Рассчитайте, сколько водорода по массе содержит ваш организм. Какой объем газообразного водорода может составить эта масса.
2.
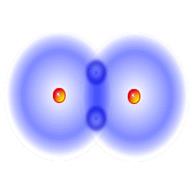 Дайте
характеристику химическому соединению (простому веществу) водороду:
Дайте
характеристику химическому соединению (простому веществу) водороду:
· Состав: множество………………………….молекул. Атомы в молекуле связаны ……….. …….. связью. Следовательно, молекулы - ……..
· Строение: Упаковка(взаимодействие) …….. молекул неплотная. Структура рыхлая - ………………… кристаллическая решетка. Следовательно,
· Физические свойства:…………., …….цвета, ………запаха, ……растворим в воде, имеет ………… температуру кипения и плавления. Мr(Н2) =…….., а Мr(воздуха) = 29, т.е. относительная плотность водорода по воздуху равна: dвозд= Мr(Н2)/ Мr(возд)=…… , а воздуха по водороду соответственно………… . Что означает – водород в ……… раз легче воздуха. Как используется это свойство? Какими специфическими свойствами обладает газообразный водород? (См. Приложение 1-3, 10-12)
· Получение водорода в лаборатории. Составьте уравнения реакций описанных в пунктах 5-6. Рассчитайте, какой объём водорода(н.у.) максимально можно получить используя одинаковую массу металла. Какие существуют способы собирания водорода(учебник стр.99).
· Получение в промышленности. В соответствии с пунктом 7-8 рассчитайте, какой объём водорода можно получить из 400 м3 природного газа, объёмная доля метана в котором составляет 96%. Составьте уравнение реакции электролиза воды.
· Химические свойства и применение. В соответствии с пунктами 13-17, 18-22 охарактеризуйте свойства и применение водорода. Представьте это в виде таблицы.
|
№ |
Уравнение реакции |
Применение |
|
|
|
|
Знаете ли вы, что:
1. ...водород во Вселенной является самым распространенным элементом; в межзвездном пространстве атомы водорода встречаются примерно в сто раз чаще, чем атомы всех остальных элементов, вместе взятых; на отдельных планетах водород может существовать в твердом состоянии
2. ...жидкий водород почти на порядок легче воды и это самая легкая жидкость;
3. ...на высоте 50 км от земли водорода содержится 3%, а на высоте 100 км его содержится 95%; на земле в среднем около 1% по массе;
4.
 ...в человеческом организме водорода содержится 10%, или около
……кг;
...в человеческом организме водорода содержится 10%, или около
……кг;
5. ...водород заметил Т.Парацельс в XVI в., когда погружал железо в серную кислоту; водород изучен Г.Кавендишем в 1766 г. и получен в чистом виде из воды А.Лавуазье в 1783 г.;
6. Щелочные металлы, чьи оксиды и гидроксиды проявляют амфотерные свойства взаимодействуют с растворами щелочей с образованием водорода.
7.
 …технический
водород получают взаимодействием природного метана с кислородом воздуха и
водяным паром по уравнению:
…технический
водород получают взаимодействием природного метана с кислородом воздуха и
водяным паром по уравнению:
2СН4 + О2 + 2Н2О = 2СО2 + 6Н2;
8. … при пропускании электрического тока через водные растворы солей, щелочей кислот протекает процесс электролиза воды;
9. …палладий – очень прочный металл из семейства платины. Но удержать водород в сосуде из палладия не удастся: он будет растворяться в металлическом палладии. При комнатной температуре 1 см3 Pd поглощает около 800 см3 водорода. Сосуд при этом разбухает и дает трещины;
10. ...при помощи стратостата, наполненного 25 000 м3 водорода, советские навигаторы Прокофьев, Бирибаум и Голдунов в 1933 г. поднимались на высоту 19 км;
11. … В июне 1794 г. для наблюдения за передвижением армии интервентов во время боя при Флёрюсе (Франция) был использован привязной воздушный шар, заполненный водородом. Для заполнения водородом воздушного шара Жан Кутель —французский инженер —и Николя Конте— французский химик—создали крупную установку, состоящую из семи чугунных труб, вмазанных в печь и заполненных железными опилками. При прохождении водяного пара через раскаленные докрасна железные опилки образовывался водород, который очищался пропусканием через воду и водную суспензию гидроксида кальция. В России в 1803 г. Химик Яков Дмитриевич Захаров создал подобную установку для производства водорода. Она вмещала 819 кг железных стружек и производства 91 м3 водорода в час.
12. ….первый большой воздушный шар, наполненный водородом, был построен в 1783 г. французским физиком Ж.Шарлем;
13. ...в 1937 г. дирижабль «Гинденбург», наполненный водородом, взорвался, и из 99 пассажиров, находившихся на нем, 48 погибли;
14. …в обычных условиях не происходит взаимодействия углерода и водорода. Но при нагревании в присутствии мелкораздробленного никеля образуется метан. Практически все реакции водорода с неметаллами(хлором, азотом, серой) протекают при нагревании и процесс этот обратим;
15. …для получения маргарина используют растительные масла, которые превращаются в твердые жиры при реакции гидрирования: С57Н98О6 + 3Н2 = С57Н104О6;
16. …оказывается, железо может болеть «водородной чумой». Дело в том, что атомарный водород активно реагирует с карбидами железа, в частности с цементитом, упрочняющим стальные изделия: Fe3C + 4H0 = 3Fe + CH4. Структура металла изменяется, а его прочность резко падает.
17. …хорошо реагирует активными металлами с образованием гидридов, солеподобных веществ, которые легко подвергаются гидролизу.
18. …в 1959 г. английский инженер Ф. Бекон сконструировал промышленный образец с мощностью 6 кВт. Начиная с 1960-х гг. бортовые системы американских кораблей «Джемини», «Аполлон», «Спейс-Шатл» получали питание от топливных элементов;
19. …в нашей стране первая энергоустановка на топливных элементах была разработана в 1970 г. и предназначалась для полета космонавтов на Луну;
20.
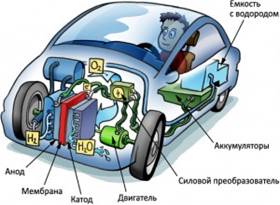 …с 1983 г. в США и Японии проходят испытание 46 электростанций на
топливных элементах. За год они вырабатывают 4 млн кВт • ч электроэнергии;
…с 1983 г. в США и Японии проходят испытание 46 электростанций на
топливных элементах. За год они вырабатывают 4 млн кВт • ч электроэнергии;
21. …способность водорода как восстановителя применяется в пирометаллургии для получения редких металлов, таких как вольфрам, ниобий из их оксидов;
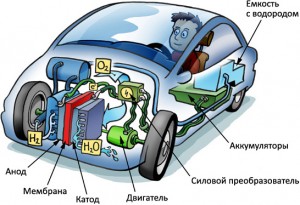
22. Водород – перспективное экологически чистое топливо.
23.
 Заслуживает внимание соединение - Перокси́д водоро́да
(перекись водорода), H2O2— простейший представитель пероксидов. Бесцветная жидкость с«металлическим»
вкусом, неограниченно растворимая в воде, спирте и эфире. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2•2H2O. В промышленных
масштабах пероксид водорода получают электролизом серной
кислоты, в ходе которого образуется надсерная
кислота, и последующим разложением последней до пероксида и серной кислоты.
Заслуживает внимание соединение - Перокси́д водоро́да
(перекись водорода), H2O2— простейший представитель пероксидов. Бесцветная жидкость с«металлическим»
вкусом, неограниченно растворимая в воде, спирте и эфире. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2•2H2O. В промышленных
масштабах пероксид водорода получают электролизом серной
кислоты, в ходе которого образуется надсерная
кислота, и последующим разложением последней до пероксида и серной кислоты.
В лабораторных условиях для получения пероксида водорода используют реакцию:
![]()
Выпускается в виде водных растворов, стандартная концентрация 1-6 %, 30, 38, 50, 60, 85, 90 и 98 %. 30 % водный раствор пероксида водорода, стабилизированный добавлением фосфатов натрия, называется пергидролем. Выпускаемый в виде таблеток твёрдого клатрата с мочевиной пероксид водорода называется гидроперитом.
Благодаря своим сильным окислительным свойствам пероксид водорода нашёл широкое применение в быту и в промышленности, где используется, например, как отбеливатель на текстильном производстве и при изготовлении бумаги. Применяется как ракетное топливо, в качестве окислителя или как однокомпонентное (с разложением на катализаторе), в том числе для привода турбонасосных агрегатов. Используется в аналитической химии, в качестве пенообразователя при производстве пористых материалов, в производстве дезинфицирующих и отбеливающих средств. В промышленности пероксид водорода также находит свое применение в качестве катализатора.
Хотя разбавленные растворы перекиси водорода применяются для небольших поверхностных ран, исследования показали, что этот метод, обеспечивая антисептический эффект и очищение, также продлевает время заживления. Обладая хорошими очищающими свойствами, пероксид водорода на самом деле не ускоряет заживление ран. Достаточно высокие концентрации, обеспечивающие антисептический эффект, могут также продлевать время заживления из-за повреждения прилегающих к ране клеток. Более того, пероксид водорода может мешать заживлению и способствовать образованию рубцов из-за разрушения новообразующихся клеток кожи. Однако в качестве средства для очистки глубоких ран сложного профиля, гнойных затеков, флегмон и других гнойных ран, санация которых затруднена, пероксид водорода остается предпочтительным препаратом. Он обладает не только антисептическим эффектом, но и создаёт большое количество пены при взаимодействии с ферментом пероксидазой. Это в свою очередь позволяет размягчить и отделить от тканей некротизированные участки, сгустки крови, гноя, которые будут легко смыты последующим введением в полость раны антисептического раствора. Без предварительной обработки пероксидом водорода антисептический раствор не сможет удалить эти патологические образования, что приведет к значительному увеличению времени заживления раны и ухудшит состояние больного.
Пероксид водорода применяется также для обесцвечивания волос и отбеливания зубов, однако эффект в обоих случаях основан на окислении, а следовательно — разрушении тканей, и потому такое применение (особенно в отношении зубов) не рекомендуется специалистами.
В пищевой промышленности растворы пероксида водорода применяются для дезинфекции технологических поверхностей оборудования, непосредственно соприкасающихся с продукцией. Кроме того, на предприятиях по производству молочной продукции и соков, растворы перекиси водорода используются для дезинфекции упаковки (технология «Тетра Пак»). Для технических целей пероксид водорода применяют в производстве электронной техники.
В быту применяется также для выведения пятен MnO2, образовавшихся при взаимодействии перманганата калия («марганцовки») с предметами (ввиду его восстановительных свойств).
3%-ный раствор пероксида водорода используется в аквариумистике для оживления задохнувшейся рыбы, а также для очистки аквариумов и борьбы с нежелательной флорой и фауной в аквариум
24.  На долю атомов элемента
Х приходится около 92 % всех атомов Вселенной. На Земле этот показатель
заметно меньше, а его массовая доля составляет всего 1 % (9 место среди
элементов). Однако его роль на нашей планете определяется вовсе не массой, а
числом атомов, доля которых среди остальных элементов составляет 17 %.
На долю атомов элемента
Х приходится около 92 % всех атомов Вселенной. На Земле этот показатель
заметно меньше, а его массовая доля составляет всего 1 % (9 место среди
элементов). Однако его роль на нашей планете определяется вовсе не массой, а
числом атомов, доля которых среди остальных элементов составляет 17 %.
· Элемент Х входит в состав практически всех органических веществ и присутствует во всех живых клетках, в которых на него приходится почти половина всех атомов.
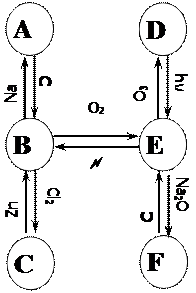
· На приведенной схеме буквами A – F зашифрованы вещества, содержащие элемент Х, и показаны некоторые пути их взаимных превращений. Обозначения над стрелками показывают, с чем реагируют вещества, либо условия проведения реакции: С – это соединение С (не углерод!), «hν» – облучение ультрафиолетом, «~» – электрический ток.
· Дополнительно известно, что вещество B – простое, а соединение D содержит 5,88 % элемента Х. Назовите элемент Х.
· Составьте уравнения реакций. Если у Вас еще нет ответа на этот вопрос, отодвиньте листик с заданием подальше от себя, подумайте хорошенько и внимательно посмотрите на схему издалека.

http://www.svarkomplekt.ru/cgi-bin/catalog/viewgroup.cgi?biggroup=1

http://www.fxyz.ru/%D1%84%D0%BE%D1%80%D0%BC%D1%83%D0%BB%D1%8B_%D0%BF%D0%BE_%D1%85%D0%B8%D0%BC%D0%B8%D0%B8/%D0%BF%D0%B5%D1%80%D0%B8%D0%BE%D0%B4%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D0%B0_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D0%BE%D0%B2_%D1%82%D0%B0%D0%B1%D0%BB%D0%B8%D1%86%D0%B0_%D0%BC%D0%B5%D0%BD%D0%B4%D0%B5%D0%BB%D0%B5%D0%B5%D0%B2%D0%B0/%D0%B2%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4/

http://www.wikiznanie.ru/ru-wz/index.php/%D0%92%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B
http://www.chemport.ru/datenews.php?news=102
http://dom.a42.ru/archives/11420
http://zaryad.com/2011/09/12/vodorod-bezopasnaya-alternativa-benzinu/
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.