
Дмитриченко Л.В.
МБОУ «Новоазовская школа №2»
администрации Новоазовского района
учитель химии
Тема урока: Скорость химической реакции.
Цели:
Образовательные: сформировать у учащихся знания о скорости химической реакции, о факторах, влияющих на скорость химической реакции; подвести учащихся к пониманию закономерностей, с помощью которых можно управлять химическими реакциями; углубить знания о катализаторах. Показать значение скорости в природе и деятельности человека.
Воспитательные: продолжить формирование мировоззренческих понятий: причинно-следственные связи и познаваемость мира; воспитывать у учащихся интерес к учению.
Развивающие: в процессе выполнения лабораторных опытов продолжить развитие мыслительных умений: анализировать, сравнивать и делать выводы.
Ход урока
1. Организационный этап
2. Актуализация знаний
Фронтальный опрос:
- Что такое химическая реакция?
- Что происходит с молекулами при протекании химических реакций?
3. Изучение темы урока
Понятие скорость химической реакции.
Учитель:
Понятие скорость изучает не только наука физика, но и химия.
Вопрос:
Как вы думаете, зачем химикам скорость? Скорость чего можно измерять в химии?
(Предполагаемый ответ: Скорость химической реакции)
Информация учителя:
Взаимодействия химических веществ могут осуществляться с различной скоростью.
Золотые украшения сохраняют свой блеск и красоту веками.
Столетиями стареют и разрушаются лаки и краски на полотнах старых мастеров.
С довольно низкой скоростью протекает процесс разрушения металла – коррозия.
Также медленно разрушаются под действием кислотных дождей мраморные сооружения, здания из камня.
Очень медленно протекают реакции выветривания горных пород.
А скорость нарастания сталактитов в каменных пещерах (т.е. образования карбоната кальция) составляет всего 0,13 мм в год.
Примером химических реакций, скорость которых довольно высока, могут послужить реакции нейтрализации, протекающие в водных растворах. Реакция выделения углекислого газа при взаимодействии соды с уксусной кислотой.
Как пример можно назвать реакцию взаимодействия раствора сульфата меди со щёлочью, в результате которой практически мгновенно выпадает осадок синего цвета – гидроксид меди. CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Долгие годы сохраняет оболочка бомбы страшное эхо войны и достаточно лишь нескольких секунд, чтобы разбудить его.
Взрыв – это мгновенное вовлечение в реакцию всей массы вещества, самый быстрый из химических процессов.
Данные примеры показывают, что реакции протекают с различными скоростями, одним нужны считанные секунды, другим миллионы лет, а многие протекают с умеренной скоростью.
Учитель: запишите тему: «Скорость химической реакции»
Создание проблемной ситуации.
Вопросы для обсуждения:
1. Как вы думаете, человек может изменить скорость химической реакции?
2. Что нужно знать, для того, чтобы управлять скоростью хим. реакции?
(учащиеся высказывают идеи)
Предлагаю вашему вниманию Видеосюжет: разрушение памятника гражданину Кузьме Минину и князю Дмитрию Пожарскому в Москве.
(Монумент состоит из бронзовой скульптурной группы и гранитного пьедестала с бронзовыми барельефами. Бро́нза — сплав меди, обычно с оловом в качестве основного компонента, добавки – цинка.)
Вопросы:
1. Что мы узнали из сюжета, что происходит с памятником?
(памятник разрушается, происходит реакция окисления)
2. Что повлияло на разрушение памятника?
(Учащиеся высказывают идеи, рассуждают:
Агрессивная окружающая среда, т.е. разрушение в результате атмосферной и других видов коррозии основных и вспомогательных материалов памятника.
Разрушения от действия воды – осадки (атмосферной и конденсационной влаги), связанные с недостатками конструкции и отсутствием стоков.
Износ поверхности (трещины) в результате применения неатмосферостойких механически непрочных защитно-декоративных покрытий, нуждающихся в периодической замене.
Механические повреждения, поломки, утраты, сколы, сбои в результате механических воздействий.)
Вопрос:Какое предположение мы можем сделать? Что оказывает влияние на протекание реакции?
(Предполагаемый ответ: На протекание хим. реакции оказывают влияние внешние факторы.)
Учитель:
Итак, наше теоретическое предположением мы должны проверить на практике. (Гипотезу нужно подтвердить экспериментально.)
Гипотеза исследования: на скорость химических реакций влияют внешние факторы.
Вопрос: Какова цель нашего исследования? (Высказывания учащихся)
Цель исследования: выяснить от каких факторов зависит скорость химических реакций.
Для решения проблемы, учащиеся выполняют практические исследования, работая в группах.
Задание: Вам необходимо точно по инструкции провести эксперимент и ответить на предложенные вопросы.
Для работы учащиеся получают инструктивную карту и памятку с правилами техники безопасности при выполнении хим. эксперимента.
Не забывайте соблюдать правила техники безопасности!
(Учащиеся работают в группах согласно инструктивным картам)
Каждая группа исследует влияние определённого фактора на скорость химической реакции.
1. Зависимость скорости химической реакции от природы реагирующих веществ.
2. Зависимость скорости реакции от концентрации реагирующих веществ (для веществ в растворённом состоянии и газов).
3. Зависимость скорости реакции от поверхности реагирующих веществ (для веществ в твёрдом состоянии).
4. Зависимость скорости реакции от температуры.
5. Зависимость скорости реакции от присутствия катализатора
После практических исследований – отчёт групп.
Вывод формулы скорости хим. реакции
Учитель: Давайте ещё раз обратимся к формуле равномерного движения. И попробуем провести аналогию с понятием скорости химической реакции.
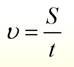
Скорость – это отношение перемещения тела в пространстве к промежутку времени, в которое произошло это перемещение.
Вопросы для обсуждения:
- Какую величину мы можем оставить из данной формулы?
( предполагаемый ответ: Время)
- А расстояние, записанное в числителе, мы можем оставить?
( предполагаемый ответ: нет)
Тогда в числителе у нас будет другой показатель.
Учитель:
Условная реакция
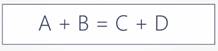
Вопрос:
Что происходит в процессе химической реакции с веществами?
(Количество исходных веществ А и В с течением времени уменьшаются, а количество продуктов реакции С и D наоборот увеличиваются. При протекании химической реакции изменяется концентрация.)
Чем быстрее происходит процесс изменения концентраций веществ, тем больше скорость химической реакции.
Вопрос:
Исходя их всего выше сказанного, какая величина изменяется в ходе химической реакции? (Ответ:Концентрация)
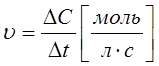
С1-С2 ; т2-т1
Вопрос:
Как можно определить скорость хим. реакции?
Скорость химической реакции определяется изменением концентрации
одного из реагирующих веществ в единицу времени.
Определим единицы измерения скорости хим. реакции.
Концентрация: моль/л
Время: сек
Скорость: моль/ л *с
Практическое применение знаний о скорости хим. реакций
Вопрос для обсуждения:Зачем нужны знания о скорости химической реакции?
(Предполагаемый ответ: для управления реакцией.)
Учитель: В жизни часто приходится управлять химической реакцией:
замедлять или ускорять процессы, сопровождающие нас в повседневной жизни и на производстве.
Вопрос: А зачем?
(Предполагаемые ответы:
Некоторые реакции нежелательны, они наносят вред и могут представлять опасность для жизни и здоровья человека.
Скорость таких реакций необходимо замедлить или остановить.
Примерами таких реакций является:
Порча пищевых продуктов, при употреблении которых возникают опасные пищевые отравления.
Реакция горения, которая приобретает большие масштабы и носит название - Пожар.
Процесс разрушения металлов под воздействием внешней среды - коррозия металлов.
Возможны также взрывы на сахарных и мукомольных заводах, а также взрывы угольной пыли в шахтах.
Конечно, большинство реакций являются необходимыми и полезными для человека.
Понятие «скорость химической реакции» это одно из важных параметров при получении многих химических веществ (волокон, красителей, полимерных материалов, лекарственных веществ, аммиака, серной кислоты и других).
Нужно ускорить и процесс выплавки металлов на металлургических заводах.
Для повышения производительности химических производств необходимо создать условия, способствующие ускорению химических процессов.
Чем выше скорость реакции, тем больше в единицу времени образуется требуемого продукта. Таким образом, увеличивается производительность производства и экономический эффект.
Например, нефтеперерабатывающая промышленность в буквальном смысле бьётся за каждые дополнительные полпроцента продукта в единицу времени. Ведь учитывая огромное количество перерабатываемой нефти, даже полпроцента вытекает в крупную финансовую годовую прибыль.)
4. Закрепление знаний по теме
Учитель: В быту и на производстве человек использует различные предметы и встречается с различными явлениями.
Вопросы для обсуждения:
Назовите, какие факторы, влияющие на скорость хим. реакций лежат в их основе.
1. На каком принципе основано использование в медицине кислородных подушек?
2. Почему продукты питания хранят в холодильнике?
3.
25 февраля 2017 г. ночью в одном из цехов Скидельского сахарного комбината в Белоруссии прогремел взрыв пылевоздушной смеси. Вспышка произошла в цеху упаковки и фасовки сахара. В результате чего пострадали пять работниц, которые были госпитализированы с ожогами различной степени тяжести.
Вопрос: Почему на сахарном заводе возможен взрыв?
4. В каком случае можно перевозить соляную кислоту в стальных цистернах?
5. Почему костёр разжигают с помощью бумаги и небольших щепочек?
6. Как правило, смесители и краны в ванной и на кухне изготовлены из нержавеющей стали, покрыты хромом или благородными металлами или сплавами: бронзой, латунью, никелем. Блестящая поверхность со временем покрывается известью и пятнами. Рано или поздно с этими проблемами сталкиваются владельцы даже самых дорогих и качественных моделей. Чистящие вещества, содержащие кислоты, позволяют быстро растворить известковый налёт, но они так же отрицательно влияют на покрытие смесителей.
Вопрос: Какой компонент должен быть в составе чистящего средства?
7. Объясните, почему сахарный песок растворяется в стакане чая быстрее, чем кусочек сахара той же массы.
8. Сухой хлор хранят в железных баллонах. Влажный хлор разрушает железо. Какую роль играет вода в этом процессе?
10. Почему стирку порошком с ферментами нельзя проводить при температуре больше 50оС?
Учитель: Давайте вернёмся к началу урока.
Вашему вниманию был представлен Скульптурный монумент, посвящённый предводителям Второго народного ополчения 1612 года, а также окончанию Смутного времени и изгнанию польских интервентов из России.
Проблема разрушения памятников и зданий архитектуры, это конечно проблема не только России. Они разрушаются с течением времени.
Вопросы для обсуждения:
- А зачем сохранять памятники?
(предполагаемый ответ: Это память народа, это наша история, уважение к истории своей страны. Важно сохранение памятников прошлого такими, какими оставили нам в наследие предшественники, любившие своё Отечество.
Проблема сохранения культурного наследия.
Памятники своим величием дают эмоциональный заряд, внушают уважение к истории своей страны, помогают сохранять значимое прошлое.
Они призваны воспитывать в гражданах чувство гордости за предков.)
- На основании того, что вы узнали, как уменьшить скорость данной реакции?
Ваши идеи, что можно сделать?
(Учащиеся высказывают мнения, идеи, приходят к решению проблемы.)
5. Рефлексия.
Продолжите фразу:
Было трудно…
Я понял, что…
Я научился
6. Подведение итогов урока.
Итак, мы познакомились с понятием «скорость химической реакции» и рассмотрели от каких факторов она зависит.
- Что изменяется в ходе химической реакции?
- Какие факторы влияют на скорость химической реакции?
- Что такое катализаторы и ингибиторы?
Домашнее задание: Выучить § 3, выполнить упр. № 2,3 стр. 15
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.