
 НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ -
АЛКАДИЕНЫ
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ -
АЛКАДИЕНЫ
Алкадиены - непредельные (ненасыщенные) углеводороды, имеющие в молекуле две двойных связи С=С. Каждая такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкадиены также называют диеновыми углеводородами. Первый член гомологического ряда - пропадиен - CH2=C=CH2. Общая формула их гомологического ряда - CnH2n-2.
НОМЕНКЛАТУРА И ИЗОМЕРИЯ АЛКАДИЕНОВ
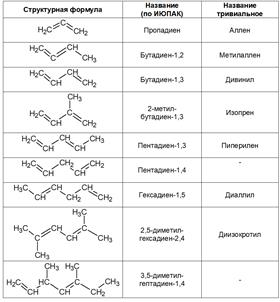
Названия алкадиенов формируются путем добавления суффикса «диен» к названию алкана с соответствующим числом: пропадиен, бутадиен, пентадиен и т.д.
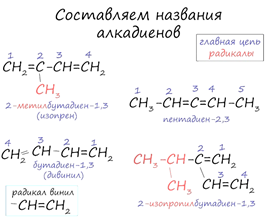 При составлении
названия алкадиена важно учесть, что главная цепь атомов углерода должна
обязательно содержать двойные связи.
При составлении
названия алкадиена важно учесть, что главная цепь атомов углерода должна
обязательно содержать двойные связи.
Нумерация атомов углерода в ней начинается с того края, к которому ближе двойная связь.
В конце названия указывают атомы углерода, у которых начинается двойная связь.
Для алкадиенов характерна:
- структурная изомерия (изомерия углеродного скелета, положения двойных связей, межклассовая изомерия с алкинами);
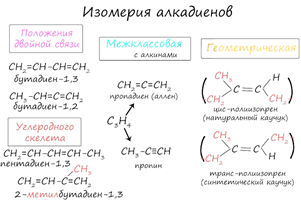 - пространственная
геометрическая изомерия (существование цис- и транс-изомеров).
- пространственная
геометрическая изомерия (существование цис- и транс-изомеров).
В зависимости от того, как чередуются двойные связи в молекуле алкадиена, они подразделяются на следующие типы:
I. Кумулированные двойные связи в случае, если две двойные связи прилежат к одному и тому же атому углерода). Пример - пропадиен-1,2 (аллен) - CH2=C=CH2
II. Сопряженные двойные связи (в случае, если две двойные связи разделены одной одинарной связью). Пример - бутадиен-1,3 - CH2=CH-CH=CH2
III. Изолированные двойные связи (в случае, если две двойные связи разделены двумя и более одинарными связями). Пример - пентадиен-1,4 - CH2=CH-CH2-CH=CH2
ПОЛУЧЕНИЕ АЛКАДИЕНОВ
Алкадиены получают несколькими способами:
1. Дегидрогалогенирование дигалогеналканов
В результате реакции молекулы алкана, содержащей два атома галогена, со спиртовым (!) раствором щелочи получается алкадиен. В зависимости от положения галогенов возможны разные варианты.
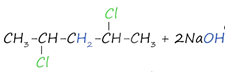 Отщепление
идет по правилу Зайцева: атом водорода отщепляется от соседнего, наименее
гидрированного атома углерода.
Отщепление
идет по правилу Зайцева: атом водорода отщепляется от соседнего, наименее
гидрированного атома углерода.
![]()
![]()
2. Синтез С.В. Лебедева
Сергей Васильевич Лебедев в 1927 году разработал первый промышленный способ получения синтетического каучука из этилового спирта.
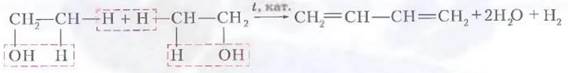
450 °C, кат. ZnO
![]() 2CH3-CH2-OH
CH2=CH-CH=CH2 + 2H2O
+ H2
2CH3-CH2-OH
CH2=CH-CH=CH2 + 2H2O
+ H2
Для придания каучуку необходимых физико-механических свойств: прочности, эластичности, стойкости к действию растворителей и агрессивных химических сред – каучук подвергают вулканизации нагреванием до 130-140°С с серой.
Вулканизация – процесс получения резины из каучука.
В результате вулканизации молекулы каучука «сливаются» между собой дисульфидными (S - S) мостиками в одну трехмерную макромолекулу, и образуется пространственный полимер – резина, которая по прочности значительно превосходит невулканизированный каучук.
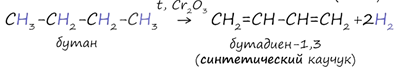
3. Дегидрирование алканов
В результате отщепления водорода от молекулы алкана образуются двойные связи. Дегидрирование происходит при повышенной температуре и в присутствии катализатора.
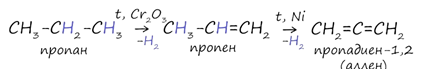
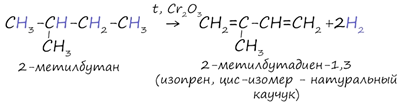
ХИМИЧЕСКИЕ СВОЙСТВА АЛКАДИЕНОВ
Алкадиены - ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны. Наличие сопряженных двойных связей увеличивает реакционную способность молекулы и обуславливает необычный механизм некоторых реакций.
Запомните, в сопряженных диенах присоединение протекает преимущественно как 1,4 – присоединение.
1. Гидрирование. Водород присоединяется к атомам углерода, образующим двойную связь.
![]()
![]()
![]()
2. Галогенирование
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение брома по кратным связям к органическому веществу. Также происходит обесцвечивание раствора перманганата калия (KMnO4).
![]() В
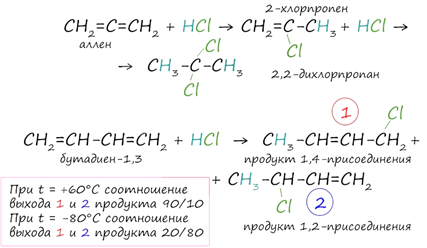
случае, если двойные связи находятся в сопряжении, выход продуктов во многом
зависит от температуры. Например, в ходе галогенирования бутадиена-1,3 при
-80°C преимущественно получается продукт 1,2-присоединения, а при +60°C -
продукт 1,4-присоединения.
В
случае, если двойные связи находятся в сопряжении, выход продуктов во многом
зависит от температуры. Например, в ходе галогенирования бутадиена-1,3 при
-80°C преимущественно получается продукт 1,2-присоединения, а при +60°C -
продукт 1,4-присоединения.
![]()
3. Гидрогалогенирование. Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена - к наименее гидрированному атому углерода.
4. Окисление. При горении алкадиены сгорают с образованием углекислого газа и воды.
![]() +
Q
+
Q
5. Полимеризация
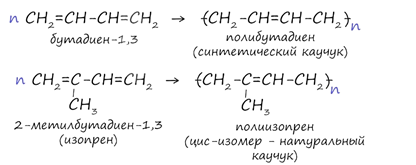
Натуральный каучук получают из млечного сока (латекса) каучуконосного дерева гевеи, растущего в тропических лесах Бразилии. При нагревании без доступа воздуха каучук распадается с образованием диенового углеводорода – 2- метилбутадиена-1,3 или изопрена.
Каучук – это полимер, в котором молекулы изопрена соединены друг с другом по схеме 1,4- присоединения с цис- конфигурацией полимерной цепи.
Натуральный каучук обладает уникальным комплексом свойств: эластичностью, износоустойчивостью, клейкостью, водо- и газонепроницаемостью, хороший изолятор, растворимостью в органических растворителях. Недостатки: при высокой t – размягчается, при низкой t – хрупкий.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.