
11 Б класс Дата: 28.09.20г.
Тема урока: Периодический закон. Распределение электронов в атомах элементов малых периодов.
Цель урока: Сформировать представление о строении электронной оболочки атомов.
Задачи урока:
Образовательная: продолжить формирование умения извлекать информацию из ПСХЭ;
Развивающая: продолжить развитие умений объяснять при выполнении заданий, делать выводы и анализировать;
Воспитательная: продолжить формирование мировоззрений, представление о единичном и целом, развитие элементов эстетического восприятия
Оборудование: презентация.
Ход урока:
1. Организационный момент
Здравствуйте, ребята! Сегодня на нашем уроке мы знакомимся с новой темой. Запишите в тетрадь ее название: “Периодический закон. Распределение электронов в атомах элементов малых периодов».
2. Мотивация
«У меня 7 электронов – кто я ?» (Азот)
«Мой символ Si - кто я?» (Кремний)
«Моя подруга живет в квартире №16, её имя - ?» ( Сера)
«У меня 20 нейтронов и 20 электронов, а живу я в подъезде номер ?» (Кальций)
«Я – фосфор, подскажите сколько у меня электронов» (15)
3. Актуализация знаний
- Что изучает химия?
- Что называют атомом, молекулой?
- Что такое абсолютная и относительная атомная и молекулярная массы? В каких единицах их выражают?
- Какие модели строения атома известны?
- Какие числа периодической системы можно использовать для описания строения атома и как?
-Какие периоды периодической системы называют большими и какие – малыми?
- Дайте определение понятия «орбиталь».
- Как определить число протонов, электронов (всего и на внешнем уровне), нейтронов с помощью чисел периодической системы?
4. Изучение нового материала
Современная формулировка периодического закона Д.И. Менделеева:
«Свойства химических элементов и образуемых ими простых и сложных веществ находятся в периодической зависимости от величины заряда ядра атомов этих элементов».
Причина периодического изменения свойств химических элементов кроется в строении электронной оболочки. Сущность явления периодичности: свойства элементов повторяются периодически потому, что периодически повторяется число электронов на внешнем энергетическом уровне атома.
Электронная оболочка атома состоит из электронов, распределённых по слоям – энергетическим уровням. Энергетический уровень обозначается латинской буквой n. Число энергетических уровне в атоме элемента равно номеру периода, в котором находится этот элемент. Электроны, наиболее прочно связанные с ядром и обладающие наименьшим запасом энергии, находятся на первом энергетическом уровне (n = 1).
Максимальное число электронов на уровне определяют по формуле
N = 2n2 (где n – номер уровня). На первом уровне (n = 1) могут находиться два электрона (N = 2 ∙ 12 = 2), на втором (n = 2) – восемь электронов
(N = 2 ∙ 22 = 8), на третьем (n = 3) – 18 электронов (N = 2 ∙ 32 = 18), на четвёртом (n = 4) – 32 электрона (N = 2 ∙ 42 = 32).
Орбиталь – это пространство вокруг атомного ядра, в котором наиболее вероятно нахождение электрона.
Каждый энергетический уровень делится на энергетические подуровни. Число подуровней равно номеру уровня, например, первый уровень состоит из одного подуровня (его называют s-подуровень).
Второй уровень состоит из двух подуровней s-подуровня и p- подуровня.
Третий уровень состоит из трёх подуровней: s-, p- и d-подуровня. Четвёртый уровень состоит из четырёх подуровней: s-, p-, d- и f-подуровня.
Каждый подуровень образован орбиталями, имеющими одинаковую форму и равную энергию. По форме различают s-, p-, d- и f-орбитали.
s-орбитали имеют форму шара, иными словами, электрон, находящийся на такой орбитали (его называют s-электроном), большую часть времени проводит внутри сферы. s-орбиталь, находящуюся на первом энергетическом уровне, обозначают 1s, на втором — 2s и т. д.
р-орбитали имеют форму объемной восьмерки. Они могут быть направлены по одной из трех координатных осей (обозначаются px,py, pz), поэтому на каждом энергетическом уровне (кроме первого, где есть только s-орбиталь) существуют три р-орбитали, обладающие одинаковой энергией.
Формы d- и f-орбиталей намного сложнее. На рисунке видно, что существует 5 форм d-орбиталей и 7 форм f-орбиталей.
На каждой из орбиталей могут размещаться не более двух электронов с противоположными спинами, следовательно, s-подуровень максимально вмещает 2 электрона, p – 6, d – 10, f – 14.
Орбитали одной и той же формы, но находящиеся на разных энергетических уровнях (например, 1s, 2s и 3s-орбитали), отличаются по энергии. Чем больше номер уровня, тем выше энергия орбитали и тем больше ее размер.
В первую очередь электронами заполняются орбитали того подуровня, который характеризуется наименьшей энергией. На одном и том же уровне наименьшей энергией обладает s-орбиталь, далее в порядке увеличения энергии следуют р-, d- и f-орбитали.
Вначале электроны поодиночке заполняют свободные орбитали энергетически выгодного подуровня, и только когда на каждой орбитали уже имеется по одному электрону, начинается их спаривание.
Запись электронной конфигурации атома. Подробные электронные конфигурации атомов изображают несколькими способами:
1) H +1 )1e– – схема строения атома, отображает распределение электронов по энергетическим уровням.
2) +1 Н 1s1 – электронная формула, отображает число электронов по уровням и по орбиталям.
3) +1 Н
|
↑1s |
- электронно-графическая формула – показывает распределение электронов по орбиталям и отображает спин электрона.
Распределение электронов в атомах элементов 1-го периода. Первый энергетический уровень вмещает максимально два электрона. Поэтому первый период состоит лишь из двух элементов – водорода и гелия. Простейший из атомов — водород. Он содержит один электрон, который занимает орбиталь с самой низкой энергией – 1s-орбиталь.
Электронная конфигурация атома водорода:
В атоме гелия первый энергетический уровень полностью завершен:
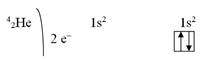
Элементы, в атомах которых заполняется s-подуровень, называют s-элементами. Водород и гелий - s-элементы.
Распределение электронов в атомах элементов 2-го периода. У элементов второго периода начинается заполнение второго энергетического уровня — он включает восемь электронов (n = 2, N = 8). Второй период содержит восемь элементов. У лития и бериллия заполняется 2s-орбиталь, это s-элементы. С бора начинает заполняться электронами р-подуровень. У неона, элемента, завершающего второй период, первый и второй энергетические уровни оказываются целиком заполненными.
Электронная конфигурация атома лития:

Электронная конфигурация атома бериллия:
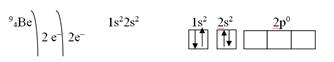
Электронная конфигурация и диаграмма атома бора:
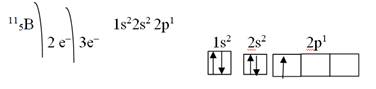
Электронная конфигурация атома углерода:
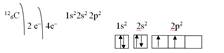
Электронная конфигурация атома неона:

Элементы, в атомах которых заполняется p-подуровень, называют p-элементами. От бора по неон - р-элементы.
Распределение электронов в атомах элементов 3-го периода. В третьем периоде происходит заполнение третьего энергетического уровня. Третий уровень (n = 3) может максимально вмещать 18 электронов. Однако элементов в третьем периоде всего восемь. К концу третьего периода (у аргона) полностью заполняются 3s- и 3p-подуровни, а 3d-подуровень остается пустым, поэтому третий уровень не заполняется до конца. От натрия до аргона заполнение электронами третьего уровня протекает аналогично заполнению второго уровня: заполняется вначале 3s-орбиталь (2 электрона), затем оставшиеся 3р-орбитали (6 электронов). Натрий и магний – это s-элементы, а с алюминия по аргон - р-элементы.
Таким образом, все элементы малых периодов относятся либо к s-, либо к р-элементам.
ВЫВОД.
Общее число электронов вокруг ядра равно заряду ядра (соответствует порядковому номеру ХЭ в ПСХЭ).
Электроны расположены на Е уровнях, число которых определяется номером периода в ПСХЭ, в котором находится ХЭ.
Число электронов на внешнем Е уровне соответствует номеру группы ПСХЭ, в которой находится ХЭ.
На внешнем Е уровне не может находиться более 8 электронов.
5. Закрепление изученного материала
Устное оценивание учащихся
Задание уровня А: вставьте пропущенные слова в тексте.
Атом - это ……………. частица, которая состоит из ……………… заряженного ядра и ………………. заряженных электронов.
Задание уровня В:
Ядра атомов состоят из элементарных частиц ……..видов : …………(p) и …………….(n). Сумма протонов и нейтронов в ядре одного атома называется ………………: где А - ………….число, N – число…………, Z – число…………
Задание уровня С:
Электроны распределяются по …………… орбиталям в соответствии с принципом ………… …………, принципом ……….. и правилом ………. . Такое распределение называется …………. ……………….. …………. .
6.Домашнее задание
___________________________________
7. Рефлексия.
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.