
ОБЛАСТНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «РОСЛАВЛЬСКИЙ МЕДИЦИНСКИЙ ТЕХНИКУМ»
Специальность: 33.02.01 «фармация»
УЧЕБНО-ИССЛЕДОВАТЕЛЬСКАЯ РАБОТА
ОЦЕНКА КАЧЕСТВА МАЗИ «ЛЕВОМЕКОЛЬ»
|
|
Выполнила студентка 3 курса Баранова Наталья Вадимовна
Научный руководитель: преподаватель профессионального цикла Вишневская Татьяна Александровна |
Рославль
2020 г.
СПИСОК СОКРАЩЕНИЙ
АТХ-классификация лекарственных средств – Анатомо-терапевтическо-химическая классификация лекарственных средств
ВФС – Временная фармакопейная статья
ВЭЖХ – высокоэффективная жидкостная хроматография
ГЛС – готовое лекарственное средство
ГОСТ – Государственный стандарт качества
ГФ – Государственная Фармакопея
ДНК – дезоксирибонуклеиновая кислота
ИК – инфракрасный
МЗ РФ – Министерство здравоохранения Российской Федерации
МКБ-10 – Международная классификация болезней 10-го пересмотра
М.м. – молекулярная масса
ОАО – Открытое акционерное общество
ОТК – Отдел контроля качества
РНК – рибонуклеиновая кислота
ТУ – Технические условия
УФ – ультрафиолетовый
ФС – Фармакопейная статья
ФСП – Фармакопейная статья предприятия
ХФК – химико-фармацевтическая компания
EAN (European Article Number) – Международная система товарных номеров
СОДЕРЖАНИЕ
|
ВВЕДЕНИЕ………………………………………………………………………... I ТЕОРЕТИЧЕСКАЯ ЧАСТЬ. МАЗИ КАК ЛЕКАРСТВЕННАЯ ФОРМА. ОБЩИЕ ПРИНЦИПЫ ОЦЕНКИ КАЧЕСТВА МАЗЕЙ………... I.1 Мази как лекарственная форма. Общая характеристика……………... I.2 Особенности технологии изготовления мазей. Показатели качества.. I.3 Нормативная документация, регламентирующая контроль и оценку качества мазей……………………………………….…………….. ВЫВОДЫ ПО ТЕОРЕТИЧЕСКОЙ ЧАСТИ…………….……………. II ПРАКТИЧЕСКАЯ ЧАСТЬ. ОЦЕНКА КАЧЕСТВА МАЗИ «ЛЕВОМЕКОЛЬ»………………………………………………………………... II.1 История создания и серийное производство мази «Левомеколь» в России………………………………………………. II.2 Стандартизация мази «Левомеколь»…………………………………. II.3 Оценка качества мази «Левомеколь»………………………………… ВЫВОДЫ ПО ПРАКТИЧЕСКОЙ ЧАСТИ…………………………… |
4
7 7 11
20 25
26
26 32 39 44 |
|
ЗАКЛЮЧЕНИЕ………………………………………………………………… СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ…………………………. |
45 48 |
ВВЕДЕНИЕ
У каждого из нас в домашней аптечке всегда есть свой проверенный набор медицинских препаратов, выручающих при различных неприятностях со здоровьем. Многие из них давно известные и не дорогие. Одним из подобных препаратов является «мазь первой помощи» – «Левомеколь».
Кто-то уже давно и постоянно пользуется этой мазью для лечения ран, кто-то знает о ее назначении, но не пробовал. Мазь для многих стала настоящей «палочкой-выручалочкой»: она быстро избавляет от прыщей, снимает воспаление на коже, лечит фурункулы, заживляет раны и язвы, укусы насекомых, инфицированные ожоги, сухие и мокрые мозоли, пролежни.
Часто «Левомеколь» называют «любимым помощником хирурга», поскольку его состав часто и широко используется врачами данной специальности для лечения гнойных ран и заживления послеоперационных швов, а также характеризуется прекрасным эффектом. Она имеет регенерирующие действие. Не подходит только тому, кто имеет аллергию на компоненты мази, не противопоказана детям, беременным и кормящим женщинам. Стоит мазь недорого, по цене доступна каждому, поэтому она давно известна и популярна среди населения и медицинских работников [25].
Мазь «Левомеколь» существует на российском рынке достаточно давно и отлично себя зарекомендовала. «Левомеколь» является наружным средством, которое обладает антибактериальным эффектом, одновременно улучшая восстановление нормальной структуры тканей ран различных форм, помогая быстрому заживлению [24].
Производится мазь «Левомеколь» двумя фирмами в России (ОАО «Химико-фармацевтический комбинат ''Акрихин''» и ОАО «Нижфарм») и должна соответствовать требованиям действующего российского законодательства в области производства и контроля качества лекарств [23]. [30], [31]. Оценка качества мази включает в себя как анализ лекарственных веществ, входящих в ее состав, так и показатели качества, характеризующие саму лекарственную форму с учетом современных требований.
Многие подходы являются общими для оценки качества мазей и, следовательно, можно выработать общие подходы к формированию показателей их качества. Однако, при оценке качества данной лекарственной формы необходимо учитывать свойства рассматриваемой мази как таковой: ее агрегатное состояние, структурно-механические свойства, особенности дозировки, набор и характер действующих и вспомогательных веществ и др. Определение подлинности и количественного содержания лекарственных веществ в мази «Левомеколь» обусловлено их физическими и химическими свойствами.
Востребованность рассматриваемого лекарственного препарата, а также особенности формирования показателей качества определяют актуальность выбранной темы.
Актуальность работы, степень ее разработанности обусловливают определение цели и задач, выбор объекта и предмета исследования.
Цель исследования: провести оценку качества мази «Левомеколь».
Задачи исследования:
1. Дать общую характеристику мазей как лекарственных форм;
2. Рассмотреть особенности технологии изготовления мазей и определить требования нормативной документации, регламентирующей контроль и оценку их качества;
3. Описать историю создания и выявить химико-фармацевтические компании по серийному производству лекарственного препарата;
4. Установить показатели стандартизации мази «Левомеколь», исходя из состава и физико-химических свойств лекарственного препарата;
5. Провести оценку качества мази «Левомеколь».
Предмет исследования: оценка качества мази «Левомеколь».
Объект исследования: мазь «Левомеколь» производства российских химико-фармацевтических компаний (ОАО «Нижфарм» и ОАО «Химико-фармацевтический комбинат ''Акрихин''»).
Методы исследования:
- изучение нормативной документации, специальной литературы и данных Интернет-источников;
- описание, наблюдение, сравнение, обобщение;
- органолептические, физические и химические методы фармацевтического анализа и оценки качества лекарственных препаратов.
База исследования: лаборатория контроля качества лекарственных средств ОГБПОУ «Рославльский медицинский техникум».
Тип работы: опытно-практический.
I ТЕОРЕТИЧЕСКАЯ ЧАСТЬ.
МАЗИ КАК ЛЕКАРСТВЕННАЯ ФОРМА.
ОБЩИЕ ПРИНЦИПЫ ОЦЕНКИ КАЧЕСТВА МАЗЕЙ
I.1 Мази как лекарственная форма. Общая характеристика
Мази – мягкой консистенции, сравнительно нестойкая недозированная лекарственная форма, предназначенная для нанесения на кожу, раны или слизистые оболочки и образующая сплошную пленку [17, с. 139]. Состоят из смеси фармацевтических веществ (жидких, или твердых, измельченных в порошок) и мазевой основы (жировой, нежировой, эмульсионной) [21, с. 5].
Традиционно мази применялись в терапии ряда дерматологических заболеваний. В настоящее время мази широко используются не только в дерматологии, но и в офтальмологии, отоларингологии, хирургии, гинекологии и других областях медицины [32].
Нанесение лекарственных веществ на поверхность кожи или слизистые оболочки в составе мазей обеспечивает хороший контакт лекарственных веществ и необходимую концентрацию в месте приложения действия. Системное действие лекарственных веществ в этом случае рассматривается как побочный эффект. Кроме местного воздействия на кожу и слизистые оболочки, лекарственные вещества в мазях могут оказывать общее резорбтивное действие за счет активного всасывания лекарственных веществ в кровь через эпидермис, волосяные фолликулы или сальные и потовые железы [6], [17, с. 139].
По характеру действия мази классифицируют на две группы:
1. Мази, оказывающие местное (локальное) действие непосредственно на верхний слой эпидермиса кожи или поверхность слизистой оболочки. Мази местного действия не всасываются кожей и слизистыми оболочками; они служат главным образом для сохранения их нормальных функций или для лечения заболеваний (повреждений) поверхностных слоев кожи. Обычно в состав таких мазей входят лекарственные вещества, оказывающие дезинфицирующее, вяжущее, адсорбирующее и прижигающее действие. Среди мазей местного действия различают покровные, защитные и косметические. Примерами могут служить мази, применяемые при лечении дерматитов, экзем и других заболеваний кожи.
2. Мази резорбтивного действия, глубоко проникающие в кожу или слизистую оболочку, достигающие кровяного русла и лимфы и оказывающие общее действие на весь организм или на отдельные органы. Чаще всего в эти мази прописывают гормоны, витамины и алкалоиды. Примером является мазь «Нитронг», содержащая 2% масляный раствор нитроглицерина и применяемая для профилактики приступов стенокардии [6], [17, с. 140].
С точки зрения технологии наибольшее значение имеет классификация, в основу которой положен тип дисперсной системы, образованной лекарственными веществами и основой. Согласно этой классификации, различают следующие типы мазей:
1. Гомогенные мази – характеризуются отсутствием межфазной поверхности раздела между лекарственными веществами и основой. В таких мазях лекарственные вещества распределены в основе по типу раствора, т.е. доведены до молекулярной или мицеллярной дисперсности. В зависимости от способа получения это могут быть:
- мази-сплавы – представляют собой сочетание нескольких плавких взаиморастворимых компонентов; в их состав могут входить жиры, воски, углеводороды, смолы, масла и другие вещества, а ингредиенты могут быть как твердыми, так и мягкими или жидкими;
- мази-растворы – мази, содержащие лекарственные вещества, растворимые в мазевой основе (независимо от ее природы);
- мази экстракционные – получают путем извлечения полезных веществ из растительного сырья, смешанного с жидкой или расплавленной основой [6].
2. Гетерогенные мази характеризуются наличием межфазной поверхности между лекарственными веществами и основой. В зависимости от характера распределения лекарственных веществ в основе гетерогенные мази классифицируют на три группы:
- суспензионные мази – в их состав входят лекарственные средства, практически нерастворимые в воде, основе и ее компонентах;
- эмульсионные мази – содержат жидкую фазу, не растворимую в основе и распределенную в ней по типу образования эмульсии;
- комбинированные (суспензионно-эмульсионные) мази – наиболее сложные многокомпонентные системы, включающие одновременно лекарственные вещества, растворимые в основе, нерастворимые порошкообразные ингредиенты и водные растворы лекарственных веществ, т.е. те, в которых одновременно находится несколько веществ с различными физико-химическими свойствами [6], [17, с. 141].
По физико-химическим признакам мази классифицируют на:
1. Однофазные – растворы, сплавы;
2. Двухфазные – эмульсии типа «масло в воде» и «вода в масле», суспензии, коллоидные дисперсии высших жирных спиртов или кислот, стабилизированные гидрофильными поверхностно-активными веществами;
3. Многофазные – множественные эмульсии «масло-вода-масло» и «вода-масло-вода», а также комбинированные системы [15, с. 115].
В зависимости от консистентных свойств мази классифицируют на несколько групп:
1. Собственно мази;
2. Пасты – мази плотной консистенции (суспензионные), содержание порошкообразных веществ в которых превышает 20-25 %;
3. Гели – мази вязкой консистенции, способные сохранять форму и обладающие упругостью и пластичностью;
4. Кремы (мягкие мази) – косметические средства в виде эмульсии типа «масло в воде» или «вода в масле»; от гелей отличаются содержанием масел и (обычно) непрозрачностью;
5. Линименты (жидкие мази) – смеси различных раздражающих веществ с маслами, масел с растворами щелочей, мыльно-водными или мыльно-спиртовыми растворами [6], [17, с. 142].
В зависимости от консистенции мази втираются, намазываются или накладываются на кожу.
Характер, продолжительность и место приложения действия мазей зависят от многих биофармацевтических факторов. К наиболее значимым из них следует отнести физико-химические свойства лекарственных и вспомогательных веществ и их концентрация, агрегатное состояние лекарственных веществ, их дисперсность, технология изготовления и др. Это обязывает к строгому подходу в обеспечении качества мазей и их контролю [21, с. 8].
I.2 Особенности технологии изготовления мазей.
Показатели качества
Производство мазей как мягких лекарственных форм сосредоточено в аптечных организациях, промышленных предприятиях и химико-фармацевтических фабриках и компаниях [16, с. 9].
В аптеках мази готовят по магистральным прописям. В современной экстемпоральной рецептуре аптек мази занимают 10-15 %. Однако производство мазей сконцентрировано, главным образом, на фармацевтических фабриках или крупных химико-фармацевтических заводах (крупнотоннажное производство), откуда они поступают в аптеку в готовом виде [18, с. 7].
Мази состоят из лекарственных веществ (твердых или жидких) и основы. Фармацевтическими факторами, в наибольшей степени влияющими на качество и биологическую доступность мазей, являются характер вспомогательных веществ и способ введения лекарственных веществ в мазевую основу [17, с. 141].
Отличительными особенностями производства мазей в заводских условиях является то, что их готовят в специальных цехах с применением сложного оборудования по технологиям, обеспечивающим их стабильность не менее 2-х лет, в соответствии с разработанной и утвержденной нормативно-технической документацией.
Производство мазей включает следующие технологические стадии:
1. Санитарная обработка производства;
2. Подготовка лекарственных веществ и основы;
3. Введение веществ в основу и их равномерное распределение в ней;
4. Стандартизация готовой продукции;
5. Упаковка и оформление [32].
В технологии мазей очень важными являются следующие факторы: степень дисперсности лекарственных веществ, способ введения лекарственных веществ в основу, время, скорость и порядок смешивания компонентов, температурный режим и другие параметры. Они влияют на консистенцию, реологические свойства, однородность, стабильность при хранении и фармакотерапевтическую эффективность мазей [21, с. 7].
При выборе оптимального варианта технологии изготовления мази необходимо учитывать характер кристаллов лекарственных веществ, способность веществ растворяться в различных средах (воде, глицерине, димексиде, растительных и минеральных маслах, полиэтиленгликолях, этаноле, диэтиловом эфире, хлороформе, расплавленном вазелине, ланолине безводном и т.д.), возможность физико-химического или химического взаимодействия между компонентами, свойства вспомогательных веществ (растворяющую, диспергирующую, эмульгирующую способности), температуры (плавления, затвердевания), вязкость, способность смешиваться с водой и другими средами и т.д. [6], [17, с. 142].
Санитарная обработка производства мазей направлена на обеспечение выпуска высококачественного готового продукта, предупреждение микробной контаминации (обсемененности) лекарственной формы в ходе производства, хранения и транспортировки, создание безопасных условий труда и охраны здоровья работающих [34].
Стадия подготовки основы включает в себя операции растворения или сплавления ее компонентов с последующим удалением механических примесей методом фильтрования.
Основу для мазей выбирают с учетом назначения лекарственного средства, эффективности, безопасности и биодоступности действующих веществ, совместимости компонентов лекарственного средства, реологических свойств, стабильности в течение срока годности [17, с. 143].
Основы, используемые при производстве мазей, подразделяются на несколько групп:
1. Гидрофобные: жировые (липофильные) (природные жиры, растительные масла, гидрогенизированные жиры и их сплав с растительными маслами и жироподобными веществами и др.), углеводородные (вазелин, вазелиновое масло, петролат, парафин, церезин и другие сплавы углеводородов), силиконовые (эсилон-аэросильная основа и др.) и др.;
2. Гидрофильные: гели высокомолекулярных углеводов (эфиры целлюлозы, крахмала, агара) и белков (желатина, коллагена и др.), гели неорганических веществ (бентонита), гели синтетических ВМС (полиэтиленоксида, поливинилпирролидона, полиакриламида) и др.;
3. Дифильные: абсорбционные основы (безводные сплавы гидрофобных основ (сплав вазелина с эмульгаторами), эмульсионные основы типа вода/масло (композиция воды, гидрофобной основы и соответствующего эмульгатора, консистентная эмульсия вода/вазелин и др.), реже – масло/вода (композиция липофильных компонентов, эмульгаторов и воды, в качестве эмульгаторов используют натриевые, калиевые, триэтаноламиновые соли жирных кислот) и др.) [6].
Плавящиеся компоненты основы расплавляют в специальных электрокотлах. Для слива растопленной массы их делают опрокидывающимися или со сливными кранами.
Расплавленную основу по обогреваемому трубопроводу переводят в реактор для приготовления мази. Для перекачивания расплавленной основы используют различные типы насосов, хорошо работающих в вязких средах [32].
В стадию подготовки лекарственных веществ включается измельчение, просеивание (если лекарственные вещества входят в мазь по типу суспензии) и растворение в воде или компоненте мазевой основы (если это мазь-эмульсия или мазь-раствор) [17, с. 144].
Стадия введения лекарственных веществ в основу может включать добавление твердых веществ к основе (мазь-суспензия) или растворение веществ в основе (мазь-раствор). В случаях комбинированных мазей могут осуществляться и тот, и другой процессы. Для введения лекарственных веществ в основу используются мазевые котлы или реакторы. Они снабжаются мощными мешалками, приспособленными для работы в вязких средах (якорные, грабельные или планетарные) [32].
Однако, с помощью одних мешалок нельзя добиться необходимой дисперсности мазей. Поэтому мази при их производстве подвергают гомогенизации, для чего используют мазетерки различных типов (дисковые, валковые, жерновые).
Существенно интенсифицировать процессы, протекающие при изготовлении мазей, а также повысить их устойчивость возможно с помощью вспомогательных веществ. В качестве вспомогательных веществ для мазей используют эмульгаторы типа масло/вода и вода/масло, гелеобразователи, антимикробные консерванты, антиоксиданты, солюбилизаторы, а также вещества, повышающие температуру плавления и вязкость, гидрофобные растворители, воду и гидрофильные растворители, отдушки и дезодорирующие средства, регуляторы рН, красители, ароматизаторы и др. Характер их может быть разнообразен: соединения тяжелых металлов, нерастворимые в мазевых основах и в воде, но растворимые в разведенных кислотах (цинка оксид, основной нитрат висмута и т.д.); нерастворимые в воде, мазевых основах и кислотах (каолин, тальк и др.); нерастворимые в мазевых основах, но растворимые в воде (ихтиол, борная кислота, йодид калия и др.); растворимые в мазевых основах и спирте, но нерастворимые в воде (ментол, камфора и др.); нерастворимые в воде, мазевых основах и кислотах вещества [6], [32].
В зависимости от состава мази и свойств входящих в нее лекарственных и вспомогательных веществ некоторые из описанных выше стадий могут быть совмещены. Например, современные автоматизированные линии производства мазей в больших количествах предполагают стадию гомогенизации мази, в результате которой обеспечивается как необходимая степень дисперсности лекарственных веществ, так и равномерное распределение их в мазевой основе [17, с. 143].
Технологический процесс изготовления мазей может быть периодическим и непрерывным. Периодический процесс может быть многоступенчатым и зависит от числа аппаратов, в которых последовательно проводят отдельные стадии.
На каждой из стадий приготовления мазей могут возникнуть ошибки как объективного, так и субъективного характера. Объективные ошибки при измерении массы лекарственных веществ и основы обусловлены метрологическими характеристиками используемых средств измерения массы. Ошибки субъективного характера должны быть исключены при промышленном производстве лекарственной формы, в то время как объективные погрешности не должны превышать допустимые предельные значения [16, с. 11].
Внутрицеховой контроль мазей осуществляется практически на каждой стадии производства и, особенно, перед фасовкой лекарственного препарата.
На предприятии контролируют внешний вид, запах и характерные органолептические свойства (при их наличии) мазей. Они не должны иметь прогорклого запаха, а также (если нет других указаний в частных статьях) признаков физической нестабильности (агрегации частиц, коалесценции, коагуляции и расслоения) [32].
Количество лекарственных веществ в мазях определяют по методикам, приведенным в частных фармакопейных статьях на испытуемую мазь или входящие в ее состав лекарственные вещества.
Стандартизация мазей и лечебных кремов по качественному и количественному содержанию лекарственных веществ или определение подлинности проводится визуально по внешнему виду и по органолептическим признакам, а также путем проведения качественных реакций на лекарственные вещества, входящие в их состав. Допустимое отклонение в содержании лекарственного вещества в мазях, линиментах, пастах и лечебных кремах не должно превышать ±5 %. При необходимости определяют подлинность вспомогательных веществ и тип основы [6], [32].
Однородность мазей определяют с учетом свойств конкретного препарата по внешнему виду или по следующей методике: для определения используют 4 пробы мази по 20-30 мг каждая, помещают по 2 пробы на предметное стекло, накрывают вторым предметным стеклом и плотно прижимают до образования пятен диаметром около 2 см. При рассмотрении полученных проб невооруженным глазом (на расстоянии около 30 см от глаз) во всех четырех пробах не должно быть включений и (если нет других указаний в частной статье) признаков физической нестабильности: агрегации и коалесценции частиц, коагуляций, расслоения. Если в одной из проб присутствуют видимые посторонние включения, то определение проводят дополнительно еще на восьми пробах. При этом во всех дополнительных пробах не допускается наличия посторонних включений [32].
Степень дисперсности частиц мазей определяют с помощью электронного микроскопа с окулярным микрометром по методике ОФС.1.4.1.0008.15 «Мази». Нормы степени дисперсности частиц являются индивидуальными для каждой мази и указаны в частных статьях [6].
Определение рН мазей необходимо для контроля поведения лекарственных веществ и основы во время хранения. Сдвиг рН свидетельствует об изменении их физико-химических свойств. Для определения рН мазей навеску препарата заливают 50 мл дистиллированной воды с температурой 50-60 0С и встряхивают на вибраторе в течение 30 минут. Полученную вытяжку фильтруют и проводят титрование по методике ОФС.1.2.1.19.0002.15 «Потенциометрическое титрование» [6].
Все мази, выпускаемые фармацевтическими предприятиями, имеют гарантийный срок хранения, в течение которого при правильном хранении они должны оставаться стабильными. Стабильность мазей определяется неизменностью содержания лекарственных веществ (в пределах установленного допуска), структурных свойств и скорости высвобождения лекарственных веществ. Особенно существенна проверка стабильности мазей в том случае, если они являются эмульсионными системами. Одной из приемлемых методик для проверки стабильности таких мазей является методика определения коллоидной устойчивости. Оценка коллоидной устойчивости мазей осуществляется на центрифуге при скорости 6000 оборотов в минуту в течение 5 минут. Под влиянием центробежной силы эмульсия разрушается тем быстрее, чем менее она стабильна. Отсутствие расслоения образца продукта свидетельствует об устойчивости композиции [6].
Термостабильность продукта определяют при нагревании мази в сушильном шкафу при температуре 60 0С в течение 1 часа. Если продукт качественный, то образец должен оставаться однородным без расслоения [32].
Иногда в мазях необходимо определять структурно-механические свойства (предельное напряжение сдвига, которое характеризует прочность структуры и консистенцию мази, и пластическую вязкость, характеризующую течение системы с разрушенной структурой), степень высвобождения лекарственных веществ из препарата и стабильность продукта при различных условиях хранения. Обычно эти определения осуществляются при разработке новых или усовершенствовании существующих мазей. Осуществляют эти определения согласно требований ОФС.1.4.1.0008.15 «Мази» [6].
Консистенция мазей и мазевых основ требует объективной оценки, поскольку она влияет на процессы их приготовления и расфасовки, легкость нанесения мазей на кожу и высвобождение из них лекарственных веществ. Одним из главных факторов, от которых зависит консистенция мазей, является предельное напряжение сдвига. Оно характеризует способность мазей оказывать некоторое сопротивление при размазывании, способность выдавливаться из туб, дозаторов и т.д.
Фасовку мазей производят с помощью шнековых и поршневых дозирующих машин в банки из стекла или полистирола, а также алюминиевые тубы.
Наиболее удобной и современной упаковкой для мазей являются тубы, изготовленные из металла или полимерных материалов. Туба является наиболее гигиеничной и удобной упаковкой – на нее можно наносить деления, допускающие дозирование мази, к ней могут прилагаться насадки (апликаторы) из пластмассы, позволяющие вводить мазь в полости и т.д. Внутренняя поверхность туб покрывается лаком, а наружная – эмалевой краской, на которую затем наносится маркировка [32].
Кроме описанных выше показателей качества мазей, контроль которых осуществляется перед фасовкой и упаковкой, после завершения всего процесса производства следует контролировать массу содержимого упаковки, которая должна быть не меньше массы, указанной на этикетке. Отклонение в массе мазей, расфасованных в тубы или баночки, проверяют взвешиванием десяти образцов [13].
Для стерильных и нестерильных мазей следует проводить определение герметичности упаковки в соответствии со следующей методикой: отбирают 10 туб с препаратом и тщательно вытирают их внешние поверхности фильтровальной бумагой. Тубы в горизонтальном положении помещают на лист фильтровальной бумаги и выдерживают в термостате при температуре 60±3 0С в течение 8 часов. На фильтровальной бумаге не должно быть подтеков препарата ни из одной тубы, при этом не принимают во внимание следы препарата, изначально находящиеся на резьбе колпачка и тубы. Если подтеки наблюдаются только из одной тубы, то испытание проводят дополнительно еще с 20 тубами. Результаты испытания считают удовлетворительными, если не наблюдалось подтеков из первых десяти туб или наблюдались подтеки только для одной из тридцати туб [9].
Окончательное заключение по всем показателям качества готовой продукции дает отдел контроля качества завода. В условиях промышленного производства испытание проводится в соответствии с требованиями ОФС.1.4.1.0008.15 «Мази», а также требованиями, включенными в статьи Государственной фармакопеи на отдельные наименования мазей.
Готовую мазь стандартизуют по внешнему виду, однородности, содержанию лекарственных веществ, значению рН, степени дисперсности твердых частиц, коллоидной устойчивости и термостабильности [6].
Упаковка и маркировка должны соответствовать требованиям ОФС.1.4.1.0001.15 «Лекарственные формы». Упаковка стерильных мазей должна быть герметичной и иметь приспособление для контроля первого вскрытия, (например, защитную мембрану) [5].
Хранят мази в упаковке, обеспечивающей стабильность в течение указанного срока годности лекарственного препарата, в защищенном от света месте при температуре от 8 до 15 0С, если нет других указаний в фармакопейной статье или другой нормативной документации. Для стерильных мазей необходимо устанавливать срок хранения после первого вскрытия [8], [10].
I.3 Нормативная документация, регламентирующая
контроль и оценку качества мазей
Характер нормативных документов, которыми следует руководствоваться как при изготовлении лекарственных форм, так и при контроле и оценке их качества, обусловлен характером изготовления лекарственных форм – заводским или в аптечных условиях [32].
Состав и технология мазей заводского изготовления регламентированы промышленными регламентами и спецификациями производства. Как было отмечено выше, в этом случае ошибки субъективного характера, как правило, будут исключены, а объективные ошибки будут обусловлены метрологическими характеристиками используемого на производстве оборудования [16, с. 11].
В отличие от контроля качества на производстве, при изготовлении мазей в условиях аптеки нормативных документов частного характера нет. Качество лекарственных форм, приготовленных по индивидуальным рецептам, определяется квалификацией провизора, который в своей работе руководствуется действующими нормативными документами общего характера (Государственная фармакопея РФ) и методическими указаниями [3], [16, с. 13], [38].
Внутрицеховой контроль мазей заводского изготовления осуществляется практически на каждой стадии и операции и, особенно, перед фасовкой лекарственного препарата с тем, чтобы убедиться в качественном изготовлении продукта. Окончательное заключение по всем показателям качества готовой продукции дает отдел технического контроля (ОТК) завода [35].
Для мазей заводского изготовления главными нормативными документами, регламентирующими производство, контроль и оценку их качества, являются:
1. Фармакопейная статья предприятия (ФСП) – стандарт качества лекарственного средства под торговым названием, содержащие перечень методов и показателей контроля качества лекарственного средства производства конкретного предприятия, где учитывается конкретная технология данного предприятия, прошедшая экспертизу и регистрацию в установленном порядке в соответствии с ГФ, фармакопейных статей настоящих стандартов. Показатели качества должны быть не ниже требований, находящихся в ГФ [35].
2. Спецификация производства – перечень испытаний, ссылок на аналитические методики и соответствующих критериев приемлемости, представляющих собой числовые пределы, интервалы или другие критерии для описываемых испытаний. В спецификации устанавливают набор критериев, которым должны соответствовать действующее вещество или лекарственный препарат для того, чтобы они считались пригодными для их предполагаемого применения. «Соответствие спецификациям» означает, что действующее вещество и/или лекарственный препарат соответствуют приведенным критериям приемлемости при условии, что испытания проведены согласно указанным в этих спецификациях аналитическим методикам [32].
Спецификации представляют собой необходимые стандарты качества, которые предлагает и обосновывает производитель, а согласовывают компетентные уполномоченные органы [36].
3. Спецификация на готовую продукцию – монография, определяющая качественные и количественные характеристики, которым должна соответствовать готовая продукция на момент ее производства (при выпуске), с указанием методик испытаний и допустимых пределов [32].
4. Технический регламент производства – нормативный документ, устанавливающий научно-обоснованный метод производства фармацевтической продукции и обеспечивающий получение лекарственного средства с показателями качества, отвечающими требованиям нормативной документации (ФС и ФСП), утвержденной МЗ РФ и ГФ [34].
Качество мази оценивают по тем технологическим показателям, которые являются общими для всех лекарственных форм. Оценивается внешний вид и органолептические признаки. Контроль качества мазей включает определение однородности, отклонения в массе, цвета, запаха, наличия или отсутствия механических включений, размера частиц (для суспензионных мазей). Наиболее важным специфическим показателем качества являются однородность и размер частиц лекарственных веществ в суспензионных и комбинированных мазях [6].
Мази стандартизируют по качественному и количественному содержанию лекарственных веществ.
Для оценки качества мазей заводского изготовления используют методики, приведенные в соответствующих статьях ГФ, ВФС, ФСП, ГОСТах, ТУ и др.
Общие требования, предъявляемые к мазям, изложены в ОФС.1.4.1.0008.15 «Мази» [6].
В ОФС.1.4.1.0008.15 «Мази» унифицированы особенности технологии изготовления мазей, а также определение размера частиц лекарственных веществ в мазях, которое позволяет определить не только размер частиц, но и их равномерное распределение в основе. В мазях должны отсутствовать частицы, размер которых превышает допустимый предел, указанный в частной ФС [6].
На различных стадиях изготовления мазей возможны потери действующего вещества. Для контроля этих погрешностей в блоке испытания мазей предусматривается определение количественного содержания лекарственных веществ. Содержание лекарственных веществ в мазях заводского изготовления обычно выражается в относительных единицах (%). ФС частного характера и ФСП регламентируют пределы количественного содержания лекарственных веществ, в которые должны укладываться результаты анализа [21, с. 10].
На стадии перенесения мази в тару для отпуска (в случае изготовления мази в аптечных условиях), либо при расфасовке мази в склянки или тубы (в случае заводского производства) возможны потери объективного характера, которые будут сказываться на общей массе мази. Вследствие неизбежности этих потерь ФСП регламентируется предел отклонений в общей массе мази [13].
Микробиологическая стабильность мазей обеспечивается соблюдением санитарных норм и правил при их производстве, а также применением консервантов. Однако мази могут быть контаминированы микроорганизмами в процессе транспортировки и хранения. Поэтому ГФ XIII регламентирует проведение испытания на микробиологическую чистоту по методике, унифицированной в ОФС.1.2.4.0002.15 «Микробиологическая чистота» [7].
Некоторые мази, например глазные или предназначенные для обработки послеоперационных областей, должны быть стерильными. Их стерильность достигается соблюдением необходимых санитарно-гигиенических условий и режима стерилизации. Для таких мазей предусматривается испытание на стерильность, о чем имеются соответствующие указания в ФС. Испытание на стерильность унифицировано и изложено в ОФС.1.2.4.0003.15 «Стерильность» [9].
Наиболее распространенными химическими процессами, приводящими к нарушению стабильности мазей, являются гидролиз и окисление основ. Основы могут также подвергаться окислению под воздействием кислорода воздуха на свету или примесей металлов с переменной валентностью. Продукты деструкции основ, в частности, альдегиды и кетоны придают мази прогорклый запах. Кроме того, они могут оказывать непосредственное раздражающее действие на кожу и слизистые оболочки при нанесении мази. Образующиеся в результате прогоркания основы активные частицы могут инициировать процессы разложения лекарственных веществ в составе мазей [21, с. 15].
Стабильность действующих веществ в мазях оценивают по появлению продуктов их разложения, а стабильность основы изучают по процессам гидролиза и окисления с использованием показателей рН, кислотного, перекисного и йодного чисел, определяемых по унифицированным фармакопейным методикам ОФС.1.4.1.0008.15 «Мази». Проведение данных исследований позволяет определять сроки годности при соблюдении условий хранения и делает возможным исключение этих испытаний при оценке качества готовых мазей. Поэтому в ОФС «Мази» определение кислотного, перекисного и йодного чисел не регламентируется [6], [21, с. 15].
Таким образом, основными факторами нарушения стабильности мазей являются свет, влага, повышенная температура, содержащиеся в качестве примесей соединения металлов с переменной валентностью и др. Поэтому упаковка и условия хранения мазей должны исключать влияние этих факторов. Упаковка и маркировка должны соответствовать требованиям ОФС.1.4.1.0001.15 «Лекарственные формы» [5].
Хранят мази в соответствии с требованиями ОФС.1.1.0010.15 «Хранение лекарственных средств» [10].
Стабильность мазей изучают общепринятыми методами долгосрочного испытания стабильности и испытания стабильности методом «ускоренного старения» согласно требований ОФС.1.1.0009.15 «Сроки годности лекарственных средств». Требования данной статьи распространяются на методы определения стабильности лекарственных средств промышленного производства, которые лежат в основе установления их сроков годности [8].
ВЫВОДЫ ПО ТЕОРЕТИЧЕСКОЙ ЧАСТИ
1. В теоретической части работы дана общая характеристика мазей как лекарственных форм. Выяснено, что мази представляют собой сравнительно нестойкую недозированную лекарственную форму мягкой консистенции, предназначенную для нанесения на кожу, раны или слизистые оболочки и образующую сплошную пленку. Состоят мази из лекарственных веществ и мазевой основы.
2. Рассмотрены особенности технологии изготовления мазей в аптечных организациях, промышленных предприятиях и химико-фармацевтических фабриках. Они определяют показатели качества контролируемой лекарственной формы. К наиболее значимым из них следует отнести внешний вид, запах и характерные органолептические свойства (при их наличии) мазей, физико-химические свойства лекарственных и вспомогательных веществ и их концентрацию, дисперсность, степень чистоты, отклонения в массе, характер упаковки и маркировки. Внутрицеховой контроль качества осуществляется на каждом этапе производства мази.
3. Определены требования и характер нормативных документов, которыми следует руководствоваться как при изготовлении мазей, так и при контроле их качества. Состав, технология и оценка качества мазей заводского изготовления регламентированы государственными стандартами качества РФ (ОФС.1.4.1.0001.15 «Лекарственные формы», ОФС.1.4.1.0008.15 «Мази», ОФС.1.2.4.0002.15 «Микробиологическая чистота», ОФС.1.2.4.0003.15 «Стерильность», ОФС.1.1.0010.15 «Хранение лекарственных средств», ОФС.1.1.0009.15 «Сроки годности лекарственных средств», а также частными ФС, описывающими качественное и количественное определение лекарственных веществ, входящих в состав лекарственного препарата) и промышленными регламентами (ФСП, спецификациями производства, техническими условиями и др.).
II ПРАКТИЧЕСКАЯ ЧАСТЬ.
ОЦЕНКА КАЧЕСТВА МАЗИ «ЛЕВОМЕКОЛЬ»
II.1 История создания и серийное производство
мази «Левомеколь» в России
Задача разработки комбинированного лекарства, которое обладает антисептическим, обезболивающим и ранозаживляющим действием, была поставлена перед отечественными фармацевтами в середине 70-х годов XX века [24].
В 1978 году на суд Фармакологического комитета Министерства здравоохранения СССР было представлено лекарство, ставшее прототипом мази «Левомеколь». В его состав было включено 6 основных компонентов. Действие антибиотика левомицетина разработчики усилили другими антибактериальными веществами (сульфаниламидами, диоксидином, йодовидоном). Мазь содержала местный анестетик, не теряющий активности при нагноении. За ранозаживление и восстановление нормальной трофики тканей отвечал метилурацил – модулятор обмена веществ. Очищению пораженной зоны способствовал полиэтиленгликоль. Аналоги данного препарата, который, как показали доклинические испытания, помогает в местном лечении ран, в мировой практике на тот момент отсутствовали [24], [27].
Однако мазь с такими компонентами не была поддержана Фармакологическим комитетом СССР: состав показался комиссии неоправданно сложным. Сложность состава не означала отсутствия эффективности: пока разработчики пытались добиться официального признания, мазь активно заказывали для лечения пострадавших в авариях; было выяснено, что он помогает при пролежнях и даже от прыщей [24].
«Подопытными пациентами» многокомпонентного препарата посчастливилось быть генералам, профессорам, чиновникам и их родственникам.
Несмотря на положительные отзывы, второй раз представлять препарат в Фармакологическом комитете не позволялось. Поэтому следующая задача, которая встала перед фармацевтами, заключалась в том, чтобы упростить состав мази при сохранении ее эффективности [24].
Результатом оптимизации состава комплексного препарата стала мазь, действие которой обусловлено следующими компонентами:
- левомицетином (хлорамфениколом), получаемым из культуры бактерий Streptomyces venezuelae, а также химическим синтезом. Антибиотик угнетает синтез белка в бактериальных клетках, от чего грамположительные и грамотрицательные бактерии теряют способность к нормальному обмену веществ, размножению и, в итоге, разрушаются. К данному веществу особо чувствительны возбудители бруцеллеза, брюшного тифа, туляремии, сальмонеллеза, риккетсиоза, хламидиоза [27];
- метилурацилом – веществом, молекулы которого структурно похожи на мономер нуклеиновых кислот (ДНК, РНК). Идея использовать подобные средства для стимулирования регенерации возникла еще в 1946 году. Точные молекулярные механизмы действия данного компонента изучены недостаточно, чего не скажешь о накоплении многочисленных данных об эффектах его использования: стимуляция регенерации, синтеза лейкоцитов и эритроцитов, активация фагоцитоза, болеутоляющее и противовоспалительное действие, уменьшение токсичности антибиотиков. Таким образом, спектр возможного для мази применения стал более широким, не ограничиваясь антибактериальным действием [29];
- полиэтиленоксидом – гидрофильной основой мази. Состав препарата включает два варианта этого полимера, различающиеся молекулярной массой. Подобно насосу, эти вещества «вытягивают» воду, освобождая рану от гноя, а также усиливают активность основных компонентов, способствуя их диффузии в ткани [24].
Новый препарат назвали мазь «Левомеколь». Мази, состав которой лишился анестетика и сульфаниламидов, были разрешены клинические испытания. Было установлено, что эта комбинированная мазь оказывает множественный эффект на звенья воспалительного процесса, существенно сокращая сроки заживления ран.
Позже эффективность мази «Левомеколь» была подтверждена в экстремальных условиях. В частности, мазь использовали во время войны в Афганистане, землетрясения в Спитаке [24].
В 1985 году началось серийное производство лекарственного препарата. Оно стало одним их самых востребованных благодаря оценке по критерию эффект/цена.
В настоящее время тюбик мази «Левомеколь» ценой около 100 рублей остается доступным и проверенным средством, которое часто встречается в домашних аптечках. Когда антисептического действия недостаточно и необходимо снижать воспаление и болевой синдром, устранять гнойное содержимое и некрозы, восстанавливать обменные процессы, применяется мазь «Левомеколь». В прилагаемой к мази инструкции по применению названы следующие показания, когда целесообразно использовать препарат:
- гнойные раны (медикамент применяется в основном в первой фазе раневого процесса);
- ожоги (тепловые, электрические, химические, радиационные);
- трофические язвы (в частности, лекарство применяется на запущенных стадиях сахарного диабета, венозной недостаточности нижних конечностей);
- пролежни (начальные стадии);
- дерматологические проблемы [25].
Учитывая действие антибактериального компонента мази «Левомеколь», показанием к применению являются, прежде всего, случаи инфицирования стафилококком. Фурункулы, карбункулы бактериальной природы – основные кожные проблемы, указанные в прилагающейся к мази инструкции по применению [24].
В настоящее время мазь «Левомеколь» производится двумя фирмами в России – ОАО «Нижфарм» и ОАО «Химико-фармацевтический комбинат ''Акрихин''» (таблица 2.1) [30], [31].
Таблица 2.1.
Производители мази «Левомеколь в России
|
№ п/п |
Химико-фармацевтическая компания |
Адрес, контакты |
Стадии производства |
|
1 |
ОАО «Нижфарм» |
603950, Нижний Новгород, ГСП-459 ул. Салганская, д. 7 Тел: +7 831 278 8088 Е-mail: med@nizhpharm.ru Cайт: http://www.nizhpharm.ru |
Все стадии, включая выпускающий контроль качества мази «Левомеколь» |
|
2 |
ОАО «ХФК ''Акрихин''» |
109029, г. Москва, Сибирский проезд, д.2 стр. 1 Тел: 721-36-97 (98) Cайт: http://www.akrihin.ru |
Компания «Нижфарм» – одна из ведущих фармацевтических компаний России. На протяжении последних 90 лет она разрабатывает, производит и предлагает потребителям более 100 наименований лекарственных средств.
Производство ОАО «Нижфарм» представляет современный комплекс, располагающийся в Нижнем Новгороде почти на 11,5 тыс. кв. метров с цехами по производству мазей, кремов, суппозиториев, линиментов, таблеток. Лекарственные препараты производятся на современном высокотехнологичном оборудовании из качественного сырья на основе современных технологий [31].
ОАО «ХФК ''Акрихин''» выпускает около 150 наименований лекарственных препаратов основных фармакотерапевтических групп: сердечно-сосудистых, психотропных препаратов, противомикробных и противовирусных средств, препаратов для лечения заболеваний желудочно-кишечного тракта, современных противоаллергических средств. В их числе оригинальные бренды и ГЛС, защищенные товарным знаком «АКРИ». Продукция представлена практически всеми лекарственными формами: таблетки, капсулы, драже, мази, сиропы, шампунь, гели. 9 торговых наименований препаратов выпускается в больничной упаковке [30].
По данным DSM Group, ОАО «ХФК ''Акрихин''» входит в пятерку крупнейших российских фармацевтических компаний. Объем продаж в 2016 году превысил 60 млн. долларов. Доля комбината составляет около 0,6 % среди всех производителей мазей на российском фармацевтическом рынке [39].
По данным Государственного реестра лекарственных средств, в России зарегистрировано 9 форм выпуска мази «Левомеколь» (таблица 2.2) [4].
Таблица 2.2.
Зарегистрированные формы выпуска мази «Левомеколь» в России
|
№ п/п |
Химико-фармацевти-ческая компания |
Зарегистрированная форма выпуска |
Цена (по данным портала АНАЛОГИ-ЛЕКАРСТВ.РФ |
|
1 |
ОАО «Нижфарм» |
Мазь для наружного применения; банка (баночка) темного стекла 100 г, пачка картонная 1. Код EAN: 4601026006029. Регистрационное удостоверение № Р N003107/01, 2009-11-17 |
63-153 руб. Средняя – 108 руб. |
|
2 |
Мазь для наружного применения; банка (баночка) темного стекла 1000 г, упаковка бумажная 1. Код EAN: 4601026006036. Регистрационное удостоверение № Р N003107/01, 2009-11-17 |
||
|
3 |
Мазь для наружного применения; туба алюминиевая 40 г, пачка картонная 1. Код EAN: 4601026006845. Регистрационное удостоверение № Р N003107/01, 2009-11-17 |
||
|
4 |
Мазь для наружного применения; пакет (пакетик) полиэтиленовый 28 кг, бочка (бочонок) стальная (ой) 1. Регистрационное удостоверение № Р N003107/01, 2009-11-17 |
||
|
5 |
Мазь для наружного применения; пакет (пакетик) полиэтиленовый 150 кг, бочка (бочонок) стальная (ой) 1. Регистрационное удостоверение № Р N003107/01, 2009-11-17 |
||
|
6 |
Мазь для наружного применения; туба алюминиевая 30 г, пачка картонная 1. Регистрационное удостоверение № Р N003107/01, 2009-11-17 |
||
|
7 |
Мазь для наружного применения; туба алюминиевая 50 г, пачка картонная 1. Регистрационное удостоверение № Р N003107/01, 2009-11-17 |
||
|
8 |
ОАО «ХФК ''Акрихин''» |
Мазь для наружного применения; банка (баночка) темного стекла 60 г, пачка картонная 1. Код EAN: 4601969002003. Регистрационное удостоверение № ЛС-001168, 2006-01-19 |
59-142 руб. Средняя – 83 руб. |
|
Продолжение Таблицы 2.2. |
|||
|
9 |
|
Мазь для наружного применения; туба алюминиевая 40 г, пачка картонная 1. Код EAN: 4601969002690. Регистрационное удостоверение № ЛС-001168, 2006-01-19 |
|
Стоит отметить, что, по данным Российского Инфо-портала о лекарствах Farmanews.ru, мазь «Левомеколь» входит в десятку самых востребованных лекарств. Так, пресс-служба руководства департамента продаж ОАО «Нижфарм» заявляет о реализации около 500 тысяч упаковок мази ежемесячно. Цена препарата и эффекты лечения, судя по отзывам, вполне устраивают большинство пациентов [40].
II.2 Стандартизация мази «Левомеколь»
Наименование на русском языке: Левомеколь.
Наименование на латинском языке: «Laevomecolum».
Действующее вещество: Диоксометилтетрагидропиримидин (Dioxomethyltetrahydropyrimidinum) + Хлорамфеникол (Chloramphenicolum).
Производитель: ОАО «Нижфарм» (Россия), ОАО «Химико-фармацевтический комбинат ''Акрихин''» (Россия).
Группа: Лекарственные средства.
Форма выпуска: мазь для наружного применения.
Классификация по МКБ-10: [T14.1] Открытая рана неуточненной области тела.
Фармакологическая группа: другие противомикробные, противопаразитарные и противоглистные средства.
Код АТХ: D03AX. Антибиотики в комбинации с другими противомикробными препаратами [4].
Состав:
Мазь – 100 г:
левомицетин – 0,75 г,
метилурацил – 4,0 г [24].
Фармакологическое действие: противовоспалительное, антибактериальное.
Показания к применению: гнойные раны, инфицированные смешанной флорой, включая стафилококки, синегнойные и кишечные палочки [26].
Способ применения и дозы: наружно. Препаратом пропитывают стерильные марлевые салфетки, которыми рыхло заполняют рану. Возможно введение в гнойные полости через катетер (дренажную трубку) с помощью шприца. В этом случае мазь предварительно подогревают до 35-36 °C. Перевязки производят ежедневно, до полного очищения раны от гнойно-некротических масс [25].
Стандартизация готовой продукции проводится согласно следующей нормативной документации:
1. Государственные стандарты качества:
- ГФ XIII ОФС.1.4.1.0008.15 «Мази» (введена взамен ст. ГФ XI);
- ГФ XIII ОФС.1.2.4.0002.15 «Микробиологическая чистота» (введена взамен ГФ ХI, вып. 2, стр. 193, изменений № 2, 3, ОФС 42 -0016-04, ГФ XII, ч. 1, ОФС 42-0067-07);
- ГФ XIII ОФС.1.2.4.0003.15 «Стерильность» (введена взамен ГФ XII ОФС 42-0066-07);
- ГФ XIII ОФС.1.4.1.0001.15 «Лекарственные формы» (введена впервые);
- ГФ XIII ОФС.1.1.0010.15 «Хранение лекарственных средств» (введена впервые);
- ГФ XIII ОФС.1.1.0009.15 «Сроки годности лекарственных средств» (введена взамен ОФС 42-0075-07 ГФ ХII, ч.1);
- ГФ XIII ФС «Диоксометилтетрагидропиримидин (метилурацил)» (введена взамен ГФ XII, ч.1, ФС 42-0256-07);
- ГФ XIII ФС «Хлорамфеникол (левомицетин)» (введена взамен ГФ XII, ч.1, ФС 42-0250-07).
2. Частная нормативная документация:
- ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''» 42-0017-6136-05.
Оценка качества мази «Левомеколь» проводится визуально по внешнему виду и органолептическим признакам (запах и др.), зависящим от свойств входящих в мазь лекарственных веществ и от использованных мазевых основ [6].
Для определения однородности используют четыре пробы мази по 0,02- 0,03 г, помещая их по две на предметное стекло. Покрывают вторым предметным стеклом и плотно прижимают до образования пятен диаметром около 2 см. При рассматривании полученных пятен невооруженным глазом (на расстоянии около 30 см от глаза) в трех из четырех проб не должно обнаруживаться видимых частиц. Если частицы видны в большем числе пятен, определение проводят повторно на восьми пробах. При этом допускается наличие видимых частиц не более чем в двух пятнах [6], [21, с. 7].
Для оценки качества комбинированного препарата мази «Левомеколь» нормативной документацией предусматривается проведение качественных реакций на лекарственные вещества, входящие в состав мази: из точной навески препарата должен быть приготовлен испытуемый спиртовой раствор (ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''»). Оптические плотности полученного раствора измеряют на спектрофотометре в УФ-спектре в кювете с толщиной слоя 10 мм при длинах волн 258 нм и 278 нм [13].
Параллельно в тех же условиях измеряют спектры поглощений при длинах волн от 258 до 278 нм рабочего стандартного раствора. В качестве раствора сравнения используют воду [13].
Согласно ГФ XIII, допустимые нормы составляют: диоксометилтетрагидропиримидина (метилурацила) – от 3,6 до 4,4 %, хлорамфеникола (левомицетина) – от 0,67 до 0,83 % [3].
ГФ XIII регламентирует применение физико-химических и химических методов оценки качества составных компонентов мази «Левомеколь».
Диоксометилтетрагидропиримидин
Метилурацил
2,4-дигидрокси-6-метилпиримидин
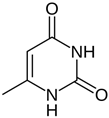
|
C5H6N2O2 |
М.м. 126,11 |
1. ИК-спектр. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру стандартного образца метилурацила.
2. ВЭЖХ. Время удерживания основного пика на хроматограмме испытуемой субстанции должно соответствовать времени удерживания основного пика на хроматограмме стандартного образца («Родственные примеси»).
3. УФ-спектр. Ультрафиолетовый спектр поглощения 0,001 % раствора субстанции в области длин волн от 220 до 300 нм должен иметь максимум при 260 нм и минимум при 231 нм [11].
4. Качественная реакция. К 0,1 г субстанции прибавляют 10 мл бромной воды и встряхивают; бромная вода должна обесцветиться в течение 5 минут.
Метилурацил, как и другие препараты группы урацила, взаимодействуют с бромом с образованием соответствующих бромпроизводных. Реакцию применяют для определения подлинности индивидуального метилурацила в порошке и в мази [22], [36]:
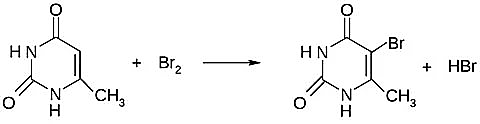
Данную реакцию можно использовать и для количественного броматометрического количественного определения метилурацила [14].
К реакциям подлинности метилурацила в мазях относится и образование азокрасителей с солями диазония (по образованию красно-оранжевого осадка под действием раствора пара-нитродиазобензола) [19, с. 383], [20, с. 83].
Количественное определение метилурацила методом неводного титрования основано на титровании таутомерной лактимной формы препарата в безводном диметилформамиде раствором метилата натрия в метаноле; индикатор – тимоловый синий, титрование проводится до появления синего окрашивания [14, с. 431], [29]:
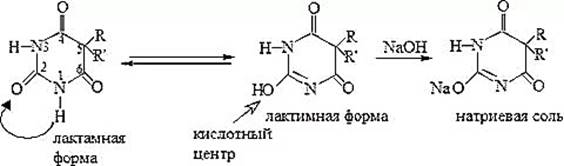
Хлорамфеникол
Левомицетин
D-(−)-трео-1-(п-нитрофенил)-2-дихлор-ацетиламино-1,3-пропандиол
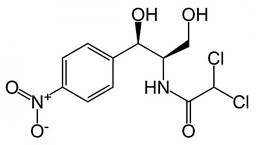
|
C11H12Cl2N2O5 |
М.м. 323,13 |
1. ИК-спектр. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру стандартного образца хлорамфеникола.
2. УФ-спектр. Ультрафиолетовый спектр 0,002 % раствора субстанции в 0,1 М растворе хлористоводородной кислоты в области длин волн от 220 до 400 нм должен иметь максимум поглощения при 278 нм и минимум поглощения при 237 нм [12].
3. Качественная реакция. 0,1 г субстанции нагревают на водяной бане с 5 мл 20 % раствора натрия гидроксида; должно появиться желтое окрашивание, переходящее в красно-оранжевое. При дальнейшем нагревании окраска усиливается, выпадает кирпично-красный осадок и выделяется аммиак, обнаруживаемый по запаху и по посинению влажной лакмусовой бумаги.
4. Качественная реакция. Раствор, полученный в предыдущем испытании, нейтрализуют азотной кислотой разведенной по бумаге индикаторной универсальной и фильтруют. Фильтрат дает характерную реакцию на хлориды с серебра нитратом в азотнокислой среде [12].
Качественные реакции испытания подлинности основаны на гидролитическом расщеплении лекарственного вещества в щелочной среде с последующей идентификацией образующихся продуктов [14, с. 79], [27]:
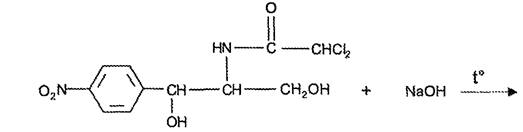
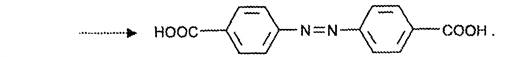
При нагревании в течение 1-2 минут с 15% раствором гидроксида натрия левомицетин приобретают желтое окрашивание, переходящее в красно-оранжевое. При дальнейшем нагревании в щелочной среде левомицетин образует кирпично-красный осадок аци-формы пара-нитрофенилпропандиола-1,3. Одновременно ощущается запах аммиака. Фильтрат после подкисления азотной кислотой дает характерную реакцию на хлориды. Это позволяет подтвердить наличие в молекуле левомицетина нитрофенильного радикала, аминогруппы и ковалентносвязанного атома хлора [28], [37].
Известны многочисленные способы идентификации и количественного определения левомицетина, основанные на предварительном восстановлении (цинковой пылью в кислой среде) нитрогруппы в молекуле левомицетина до аминогруппы. Одновременно отщепляются атомы хлора [19, с. 465]:
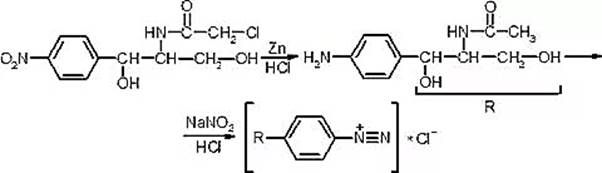
Образовавшийся 1-пара-аминофенил-2-ацетиламинопропандиол-1,3 диазотируют и превращают в азокраситель, сочетая с β-нафтолом, α-нафтиламином или другим амином или фенолом (в результате азосочетания с β-нафтолом образуется азокраситель красного цвета) [28].
ГФ XIII также рекомендует применение метода тонкослойной хроматографии [3].
Срок хранения препарата: 3,5 года. Условия хранения: в сухом, защищенном от света месте, при температуре не выше 20 °C. Хранить в недоступном для детей месте [26].
Условия отпуска: без рецепта. Не применять по истечении срока годности, указанного на упаковке [4].
II.3 Оценка качества мази «Левомеколь»
Для достижения поставленной цели и решения задач в ходе выполнения работы проведена оценка качества мази «Левомеколь» на примере двух образцов в тубе алюминиевой 40 г двух крупнейших российских заводов-изготовителей – ОАО «Нижфарм» и ОАО «Химико-фармацевтический комбинат «Акрихин». Лекарственные препараты приобретены в аптеке г. Рославль Смоленской области «Сердце Смоленска». Аналитические работы произведены на базе лаборатории контроля качества лекарственных средств ОГБПОУ «Рославльский медицинский техникум» с учетом имеющегося оборудования и реактивов.
1. Оценка упаковки и маркировки мази «Левомеколь»: требования установлены правилами упаковки и маркировки, размещенной на упаковках лекарственных средств для медицинского применения, изложенными в Федеральном законе РФ от 12.04.2010 г. № 61-ФЗ (ред. от 28.12.2017 г.) «Об обращении лекарственных средств» и проекте ОФС «Упаковка, маркировка и транспортирование лекарственного растительного сырья и лекарственных растительных препаратов» (таблица 2.3).
Таблица 2.3
Оценка упаковки и маркировки мази «Левомеколь»
|
№ п/п |
Химико-фармацевти-ческая компания |
Требования нормативной документации к первичной упаковке |
Требования нормативной документации к вторичной упаковке |
Вывод о соответствии/ несоответствии |
|
1 |
ОАО «Нижфарм» |
Туба алюминиевая 40 г. Указано: - торговое наименование препарата; - дозировка; - наименование производителя и его товарный знак (логотип); - номер серии; - срок годности/дата истечения срока годности. |
Пачка картонная вместе с инструкцией по применению на русском языке. Указано: - торговое наименование препарата; - международное непатентованное наименование; - наименование производителя и его товарный знак (логотип); - адрес владельца регистрационного удостоверения; |
Соответствует требованиям нормативной документации
|
|
2 |
ОАО «ХФК ''Акрихин''» |
Соответствует требованиям нормативной документации |
||
|
Продолжение Таблицы 2.3 |
||||
|
|
|
|
- лекарственная форма; - дозировка; - состав; - номер серии; - дата производства; - срок годности/дата истечения срока годности; - условия хранения; - способ применения; - условия отпуска; - штрих-код. |
|
2. Определение и оценка внешнего вида мази «Левомеколь»: регламентирована ОФС.1.4.1.0008.15 «Мази» и частной нормативной документацией ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''» 42-0017-6136-05; проведена органолептически (таблица 2.4) [3].
Таблица 2.4
Определение и ценка внешнего вида мази «Левомеколь»
|
№ п/п |
Химико-фармацевти-ческая компания |
Требования нормативной документации
|
Вывод о соответствии/несоответствии |
|
1 |
ОАО «Нижфарм»
|
Описание: мазь белого или белого с желтоватым оттенком цвета. Прогорклого запаха не имеет.
|
Соответствует требованиям нормативной документации |
|
2 |
ОАО «ХФК ''Акрихин''»
|
Соответствует требованиям нормативной документации |
3. Определение и оценка однородности мази «Левомеколь»: регламентировано ОФС.1.4.1.0008.15 «Мази» и частной нормативной документацией ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''» 42-0017-6136-05. Четыре пробы препарата по 0,02 г помещают по две на предметное стекло, закрывают другим предметным стеклом и плотно прижимают до образования пятен диаметром около 2 см. Пятна рассматривают невооруженным глазом на расстоянии 25-30 см (таблица 2.5) [3].
Таблица 2.5
Определение и оценка однородности мази «Левомеколь»
|
№ п/п |
Химико-фармацевти-ческая компания |
Требования нормативной документации
|
Вывод о соответствии/несоответствии |
|
1 |
ОАО «Нижфарм»
|
Однородность: не менее, чем в трех пробах не должно наблюдаться видимых частиц. Видна сетчатая структура препарата.
|
Соответствует требованиям нормативной документации |
|
2 |
ОАО «ХФК ''Акрихин''»
|
Соответствует требованиям нормативной документации |
4. Определение и оценка массы содержимого тубы мази «Левомеколь»: регламентировано ОФС.1.4.1.0001.15 «Лекарственные формы» и частной нормативной документацией ФСП ОАО «Химико-фармацевтический комбинат "Акрихин''» 42-0017-6136-05. Алюминиевую тубу с мазью взвешивают с точностью до 0,01 г, делают продольный разрез ножницами. Затем тубу освобождают от содержимого, промывая ее горячей водой. Тщательно удаляют остатки влаги фильтровальной бумагой и снова взвешивают (таблица 2.6) [3].
Таблица 2.6
Определение и оценка массы содержимого тубы мази «Левомеколь»
|
№ п/п |
Химико-фармацевти-ческая компания |
Масса содержимого тубы
|
Отклонение |
Требования нормативной документации |
Вывод о соответствии/ несоответствии |
|
1 |
ОАО «Нижфарм»
|
39,31 г
|
40,0 г – 100 % 0,69 г – х % х = 1,73 % |
40 г ± 4 % |
Соответствует требованиям нормативной документации
|
|
2 |
ОАО «ХФК ''Акрихин''»
|
38,64 г |
40,0 г – 100 % 1,36 г – х % х = 3,40 % |
Соответствует требованиям нормативной документации
|
5. Идентификация действующих веществ: регламентирована ФС «Диоксометилтетрагидропиримидин (метилурацил)», ФС «Хлорамфеникол (левомицетин)» и частной нормативной документацией ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''» 42-0017-6136-05. Проводят качественные химические реакции (таблица 2.7) [3].
Таблица 2.7
Идентификация действующих веществ мази «Левомеколь»
|
№ п/п |
Химико-фармацевти-ческая компания |
Требования нормативной документации
|
Вывод о соответствии/несоответствии |
|
1 |
ОАО «Нижфарм»
|
Качественная реакция. 1 г препарата растворяют при нагревании на водяной бане в 3 мл воды дистиллированной и прибавляют 1 мл бромной воды; раствор обесцвечивается.
Качественная реакция. 3 г препарата помещают в коническую колбу вместимостью 50 мл, прибавляют 5 мл раствора едкого натра и нагревают на водяной бане. Появляется желтое окрашивание, переходящее в оранжевое. При кипячении пробы окраска становится красно-оранжевой и выделяется аммиак, обнаруживаемый по посинению влажной красной лакмусовой бумаги. После охлаждения пробу нейтрализуют азотной кислотой по универсальной индикаторной бумаге и фильтруют. Фильтрат дает характерную реакцию на хлориды. К 2 мл раствора прибавляют 0,5 мл разведенной азотной кислоты и 0,5 мл раствора нитрата серебра. Образуется белый творожистый осадок, нерастворимый в разведенной азотной кислоте и нерастворимый в растворе аммиака. |
Соответствует требованиям нормативной документации |
|
2 |
ОАО «ХФК ''Акрихин''» |
Соответствует требованиям нормативной документации |
6. Испытание на чистоту: регламентировано ОФС.1.4.1.0008.15 «Мази» и частной нормативной документацией ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''» 42-0017-6136-05. 3 г препарата помещают в коническую колбу вместимостью 50 мл, прибавляют 30 мл воды, нагревают на водяной бане до расплавления основы, перемешивают в течение 3 минут, охлаждают и фильтруют, определяют рН (таблица 2.8) [3].
Таблица 2.8
Испытание на чистоту мази «Левомеколь»
|
№ п/п |
Химико-фармацевти-ческая компания |
рН раствора
|
Требования нормативной документации |
Вывод о соответствии/ несоответствии |
|
1 |
ОАО «Нижфарм»
|
6,3
|
рН: от 5,0 до 7,5 |
Соответствует требованиям нормативной документации
|
|
2 |
ОАО «ХФК ''Акрихин''»
|
7,1 |
Соответствует требованиям нормативной документации
|
Вывод: результаты оценки качества мази «Левомеколь» двух образцов в тубе алюминиевой 40 г промышленного производства ОАО «Нижфарм» (Россия) и ОАО «Химико-фармацевтический комбинат «Акрихин» (Россия) свидетельствуют о соответствии анализируемых лекарственных препаратов требованиям действующей нормативной документации РФ по производству и контролю качества лекарств.
ВЫВОДЫ ПО ПРАКТИЧЕСКОЙ ЧАСТИ
1. В практической части работы описана история создания мази «Левомеколь», разработанной в Харьковском фармацевтическом институте в середине 1970-х годов. Серийное производство началось в 1985 году. Выявлено, что в настоящее время мазь «Левомеколь» производится двумя фирмами в России – ОАО «Нижфарм» и ОАО «Химико-фармацевтический комбинат ''Акрихин''» и стала одной их самых востребованных благодаря оценке по критерию эффект/цена.
2. Установлены показатели стандартизации мази «Левомеколь», исходя из состава и физико-химических свойств лекарственного препарата. Отмечено, что она проводится согласно ОФС ГФ XIII, о также ФС «Диоксометилтетрагидропиримидин (метилурацил)», «Хлорамфеникол (левомицетин)» и частной нормативной документации (ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''» 42-0017-6136-05) и предусматривает:
- оценку упаковки и маркировки мази;
- определение и оценку внешнего вида мази;
- определение и оценку однородности мази;
- определение и оценку общей массы мази;
- идентификацию лекарственных веществ в составе мази;
- испытание на чистоту (определение рН водной вытяжки).
3. Проведена оценка качества двух образцов мази «Левомеколь» в тубе алюминиевой 40 г производства ОАО «Нижфарм» и ОАО «Химико-фармацевтический комбинат ''Акрихин''» на базе лаборатории контроля качества лекарственных средств ОГБПОУ «Рославльский медицинский техникум» с учетом имеющегося оборудования и реактивов по приведенным показателям. В работе применены органолептические, физические и химические методы оценки качества. Результаты оценки качества свидетельствуют о соответствии анализируемых лекарственных препаратов требованиям действующей нормативной документации РФ по производству и контролю качества лекарств.
ЗАКЛЮЧЕНИЕ
Мазь «Левомеколь», любимый помощник врача, давно зарекомендовала себя как эффективное антибактериальное средство, ускоряющее заживление ран и способствующее восстановлению нормальных структур поврежденной кожи. Являясь одновременно антибиотиком и репарантом, мазь стала одной из самых популярных у населения в лечении гнойников, ран разной сложности и при восстановлении целостности кожного покрова после наложения швов.
В теоретической части работы была дана общая характеристика мазей как лекарственных форм, рассмотрены особенности технологии изготовления мазей, определены требования нормативной документации, регламентирующей контроль и оценку их качества. Выяснив, что мази представляют собой сравнительно нестойкую недозированную лекарственную форму мягкой консистенции, состоящую из лекарственных веществ и мазевой основы, в работе особенно подчеркнуто что, это обязывает к строгому подходу в обеспечении качества мазей и их оценке качества.
Оценка качества лекарственной формы включает в себя как анализ лекарственных веществ, входящих в ее состав, так и показатели качества, характеризующие саму лекарственную форму с учетом современных требований. В работе установлено, что к наиболее значимым показателям оценки качества мазей заводского изготовления относятся внешний вид, запах и характерные органолептические свойства, физико-химические свойства лекарственных и вспомогательных веществ и их концентрация, дисперсность, степень чистоты, отклонения в массе, характер упаковки и маркировки. Перечисленные показатели оценки качества регламентированы Государственными стандартами качества РФ (ГФ, ОФС и ФС) и промышленными регламентами (ФСП, спецификациями производства, техническими условиями и др.).
Основным Государственным стандартом, на основе которого выстраивается оценка качества мазей, является ОФС.1.4.1.0008.15 «Мази». Частные ФС описывают оценку качества мазей по идентификации действующих веществ, входящих в состав лекарственного препарата, и их количественному определению.
В практической части работы была описана история создания мази «Левомеколь», разработанной в Харьковском фармацевтическом институте в середине 1970-х годов. Серийное производство началось в 1985 году.
По данным Государственного реестра лекарственных средств, в России зарегистрировано 9 форм выпуска мази «Левомеколь». Выявлено, что в настоящее время она производится двумя фирмами – ОАО «Нижфарм» и ОАО «Химико-фармацевтический комбинат ''Акрихин''» и стала одной их самых востребованных благодаря оценке по критерию эффект/цена. По данным Российского Инфо-портала о лекарствах Farmanews.ru, мазь «Левомеколь» входит в десятку самых востребованных лекарств в России. Цена препарата и эффекты лечения, судя по отзывам, устраивают большинство пациентов.
Также в практической части работы были установлены показатели стандартизации мази «Левомеколь», исходя из состава и физико-химических свойств лекарственного препарата, проведена ее оценка качества по следующим показателям, регламентированным Государственной и частной нормативной документацией:
- оценка упаковки и маркировки мази;
- определение и оценка внешнего вида мази;
- определение и оценка однородности мази;
- определение и оценка общей массы мази;
- идентификация лекарственных веществ в составе мази;
- испытание на чистоту (определение рН водной вытяжки).
Оценка качества мази «Левомеколь» проведена для двух образцов мази в тубе алюминиевой 40 г производства ОАО «Нижфарм» и ОАО «Химико-фармацевтический комбинат ''Акрихин''» на базе лаборатории контроля качества лекарственных средств ОГБПОУ «Рославльский медицинский техникум» с учетом имеющегося оборудования и реактивов по приведенным показателям. В работе применены органолептические, физические и химические методы оценки качества. Результаты оценки качества свидетельствуют о соответствии анализируемых образцов лекарственных препаратов требованиям действующей нормативной документации РФ по производству и контролю качества лекарств.
Таким образом, цель настоящего исследования достигнута, поставленные задачи успешно решены. Проведенное исследование показало, что оценка качества мазей является многоаспектной проблемой, она требует высокой квалификации ученых, практических работников органов государственной власти и организаций здравоохранения, а также всех работников фармацевтической отрасли.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Федеральный закон от 12.04.2010 г. № 61-ФЗ «Об обращении лекарственных средств». [Электронный ресурс]: Справочно-правовая система «Консультант Плюс». Режим доступа: http://www.consultant.ru.
2. Приказ Министерства здравоохранения Российской Федерации от 26.10.2015 г. № 751н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность». [Электронный ресурс]: Справочно-правовая система «Консультант Плюс». Режим доступа: http://www.consultant.ru.
3. Государственная фармакопея РФ. XIII издание. [Электронный ресурс]: ФГБУ «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения РФ. Режим доступа: http://www.regmed.ru.
4. Государственный реестр лекарственных средств. [Электронный ресурс]: Официальный сайт Министерства здравоохранения РФ. Режим доступа: http://www.grls.rosminzdrav.ru.
5. ОФС.1.4.1.0001.15 «Лекарственные формы». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
6. ОФС.1.4.1.0008.15 «Мази». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
7. ОФС.1.2.4.0002.15 «Микробиологическая чистота». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
8. ОФС.1.1.0009.15 «Сроки годности лекарственных средств». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
9. ОФС.1.2.4.0003.15 «Стерильность». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
10. ОФС.1.1.0010.15 «Хранение лекарственных средств». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
11. ФС «Диоксометилтетрагидропиримидин (метилурацил)». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
12. ФС «Хлорамфеникол (левомицетин)». [Электронный ресурс]: Фармакопея.рф. Режим доступа: http://pharmacopoeia.ru.
13. ФСП ОАО «Химико-фармацевтический комбинат ''Акрихин''» 42-0017-6136-05. [Электронный ресурс]: Официальный сайт ОАО «Химико-фармацевтический комбинат ''Акрихин''». Режим доступа: http://www.akrikhin.ru.
14. Арзамасцев А.П. Анализ лекарственных смесей: учеб. пособие для студ. фарм. ин-тов и фарм. фак. мед. вузов / А.П. Арзамасцев и др. – М. : Компания Спутник, 2000.
15. Арзамасцев А.П. Фармакопейный анализ: учеб. пособие для студ. фарм. ин-тов и фарм. фак. мед. вузов – М.: Медицина, 2001.
16. Глущенко Н.Н. Фармацевтическая химия: учебник для студ. сред. проф. учеб. заведений / Н.Н. Глущенко, Т.В. Плетенева, В.А. Попков. Под ред. Т.В. Плетеневой. – М.: Издательский центр «Академия», 2004.
17. Ермилова Е.В. Анализ лекарственных средств: учебное пособие / Е.В. Ермилова, Т.В. Кадырова, В.В. Дудко. Под ред. Е.В. Ермиловой. – Томск: СибГМУ, 2010.
18. Кулешова М.И. Анализ лекарственных форм, изготовляемых в аптеках: пособие для фармацевтов и провизоров / М.И. Кулешова, Л.Н. Гусева, О.К. Сивицкая. 2-е изд., перераб. и доп. – М.: Медицина, 1989.
19. Сенов П.Л. Фармацевтическая химия. Изд. 8-е, испр. – М.: Медицина, 1978 г.
20. Сливкин А.И. Функциональный анализ органических лекарственных веществ / А.И. Сливкин, В.П. Садчикова. – Воронеж: ВГУ, 2007.
21. Тыжигирова В.В. Показатели качества и особенности анализа мазей и суппозиториев: учеб. пособие. – Иркутск: ГБОУ ВПО ИГМУ Минздравсоцразвития России, 2012.
22. Анализ лекарственных средств – производных пиримидина. [Электронный ресурс]: Студопедия. Режим доступа: http://studopedia.ru.
23. Качество лекарственных препаратов. Суть вопроса и зарубежный опыт. [Электронный ресурс]: Новости медицины портала Remedium.ru. Режим доступа: http://www.remedium.ru.
24. Левомеколь. [Электронный ресурс]: MEDSIDE.RU. Лекарства. Антибиотики. Антибиотики. Режим доступа: http://medside.ru.
25. Левомеколь – инструкция по применению, отзывы, аналоги, цена. [Электронный ресурс]: Тiensmed.ru. Режим доступа: http://www.tiensmed.ru.
26. Левомеколь. [Электронный ресурс]: Реестр лекарственных средств. Режим доступа: http://www.reles.ru.
27. Левомицетин. [Электронный ресурс]: Студопедия. Режим доступа: http://studopedia.ru.
28. Левомицетин: получение, качественные и количественные реакции. [Электронный ресурс]: Кazedu.kz/news. Режим доступа: https://www.kazedu.kz/news.
29. Нитрофенилалкиламины. [Электронный ресурс]: Сборник лекций для фармацевтов и провизоров. Режим доступа: http://farmf.ru.
30. ОАО «ХФК ''Акрихин''». [Электронный ресурс]: Официальный сайт ОАО «Химико-фармацевтический комбинат ''Акрихин''». Режим доступа: http://www.akrikhin.ru.
31. Продукция ОАО «Нижфарм». [Электронный ресурс]: Официальный сайт ОАО «Нижфарм». Режим доступа: http://www.fptl.ru.
32. Регламент производства лекарственного средства технологический. [Электронный ресурс]: Словарь финансовых и юридических терминов. Режим доступа: http:/consultant.ru.
33. Спектрофотометрическое определение комбинированного препарата «Левомеколь» мазь. [Электронный ресурс]: Электронный научный журнал «Международный студенческий научный вестник». Режим доступа: https://eduherald.ru.
34. Технический регламент. [Электронный ресурс]: Студопедия. Режим доступа: http://studopedia.ru.
35. Фармакопейная статья предприятия. [Электронный ресурс]: Информационный сайт для провизоров. Режим доступа: http://www.consultpharma.ru.
36. Фармакопейный анализ органических лекарственных веществ. Методические рекомендации к лабораторно-практическим занятиям. – Нижний Новгород: изд-во Нижегородской государственной медицинской академии, 2009. [Электронный ресурс]: Сайт Нижегородской государственной медицинской академии. Режим доступа: http://www.mma.ru.
37. Хлорамфеникол. [Электронный ресурс]: Википедия. Режим доступа: https://ru.wikipedia.org.
38. Что такое Фармакопейная статья? [Электронный ресурс]: Удивительный мир фармации. Режим доступа: http://flogia.ru.
39. Farmanews.ru. Российский Инфо-портал о лекарствах. [Электронный ресурс]: Farmanews.ru. Режим доступа: http://farmanews.ru.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.