
Федеральное агентство по образованию
Государственное учреждение высшего профессионального образования
«Бирская государственная социально – педагогическая академия»
Факультет биологии и химии
Кафедра химии и МОХ
Лыгин Сергей Александрович
Кашкина Татьяна Александровна
Учебно-методическое пособие
Химический состав комбикормов.
Влияние компонентов на живой организм
Бирск - 2010
Оглавление
Введение…………………………………………………………………….……..3
Глава I. Комбикорма и их состав……………………………… ………………8
1.1. Контроль токсичности кормов…………………………………… ……43
Глава II Методы качественного и количественного анализов комбикормов 46
2.1.Методы определения кальция………………………………………………46
2.2. Методы определения содержания натрия и хлорида натрия…………….58
2.3.Методы определения содержания фосфора………………………………..63
Глава III. Результаты проведенных исследований………… 72
Заключение……………………………………………………………………….73
Литература……………………………………………………………………….74
Введение
Химические элементы – это неотъемлемая часть нашей жизни. Их наличие в организме в строго определенных количествах - непременное условие для сохранения здоровья. В зависимости от потребности организма они подразделяются на микро- и макроэлементы. Макроэлементы - вещества, содержащиеся в организме в большом количестве (их концентрация превышает 0,001%). Это углерод, водород, кальций, фосфор, сера, азот, магний, натрий, хлор и др. Микроэлементы - вещества, доля которых в организме невелика (от 0,001 до 0,000000000001%). Это цинк, медь, марганец, молибден, бор, кобальт, йод, фтор и др. Они называются также "следовыми" элементами.
В России эта потребность даже у людей удовлетворяется лишь на 10-18%. Значит, мы и живем, используя только 10-18% своего потенциала. Полноценному питанию человека в нашем государстве уделяется значительное внимание. Так, Постановлением Правительства Российской Федерации от 10 августа 1998 года № 917 была принята Концепция государственной политики в области здорового питания населения Российской Федерации. [2].
На первом этапе реализации Концепции совершенствуется нормативная база в сфере производства и реализации пищевых продуктов, определяется уровень дефицита пищевых веществ, создаются методические рекомендации по разработке региональных программ здорового питания. В качестве неотложных мер по реализации Концепции осуществляется улучшение структуры питания за счет увеличения доли продуктов массового потребления с высокой пищевой и биологической ценностью, в том числе на 20-30 процентов продуктов, обогащенных витаминами и минеральными веществами, на 30-40 процентов свежих овощей и фруктов.
Одновременно реализуются мероприятия по приведению в соответствие показателей качества и безопасности продовольствия с учетом рекомендаций международных организаций (Всемирная торговая организация, Всемирная организация здравоохранения и Всемирная продовольственная организация).
На втором этапе будет увеличено производство витаминов и других микроэлементов, и разработана система экономического стимулирования отечественного производства продовольственного сырья пищевой продукции, витаминов и других микронутриентов.
На третьем этапе предусматривается совершенствование системы государственного контроля качества сельскохозяйственного сырья и пищевых продуктов на всех стадиях производства, формирование системы адресной помощи малоимущим слоям населения, преодоление негативных тенденций в состоянии здоровья нации, улучшение структуры потребления пищевых продуктов, в том числе обогащенных витаминами, микроэлементами, биологически активными добавками, стабилизация и снижение частоты заболеваний, обусловленных недостаточным потреблением пищевых веществ, улучшение антропометрических показателей детей и подростков, снижение распространенности анемии среди детей раннего возраста, женщин детородного возраста и беременных, преодоление последствий дефицита фтора и йода.
Вместе с тем известно, что минеральные вещества наряду с белками, жирами, углеводами и витаминами являются жизненно важными компонентами пищи человека, необходимыми для построения химических структур живых тканей и осуществления важнейших биохимических и физиологических процессов, лежащих в основе жизнедеятельности организма. Минеральные элементы относятся к незаменимым веществам организма. Они входят в состав всех клеток органов и тканей, вместе с водой участвуют в поддержании осмотического давления и обеспечивают постоянство рН внутри- и внеклеточной жидкости, процессы мышечного сокращения, нервной проводимости, являются структурными компонентами многих ферментов и витаминов, включаются в разнообразные реакции обмена веществ.[6] Для клинической практики и профилактической медицины достаточно удобной является классификация микроэлементов в зависимости от воздействия на организм:
1. Эссенциальные – микроэлементы, необходимые для нормальной жизнедеятельности и являющиеся незаменимыми компонентами пищевых рационов (медь, цинк, марганец, кобальт, молибден, хром, никель, ванадий, йод, фтор, селен, кремний).
2. Токсичные микроэлементы - при их поступлении в организм могут возникать тяжелые токсические реакции. К токсичным элементам отнесены алюминий, кадмий, свинец, ртуть, бериллий, барий, таллий, висмут, сурьма.
3. Нейтральные микроэлементы (инертные) не оказывают выраженных токсических или физиологических воздействий на организм. В литературе встречается и другое название указанной группы - «потенциально-токсичные» микроэлементы. К данной группе относят рубидий, цирконий, олово, серебро, золото, титан, стронций, германий, галлий и другие.
Потребность домашней птицы в микроэлементах в количественном отношении намного (в 400-500 раз) меньше, чем в макроэлементах, но это именно тот случай, когда "мал золотник, да дорог". Так, фтор необходим для здоровья костной и особенно зубной ткани; цинк, кобальт и медь - кроветворные элементы, а соединения марганца ответственны за рост, размножение и уровень холестерина в крови, недостаток этого элемента ведет к возникновению нервных расстройств. Доказано, что живой организм массой 70 кг состоит из следующих составляющих:
45 кг кислорода; 12 кг углерода; 7 кг водорода; 2 кг азота; 1,2 кг кальция;
800 г фосфора; 300 г серы; 210 г калия; 100 г натрия; 70 г хлора.
Плюс целый набор микроэлементов. Все макро- и микроэлементы в различной степени и в разные периоды жизненного цикла оказывают на него большое влияние, так как они вступают в соединение с opганическими веществами, синтезируемыми нашими клетками. Они влияют на развитие организма, на оплодотворения, дыхание, иммунную систему, словом, на деятельность всех физиологических систем организма.
Актуальность выбранной темы очевидна. Питание домашних животных на сегодняшний день состоит из соевой пищи, генетически модифицированных продуктов, биологических добавок. Дисбаланс минеральных веществ в организме приводит к таким заболеваниям как сахарный диабет, остеохондроз, подагра, гипертония, атеросклероз, катаракта, глухота, рахит, язва желудка и двенадцатиперстной кишки и др. [12]. В основе рациона домашних животных находятся искусственные корма. Как же удается достичь тонкой грани в определении баланса тех или иных компонентов? Как компоненты комбикормов влияют на животных? Как организуется питание животных для сохранения баланса в организме?
Цель работы: раскрыть основные принципы и стороны искусственного питания в птицеводстве, разработать основные методы качественного и количественного анализа комбикормов.
Следовательно, объектом исследования данной работы являются искусственные корма (комбикорма), предметом исследования – состав комбикорма, влияние его компонентов на живой организм на примере кур породы Бройлер кросс Смена.
Задача работы: установить состав искусственных кормов, влияние компонентов питания на живой организм, организацию питания в искусственных условиях.
Гипотеза исследования: при сбалансированном, соответствующем физиологическим потребностям организма питании вызываются привесы в сельском хозяйстве.
База исследования: ОАО «Турбаслинские бройлеры» г. Благовещенск.
Методологической основой исследования является анализ и синтез полученных данных, комплексонометрический метод, пламенно-фотометричес-кий метод, титриметрический метод и др.
Все исследования мы проводим на курах породы Бройлер кросс Смена. Бройлер – гибридный мясной цыпленок не старше 10 недель (независимо от пола), специализированного выращивания, отличающийся интенсивным ростом, высокой мясной скороспелостью, высокой конверсией корма, хорошими мясными качествами, нежным мясом, мягкой и гладкой кожей, мягкими хрящами грудной кости.
Одним из основных технологических принципов, на которых базируется современное птицеводство является применение полнорационных сухих кормов, отвечающих биологическим потребностям птицы и позволяющим получать высококачественную продукцию при низких затратах корма на 1 кг прироста. На изучение состава комбикормов направлены исследования в данной работе.
Глава I Комбикорма и их состав
Комбикормами называют однородную смесь измельченных кормовых средств (в основном концентрированных кормов), составленную по научно обоснованным рецептам и предназначенную для определенного вида животных и сельскохозяйственной птицы. Изготавливают комбикорма на государственных комбикормовых заводах и в цехах. Комбикорма должны обеспечить эффективное использование питательных веществ и высокую продуктивность птицы при наименьшем расходе комбикорма на единицу продукции. Производство комбикормов базируется на научно обоснованных нормах кормления разных видов и возрастных групп птицы, оптимальной структуре комбикормов и допустимых нормах ввода отдельных компонентов. Основные параметры производства регламентируются требованиями ГОСТа на комбикормовое сырье и комбикорма. Готовый комбикорм представляет собой смесь очищенных и измельченных до необходимой величины различных кормовых средств и микродобавок, изготовленную по научно обоснованной рецептуре и обеспечивающую полноценное кормление птицы. Комбикорм должен быть однородным по внешнему виду, без признаков плесени.

Рис.1. Комбикорма.
В зависимости от назначения комбикорма производят мелкого, среднего и крупного размола (рис.1). Степень размола определяют остатками на сите: мелкий размол—остаток на сите с отверстиями 5 мм не допускается; средний размол — остаток на сите с отверстиями 3 мм не более 12 %, с отверстиями 5 мм не допускается; крупный размол—остаток на сите с отверстиями диаметром 3 мм не более 35 %, остаток на сите с отверстиями 5 мм не более 5 %. В Российской Федерации в составе комбикормов животных и птицы зерно злаковых культур составляет 60-75%, в основном это пшеница, ячмень, кукуруза.
Для птицы изготовляют полнорационные комбикорма в рассыпном и гранулированном виде, комбикорма-концентраты и комбикормовую крупку. Полнорационные комбикорма (ПК) обеспечивают потребность птицы в энергии, питательных, минеральных и биологически активных веществах без дополнительного скармливания других кормов и микродобавок. Гранулированный комбикорм имеет ряд преимуществ перед рассыпным, так как исключается расслоение компонентов во время транспортировки и раздачи, птица не имеет возможности выбора отдельных частиц комбикорма, что исключает нарушение сбалансированности кормления и уменьшает потери за счет россыпи и пыли. В гранулах лучше сохраняются биологически активные вещества, особенно каротин, витамины; в процессе гранулирования за счет давления и температуры повышается доступность питательных веществ и разрушаются антипитательные факторы. Переваримость органических веществ гранулированного комбикорма повышается на 2,2-3 %. Комбикорма-концентраты выпускают с повышенным содержанием сырого протеина, минеральных веществ и микродобавок. Комбикорма-концентраты применяют в качестве добавки к основному рациону для повышения полноценности кормления птицы (30-50 %). Минеральные вещества комбикорма представляют собой остаток, полученный при озолении сухой массы корма. Зола состоит из макроэлементов (кальций, фосфор, магний, калий, натрий, хлор, сера) и микроэлементов (железо, марганец, цинк, медь, кобальт, йод, селен и др.). Физиологическая роль минеральных веществ в организме птицы разнообразна. К основным нормируемым в комбикормах для птицы макроэлементам относятся кальций, фосфор и натрий, а к микроэлементам - железо, медь, цинк, кобальт, марганец и йод. [24]
1.1. Влияние макро- и микроэлементов на рост, развитие и
жизненную способность живого организма
Кальций не только структурный компонент костной, ткани. Ионы кальция играют ключевую роль в мышечном сокращении, увеличивают проницаемость мембраны клеток для ионов калия, влияют на натриевую проводимость клеток, на работу ионных насосов, способствуют секреции гормонов, участвуют в каскадном механизме свёртывания крови, необходим для образования костной ткани и формирования скорлупы яиц. Основным депо кальция в организме (99% кальция от общей массы) являются кости. В костях около 99% кальция присутствует в малорастворимой форме кристаллов гидроксиапатита [Ca10(PO4)6(OH)2H2O]. В виде фосфатных солей в костях находится лишь 1 % кальция, который может обмениваться и играть роль буфера при изменении концентрации кальция в плазме крови. Другой фонд кальция (1% от общей массы кальция) – кальций плазмы крови. В плазму кальций поступает из кишечника (с водой и пищей) и из костной ткани (в процессе резорбции). Ионы кальция необходимы для нормальной деятельности сердца, участвуют в регуляции мышечной и нервной деятельности, повышают защитные функции организма, регулируют репродуктивные функции самцов и самок. Кроме того, они служат важнейшими посредниками во внутриклеточной передаче сигналов.
Кальций - это внеклеточный катион: в плазме крови его содержание составляет 2,12-2,6 ммоль/л. Кальций плазмы крови представлен в виде:
- несвязанного, ионизированного кальция (около 50%);
2. ионов кальция, соединённых с белками, главным образом, с альбумином (45%);
3. недиссоциирующих комлексов с цитратом, фосфатом, сульфатом и карбонатом (5%).
Биологически активной фракцией является ионизированный кальций, концентрация которого поддерживается в пределах 1,1 - 1,3 ммоль/л. Концентрация ионов кальция в плазме крови регулируется с высокой точностью: изменение её всего на 1% приводит в действие гомеостатические механизмы, восстанавливающие равновесие.
Основная часть кальция выводится из организма с калом (500-800 мг/сут) и мочой (100-300 мг/сут). Усвоение и обмен кальция тесно связаны с обеспеченностью фосфором, магнием, калием, железом и витамином Д3, аминокислотной сбалансированностью, то есть, с факторами, обеспечивающими достаточный синтез кальцийсвязующего белка. Усвоение кальция в верхнем отделе тонкого кишечника происходит двумя путями - в результате активного переноса кальция через стенку кишечной при помощи специфического кальцийсвязующего белка. Оба процесса активизируются витамином Д3.
Роль кальция в организме очень велика: он обеспечивает двигательную активность клеток (в том числе мышечные сокращения), возбудимость, пиноцитоз, внутриклеточный метаболизм.
Кальцитриол обладает кальцийсберегающим действием за счет трех основных процессов: усиления всасывания кальция в кишечнике, увеличения реабсорбции (обратного всасывания) кальция в почках и мобилизации кальция из костей. Все эффекты кальцитриола обусловлены его гормональной природой: кальцитриол связывается со своим рецептором, образуется комплекс рецептор — гормон, который проникает в ядро и связывается с соответствующими генами, репрессируя или активируя их. Если он связывается с геном синтеза кальцийсвязывающего белка, то активирует его и таким образам усиливается синтез этого белка в щеточной кайме эпителия кишечника и канальцах почек. В результате в организм поступает больше кальция. Если он связывается с геном синтеза коллагена костей, то репрессирует его, обеспечивая вымывание кальция из костей. Возможен другой механизм воздействия кальцитриола — увеличение содержания кальция в клетке за счет действия на структурно-функциональные характеристики фосфолипидов клеточной стенки или непосредственно на пропускную способность кальциевых каналов. Кальцитриол регулирует также синтез некоторых других белков, влияющих на метаболизм кальция,— тропонина С (мышцы), кальбиндина (эпителий желудочно-кишечного тракта), остеокальцин (кости), кальмодулин (все клетки организма). Главная физиологически активная форма кальция - ионизированная, которая абсорбируется в кишечнике.
Низкая концентрация кальция в крови вызывает синтез и секрецию паратгормона - гормона щитовидной железы (менее 1 ммоль/л). Паратгормон в костях активирует остеокласты, что приводит к выходу ионов кальция и фосфатов во внеклеточную жидкость; тормозит остеоциты. В почках увеличивает реабсорбцию ионов кальция и снижает реабсорбцию фосфатов. Индуцирует синтез кальцитриола, который усиливает всасывание кальция в кишечнике. Суммарное действие – повышение концентрации кальция во внеклеточной жидкости при постоянной или пониженной концентрации фосфатов.
Избыток кальция в рационе также нежелателен, ибо при этом ухудшая поедаемость корма, нарушается обмен фосфора, магния и микроэлементов (марганец, цинк, железо, йод). Высокие дозы кальция в ростовых рационах, являются нефрогенными факторами, способными спровоцировать развитие подагры. Усвоение кальция зависит от его источника, уровня в рационе и возраста птицы. Чем выше уровень кальция, тем меньше его усвояемость. В период пика использование кальция составляет около 70%. С возрастом использование кальция снижается до 30 %, поэтому после 42-недельного возраста кур уровень кальция в рационе рекомендуется повышать. Лучшим источником кальция для птицы служит ракушка; мел и известняк менее эффективны. Основные компоненты комбикормов (зерновые культуры, шроты, продукты микробного синтеза, травяная мука и небольшое количество кормов животного происхождения) не удовлетворяют потребность птицы в кальции, фосфоре и натрии, поэтому в комбикорма вводят добавки, являющиеся источниками этих элементов. Основную часть этих элементов вносят в комбикорма в виде минеральных компонентов. В качестве источника кальция используют ракушку, известняк, мел. Добавки мела не должны превышать 3 %, так как в большом количестве он ухудшает вкусовые качества и физическую структуру комбикорма, снижая его поедаемость. Кроме того, мел является наименее технологическим сырьем для кормового производства, поскольку при измельчении и просеивании налипает на рабочие поверхности оборудования. В высушенном виде мел пылеообразен, в комбикормах он отсеивается в отдельную фракцию и в виде остатков выбрасывается. Ракушка часто загрязнена песком и содержит много цельных раковин, этому вводить в комбикорм рекомендуется предварительно промытую ракушечную крупку. Известняки равноценны ракушке по химическим свойствам и биологической доступности кальция.
Таблица 1
Элементы |
Количество |
|
Кальций |
28—34% |
|
Магний |
не более 1,5% |
|
Фтор |
не более 0,2% |
|
Мышьяк |
не более 0,015% |
|
Свинец |
не более 0,008% |
|
Нерастворимый остаток (песок) |
до 5 % |
В хозяйствах целесообразно использовать известняки местных месторождений, предварительно проверенные на вышеперечисленные показатели. Фосфаты кальция, в частности ортофосфат, составляют минеральную основу костей и зубов. Другие соединения кальция участвуют в нервной и мышечной деятельности, входят в состав тканевой жидкости, ядер и стенок клеточной ткани живого организма. Кальций уменьшает аллергические реакции, а это особенно важно в наше время [16].
.
Фосфор содержится во всех тканях организма и является непременным компонентом его внутренней среды. Основная часть фосфора в виде фосфорнокислого кальция находится в костяке. Фосфорная кислота входит в состав многих коэнзимов. Макроэргические соединения (АТФ, АДФ и др.) являются универсальными аккумуляторами энергии, исключительную роль играет АТФ в мышечной деятельности. Кроме того, фосфор входит в состав фосфолипидов, фосфолипо- и фосфогликопротеинов. Дефицит фосфора в рационах приводит к нарушению обмена кальция и развитию рахита у молодняка, а у взрослой особи вызывает остеопороз. Избыток фосфора свыше 0,8 % в рационах молодняка, как и недостаток его, может быть причиной рахита. У взрослой особи избыток фосфора снижает усвоение кальция из корма, резорбцию кальция из костей или же ингибирует образование карбоната кальция в скорлуповой железе, отрицательно влияя на качество скорлупы. Кроме того, ухудшается использование цинка, марганца, магния. У птицы при избытке фосфора нарушается подвижность суставов. При нормировании фосфора следует иметь ввиду, что из общего фосфора растений 60-80 % связано с фитином и практически птицей не используется. Неорганический фосфор и фосфор кормов животного происхождения используется птицей хорошо. Считается, что молодняк старших возрастов и взрослая птица усваивает фитиновый фосфор на 30-5 %. Молодняк в первые 2-3 недели жизни соединения фитиновой кислоты практически не усваивает. Применяемые в птицеводстве источники фосфора по уровню его доступности (в %) располагаются в следующем порядке:
монокальцийфосфат, рыбная мука, костная мука - 100-96 %,
мясо-костная мука и кормовые дрожжи, трикальцийфосфат -90-86%,
жмыхи, шроты и травяная мука - 50 %,
зерновые корма — 30 %.
Таблица 2
|
монокальций и дикальций фосфаты |
100 % |
|
рыбная мука |
98 % |
|
костная мука |
96 % |
|
мясо-костная мука |
90 % |
|
трикальцийфосфат |
86% |
|
жмыхи, шроты, травяная мука и зерновые корма |
30 %. |
Фосфор также относится к макроэлементам, необходимым организму. Помимо зубной, костной и нервной тканей, фосфорные соединения входят в состав жиров (фосфолипидов), многих белков, биологически активных веществ, таких как ферменты. Фосфор поступает в организм обычно с белковой пищей. Ученые-медики считают, что следует строго выдерживать соотношение кальция и фосфора, поступающих с пищей; оптимальным признано соотношение этих элементов, равное 1:1 по массе (или, в крайнем случае, 1:1,5). При избытке фосфора возможна даже потеря кальция костной тканью (остеопороз), что ведет к уменьшению их прочности и частым переломам. Фосфор, минеральный элемент питания, соединения которого активно участвуют во многих обменных процессах.
Недостаток фосфора в организме чаще всего связан с несбалансированностью питания. В частности, этому способствует избыток кальция при дефиците белков и витамина D. Проявляется это потерей аппетита, апатией, снижением умственной и физической работоспособности, похуданием. Излишнее поступление фосфора в организм вероятно при длительном преобладании в питании мясных, рыбных и зерновых продуктов. Избыток фосфора нарушает всасывание кальция из кишечника, тормозит образование активной формы витамина D, связывает часть кальция в крови, что ведет к его выведению из костей и отложению солей кальция в почках и кровеносных сосудах.
Натрий является основным катионом внеклеточной среды. Содержание его в плазме крови составляет 135-150 ммоль/л, в эритроцитах – 8-13 ммоль/л. В течение суток с пищей поступает 3-4 г натрия, практически такое же количество выводится с почками. Реабсорбция натрия в почечных канальцах – активный процесс, требующий затраты АТФ и сопровождающийся секрецией калия и протонов в мочу. Натрий создает электрохимический потенциал на мембранах клетки; поддерживает осмотическое давление, регулирует кислотно-основное равновесие (при реабсорбции натрия в мочу секретируются протоны, т.е. удаляются кислые продукты метаболизма). Он необходим для построения тканей, поддержания осмотического давления и для регуляции водного, минерального, азотистого и жирового обменов. Натрий не выполняет в организме какой-либо специфической функции, но он необходим для нормальной жизнедеятельности тканей. При недостатке натрия нарушается обмен кальция и фосфора, а это может привести к размягчению костей, снижению продуктивности и качества скорлупы. В связи с уменьшением секреции желудочного сока при недостатке натрия снижается использование питательных веществ корма, что приводит к каннибализму. Дозы натрия, превышающие потребность, приводят к избыточному потреблению воды и к сопутствующим проблемам, связанным с удалением жидкого помета. Натрий, один из наиболее важных минеральных элементов питания. Его биологическая активность и роль в процессах жизнедеятельности организма человека исключительно велика. Больше всего натрия содержится во внеклеточных жидкостях (лимфе и сыворотке крови), так же он присутствует практически во всех органах и тканях. Натрий активно участвует в процессах внутриклеточного обмена, поддержании кислотно-щелочного равновесия. В организм он поступает в основном в виде поваренной соли— хлорида натрия.
Железо необходимо для образования гемоглобина, участвует в окислительно-восстановительных реакциях, входя в состав цитохромов, каталаз, оксидаз. Обмен и усвоение железа связаны с содержанием в рационе витаминов Вс, В12, B6 С, фитатов, кальция, меди и зависят от интенсивности образования железосвязывающего белка. Для кроветворения и тканевого дыхания необходимо железо, входящее в состав гемоглобина крови и миоглобина мышц. Этот элемент переносит кислород в организме. Функцию переноса кислорода вдыхаемого воздуха (в составе гемоглобина) осуществляет примерно 60% этого количества железа.
Организм очень экономно использует этот микроэлемент в процессе кроветворения: железо, которое высвобождается при разрушении отработавших свой срок эритроцитов, повторно используется на те же цели. Кроме того, около 20% железа организма депонируется на случай повышенной в нем потребности. Вместе с тем при столь, казалось бы, надежной, предусмотренной самой природой системе предупреждения недостаточности железа, железодефицитные анемии не редкость. Причиной тому— преобладание в питании растительной пищи с незначительным содержанием железа, которое в ряде мест осложняется пониженным его содержанием в почвах и распространенностью желудочно-кишечных заболеваний, препятствующих усвоению железа из пищи.
Медь катализирует включение железа в структуру гема, регулятор созревания эритроцитов, компонент многих оксидаз, нормализует обмен кальция и фосфора, синтез некоторых гормонов. Медь необходима для нормальной кератинизации пера и нормализации эмбрионального развития.
Очень тесна в организме взаимосвязь цинка с медью, свинцом, кадмием. Медь - это эссенциальный микроэлемент, участвующий вместе с различными ферментами в обмене железа, синтезе коллагена и меланина. Медь обладает выраженным противовоспалительным свойством. В составе ферментов она необходима для нормального роста и развития костной ткани, играет важнейшую роль в функционировании центральной нервной системы. Клинические признаки дефицита меди включают анемию, устойчивую к препаратам железа, задержку психомоторного развития, общую гипотонию, изменения костной ткани, иммунитета, цирроз печени и повышение уровня холестерина. Основным источником поступления меди в окружающую среду являются предприятия цветной металлургии, транспорт, удобрения, пестициды. В промышленных центрах с высоким уровнем загрязнения внешней среды возможно поступление в организм избыточного количества металлов. Симптомы отравления солями меди - тошнота, рвота, головная боль, диарея и боли в животе. Могут развиться повреждение печени, желтуха и анемия.
Кобальт участвует в кроветворении, играет роль активатора ферментов в обмене веществ. Физиологический эффект кобальта обусловлен его присутствием в молекуле витамина B12. Потребность птицы в железе, меди и кобальта невелика. Все эти микроэлементы участвуют в процессах кроветворения.[21]
Цинк входит в состав многих ферментов, а также участвует в процессах костеобразования, кроветворения, формирования скорлупы и оперения, влияет на рост, развитие и воспроизводительную функцию организма. Дефицит цинка обнаруживается у птицы при избытке кальция в рационе. Высокий уровень кальция, особенно в присутствии фитиновой кислоты, замедляет абсорбцию цинка и может быть причиной его вторичной недостаточности.
Микроэлементу отводится важная роль в развитии иммунологических реакций, особенно клеточного иммунитета. Цинк принимает участие в функционировании гормонов гипофиза (гормонов роста), надпочечников, поджелудочной железы (инсулина), предстательных желез и семенников. Он незаменим для нормального развития и работы органов чувств: вкуса, зрения, обоняния. В условиях недостатка цинка развивается снижение вкусовой чувствительности (снижение аппетита) и гипоосмия (снижение обоняния). Клетки слизистой оболочки кишечника и кожи обновляются постоянно и нуждаются в цинке. Дефициту цинка придается особое значение при формировании дисфункций и появлении заболеваний органов пищеварения. Достоверным отражением содержания цинка в организме считается его концентрация в волосах. Она равна 3,3 мкмоль/л, снижается с возрастом и подвержена сезонным колебаниям. Недостаток цинка может развиваться при различных состояниях, сопровождающихся нарушением всасывания, таких как диарея, непереносимость глютена (целиакия), недостаточность лактазы. При хронических заболеваниях органов пищеварения также отмечены симптомы недостаточности цинка. Дефицит цинка влияет на центральную и периферическую нервную систему. Расстройства проявляются поведенческими нарушениями, эмоциональной неустойчивостью, снижением памяти и способности к обучению, периферическими нейропатиями. Цинкдефицитное состояние провоцирует замедленное заживление ран. Недостаток цинка развивается также у больных хроническими заболеваниями органов дыхания, бронхиальной астмой. Скрытый дефицит цинка часто встречается при рахите, ревматизме, хроническом пиелонефрите, нефротическом синдроме, острых инфекционных заболеваниях, ожогах, сахарном диабете, гипотиреозе (недостаточная выработка гормонов щитовидной железы). Избыток цинка в организме возникает исключительно при отравлении цинксодержащими соединениями. Воздействие солей цинка может раздражать кожу, дыхательные пути и желудочно-кишечный тракт. Нечастое пероральное отравление обусловлено использованием воды из гальванизированных бидонов и вызывает лихорадку и желудочно-кишечные расстройства.
Марганец активизирует окислительные процессы и обладает специфическим липотропным действием, повышает утилизацию жиров в организме противодействует жировой дегенерации печени. Недостаток его в организме птицы вызывает заболевание - перозис, при котором сильно увеличен скакательный сустав, скручен или изогнут нижний конец большой берцовой кости и верхний конец плюсны, пяточное сухожилие соскакивает с мыщелка. При недостатке марганца снижается яйценоскость ухудшается качество скорлупы и состояние оперения, снижаются воспроизводительные качества (оплодотворенность яиц и выводимость цыплят). Эмбрионы гибнут на 20-21 день инкубации. На вскрытии обнаруживают признаки хондродистрофии — ноги укорочены, клюв искривлен (попугаев). У вылупившихся цыплят иногда отмечают атаксию, повышенную возбудимость, в последующем проявляются признаки перозиса. Марганцевая недостаточное усугубляется при избытке кальция и фосфора.
Магний наряду с кальцием в виде ортофосфата образует костную ткань. Им богаты все зеленые овощи: магний входит в состав хлорофилла. Ежесуточная потребность в магнии составляет 0,4 г. В организме взрослого человека его содержится около 25 г(преимущественно в составе костной ткани). Магний нужен для высвобождения энергии углеводов при их окислении в организме, участвует в нормализации возбудимости нервной системы, благоприятно влияет на функциональное состояние мышц сердца и его кровоснабжения, обладает антиспастическим и сосудорасширяющим действием, стимулирует двигательную функцию кишечника и желчеотделение, способствует выведению холестерина из организма. При длительной недостаточности магния в организме наблюдается усиленное отложение солей кальция в стенках артериальных сосудов, сердечной мышце и почках. Избыток в пище жиров и кальция тормозят усвоение магния. Оптимальное усвоение его происходит при соотношении кальция и магния, близком к 1:0,5. Некоторые географические районы отличаются повышенным содержанием магния в окружающей среде и соответственно в местных продуктах питания. В этих районах регистрируется значительно более низкая заболеваемость злокачественными новообразованиями. В то же время избыток солей магния в крови сопровождается возникновением наркотического состояния, которое может сниматься введением солей кальция. Высоким содержанием магния отличаются продукты растительного происхождения. В этом отношении в первую очередь можно назвать пшеничные отруби, овсяную крупу, абрикосы, фасоль, чернослив. Несколько меньше количество его в гречневой и перловой крупе, горохе, хлебе, укропе, салате.
Калий жизненно необходимый минеральный элемент питания из числа макроэлементов. Он играет важную роль в функционировании клеток всех тканей организма, является непременным компонентом систем обеспечения кислотно-щелочного равновесия в тканевых и межтканевых жидкостях. Это необходимо для нормального обмена веществ, что в свою очередь предопределяет хорошее самочувствие.
Отличительная особенность калия— его способность вызывать усиленное выведение воды из организма. Поэтому пищевые рационы с повышенным содержанием элемента облегчают функционирование сердечно-сосудистой системы при ее недостаточности, обусловливают исчезновение или существенное уменьшение отеков. Недостаток калия приводит к нарушению деятельности сердечной мышцы, повышению давления, кровоизлиянию в мозг, расстройству желудка, нарушениям в работе нервной системы и мышц, усталости, слабости мышц, повышению уровня сахара в крови, сухости кожи, необычной жажде, отеку конечностей. Недостаток калия может быть вызван применением некоторых лекарственных препаратов.
Йод необходим для синтеза гормонов щитовидной железы. При недостатке йода увеличивается щитовидная железа, нарушается синтез тиреоидных гормонов, что приводит к снижению яичной и мясной продуктивности, массы яиц, выводимости яиц, уменьшается масса эмбриона, цыплята выводятся слабыми, с увеличенной щитовидной железой. Представление о йоде как об одном из микроэлементов прежде всего связано с возможностью возникновения эндемического зоба при его недостаточности во внешней среде, особенно в продуктах питания (избыток йода в окружающей нас природной среде неизвестен). Регионы, где ощущается дефицит йода, достаточно обширны. Источником йода являются пища и вода, а в приморских районах и воздух. В организме он обнаруживается во всех тканях, но основное его количество сосредоточено в щитовидной железе. Биологическая роль йода заключается в обеспечении нормального состояния и функционирования щитовидной железы. Соединения йода способны выполнять радиозащитную функцию. Дефицит йода в организме провоцируют суперхлорированная вода, консерванты и токсическое воздействие промышленных отходов. Известно, что на содержание йода в пищевых продуктах оказывают влияние сроки и условия хранения. Так, например, при хранении картофеля содержание в нем йода значительно снижается, потери с октября по май составляют до 64,5%. Весьма эффективно введение в рацион йодистого калия. Обычно для этой цели йодируют пищевую соль из расчета 25 г на 1 т соли. Такая соль привносит в суточный рацион около 0,2 мг (200 мкг) йода. При этом нужно учитывать нестойкость йодного компонента при хранении соли. В связи с большой гигроскопичностью соли хранение ее должно осуществляться в сухих местах с предельным сроком в 6 месяцев. По истечении этого срока соль переходит в категорию обычной. Источники йода: вода, морские водоросли. Очень много йода в рыбьем жире.
Селен является составной частью фермента глютатионпероксидазы, необходимого для гашения перекисей в процессе метаболизма, необходим для регуляции проницаемости клеточных мембран, предотвращения миопатии желудка и сердца, фиброзной дегенерации поджелудочной железы. Один из важнейших антиоксидантов, входит в состав ферментов, защищающих организм от свободных радикалов, без него невозможно нормальное развитие и размножение, работа печени, щитовидной железы, он обеспечивает здоровье кожи.
При остром отравлении возникают гемморагические воспаления кишечника, блокада окисления и, как следствие, отек легких и обескровливание печени. Синергистами селена являются витамин Е и антиоксиданты, например, сантохин. Антагонистами селена являются свинец и ртуть. Селен может служить антидотом при отравлении ртутью и свинцом. Таким образом, характеризуя роль макро- и микроэлементов в питании птицы, следует отметить, что в практических условиях в рационах для сельскохозяйственной птицы возможен дефицит по основным макроэлементам: кальцию, фосфору и натрию. Для удовлетворения потребности птицы в этих ферментах в комбикорма вводят минеральные добавки, являющиеся источниками кальция, фосфора и натрия, по нормам, обеспечивающим потребность конкретных видов и возрастных групп птицы. Следует учитывать, что дефицит белковых кормов животного происхождения в комбикормах для птицы приводит к снижению доступного фосфора и к увеличению содержания фитинового фосфора, который усваивается птицей только на 30-50 %. При этом создается недостаточность рационов и по кальцию, вызванная образованием плохо усвояемой формы фитата кальция. Дефицит доступного фосфора восполняют введением источников фосфора в виде кормовых фосфатов.
Основные компоненты комбикормов для птицы дефицитны по марганцу, и йоду и менее дефицитны по меди, железу, кобальту. Для сбалансированности рационов по микроэлементам разработана система гарантированных добавок без учета содержания их в кормах. Микроэлементы в комбикорма вводят в составе витаминно-минеральных премиксов.
1.2. Нормы добавок, ПДК, состав макро- и
микроэлементов в комбикормах
Таблица 5
Нормы добавок микроэлементов в комбикорма для птицы
(г элемента на 1 т комбикорма)
|
Вид птицы и возраст |
Марганец |
Цинк |
Железо |
Медь |
Кобальт |
Йод |
Селен |
|
|
Яичные куры |
100 |
70 |
25 |
2,5
|
1,0 |
0,7 |
0,2 |
|
|
Мясные куры: |
|
|
|
|
|
|
|
|
|
при напольном содержании |
100 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
при клеточном содержании |
100 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
Молодняк яичных кур |
70 |
60 |
25 |
2,5 |
1,0 |
0,7 |
- |
|
|
Молодняк мясных кур при напольном содержании |
70 |
60 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
То же при клеточном содержании в возрасте нед.: |
|
|
|
|
|
|
|
|
|
1-7 |
100 |
60 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
8-26 |
70 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
Цыплята-бройлеры |
100 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
Индейки |
100 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
Молодняк индеек в возрасте, нед.: |
|
|
|
|
|
|
|
|
|
1-2 |
100 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
3-4 |
100 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
13 и старше |
100 |
70 |
25 |
2,5 |
1,0 |
0,7 |
0,2 |
|
|
Фазаны |
100 |
70 |
30 |
2,5 |
1,0 |
0,3 |
0,2 |
|
|
Молодняк фазанов |
100 |
60 |
30 |
2,5 |
1,0 |
0,3 |
0,2 |
|
|
Утки кряковые |
65 |
70 |
30 |
2,5 |
1,0 |
0,3 |
0,2 |
|
|
Молодняк кряковых уток |
85 |
50 |
30 |
2,5 |
1,0 |
0,3 |
0,2 |
|
Критерием полноценности минерального питания служат: интенсивность роста, продуктивность, качество продукции (скорлупа яиц), затраты корма на единицу продукции, состояние скелета, общее состояние здоровья птицы, отдельные характерные биохимические показатели. При нормировании микроэлементов рекомендуется расчет вести в элементарном исчислении, давать полную химическую формулу соединений или указывать степень гидратации. Следует также учитывать возможные вариации в действии отдельных микроэлементов на организм птицы. Как правило, максимальный эффект от действия микроэлементов наблюдается при оптимальной концентрации элемента. При избытке некоторых элементов может происходить снижение биологического действия, например, цинка. В то же время есть элементы, которые практически не токсичны даже в высоких дозах (йод). При очень маленькой потребности птица может переносить высокие дозы этого элемента.
Таблица 6
Токсическая концентрация основных микроэлементов в составе
комбикормов для птицы
|
Элемент |
Вид птицы |
Возраст |
Химич. формула |
Токсическая конц-ция,мг/кг |
Симптомы токсичности |
|
Медь |
Куры |
Рем. молодняк |
CuO |
806 |
Задержка роста, гибель |
|
Куры |
Рем. молодняк |
CuSO4×5H2O |
800 |
Эксудативный диатез, мышечная дистрофия |
|
|
Куры |
Рем. молодняк |
CuSO45H2O |
500 |
Задержка роста, эрозия желудка. На вскрытии обнаруживают зеленовато-голубоватую окраску зоба, гиперемию и эрозии железистого желудка, язвы под кутикулой мышечного желудка. Снижается аппетит и темпы роста |
|
|
Куры |
Рем. молодняк |
CuSO45H2O |
250 |
||
|
Куры |
Рем. молодняк |
CuSO45H2O |
300 |
Задержка роста |
|
|
индейки |
Рем. молодняк |
CuSO45H2O |
676(практ. рацион) |
Задержка роста |
|
|
индейки |
Рем. молодняк |
CuSO45H2O |
800(очищенный рацион) |
Задержка роста |
|
|
индейки |
Рем. молодняк |
CuCO3 |
50(очищенный рацион) |
Задержка роста |
|
|
индейки |
Рем. молодняк |
СuCO3 |
800(практический рацион) |
Задержка роста |
|
|
Йод |
Куры |
Куры-несушки |
KI |
625 |
Снижение яйценоскости, массы яйц, выводимости |
|
Железо |
Куры |
Рем. молодняк |
Fe2(CO4)3 |
4500 |
Рахит |
|
Куры |
Рем. молодняк |
Fe2(CO4)3 |
500 |
Замедление роста, эрозии |
|
|
Марга-нец |
Куры |
Рем. молодняк |
MnCl×4H2O |
4000 |
Задержка роста |
|
Индейки |
Рем. молодняк |
MnSO4H2O |
4800 |
Задержка роста |
|
|
Селен |
Куры |
Рем. молодняк |
Na2SeO3+Se В пшенице |
10 |
Задержка роста |
|
Куры |
Рем. молодняк |
Na2SeO3 |
33-37мг/кг живой массы |
Острое отравление, сопровождающееся геморрогическим воспалением кишечника |
|
|
Куры |
Несушки |
Na2SeO3 |
10 |
Снижение выводимости |
|
|
Кобальт |
Куры |
Рем. молодняк |
CoCl26H2O |
200 |
Задержка роста |
|
Куры |
Рем. молодняк |
CoCl2 |
100 |
Задержка роста |
|
|
Цинк |
Куры |
Рем. молодняк |
ZnSO4 ZnSO3 |
1500 |
Задержка роста |
|
Куры |
Рем. молодняк |
ZnO |
3000 |
Задержка роста |
|
|
Куры |
Несушки |
ZnO |
3000 |
Угнетение репродуктивной функции |
Большинство из этих элементов концентрируется в печени, почках, или в меньшей степени - в мышечной ткани. Накапливаясь в печени и почках, токсичные элементы отрицательно влияют на их функцию, возможность обезвреживать и выводить различные вредные вещества, поступающие из пищеварительного тракта. Из химических элементов наибольшее токсикологическое и санитарное значение имеют тяжелые металлы (ртуть, кадмий, свинец и т.д.), а также металлоиды - мышьяк, фтор, сурьма, селен. На эти элементы установлены допустимые уровни в кормах.
Таблица 7
Предельно допустимый уровень некоторых химических элементов в
комбикормах для птицы
|
Химические элементы |
Птица на откорме мг\кг |
Куры, мг/кг |
|
Кадмий |
0,4 |
0,3 |
|
Свинец |
5,0 |
,0 |
|
Медь |
80,0 |
80,0 |
|
Железо |
200,0 |
100,0 |
|
Селен |
1,0 |
0,5 |
|
Фтор |
50,0 |
20,0 |
|
Йод |
5,0 |
2,0 |
|
Кобальт |
3,0 |
2,0 |
Исключение составляет зерно, протравленное гранозеном, при скармливании которого наблюдаются клинические признаки ртутного отравления: отказ от корма и воды, слезо- и слюнотечение, рвота, понос, мышечная слабость, исхудание, нарушение координации движений, параличи и парезы конечностей, ослабление дыхания, замедление сердечных сокращений, у цыплят - отечность головы, у кур яйцекладка понижается или прекращается. В целях профилактики ртутных отравлений запрещается скармливать протравленное зерно, использовать его для приготовления комбикормов и для проращивания и выращивания гидропонной зелени. Для профилактики ртутных отравлений рекомендуется использовать элементарную серу и ее соединения, молоко и молочные продукты, метионин. Для предотвращения отравлений соединениями ртути рекомендуется выращивать гидропонную зелень и прогнивать зерно из протравленных семян.
Кадмий по физико-химическим свойствам близок к цинку и в природе встречается вместе с этим элементом. Минимально токсичная доза кадмия в хронических опытах, вызывающая дегенеративные изменения в печени, находится на уровне 5-10, максимальная нетоксичная - в пределах 1-2 мг/кг корма. Клинические признаки отравления нечетко выражены, но всегда сопровождаются снижением поедаемости кормов, интенсивности роста цыплят и яйценоскости кур. В крови уменьшается количество гемоглобина. Содержание кадмия в кормах для бройлеров на уровне 5 мг/кг приводит к поражению костной ткани, при 3 мг/ кг регистрируются энтериты и нефриты. Допустимый уровень кадмия в кормах составляет 0,3-0,4 мг/кг. Кадмий - антагонист цинка, меди, железа и других элементов, поэтому токсичность его в значительной степени зависит от уровня их содержания кормах.
Свинец при попадании в организм через корма накапливается в первую очередь в костной ткани, затем в убывающем ряду идут печень, почки. Однако даже при сравнительно невысоком содержании свинца в кормах (свыше 10 мг/кг) возможно его накопление в костной ткани до значительного уровня. Клинические признаки хронической интоксикации характеризуются постепенной потерей в весе, общей слабостью, снижением продуктивности. Пороговая концентрация свинца в воде 0,2—10 мг/л, поэтому ПДК свинца составляет 0,1 мг/л. Максимально нетоксичная доза свинца составляет 50 мг/ корма, токсичная — 100 мг/кг. Для профилактики отравлений соединениями свинца рекомендуется исключать из рациона корма и воду, содержащие свинец в количествах, превышающих ПДК. Малые дозы сульфата натрия или сульфата магния (50-100 мг/кг массы тела), задаваемые внутрь 2-3 раза в неделю, будут взаимодействовать с соединениями свинца, переводить его в нерастворимые соли и выводить через кишечник из организма.
Мышьяк широко распространен в природе, соединения мышьяка обладают местным раздражающим действием, вызывают повреждение капилляров, блокируют синтез сульфгидрильных групп ферментов, в результате чего нарушается тканевое дыхание, оказывают непосредственное влияние на нервную систему. Фоновый уровень содержания мышьяка в условно благополучных зонах в кормовых средствах составляет 0,2-0,5 мг/кг, в районах рудных мышьяковых и медных месторождений он может достигать 5,0 мг/кг. Высокую концентрацию мышьяка находят в рыбной и особенно в крилевой муке, где количество элемента составляет от 20 до 50 мг/кг. Максимально недействующая доза мышьяка при хроническом воздействии для наиболее токсичных соединений находится на уровне 0,5; минимально токсическая - 5 мг/кг корма. Однако величины предпороговой и пороговой доз мышьяксодержащих веществ в значительной степени варьируют в зависимости от вида соединений.
Учитывая, что перечисленные выше элементы накапливаются в органах и тканях птицы, в таблице приведем допустимые уровни некоторых из них.
Таблица 8
Допустимые уровни некоторых химических элементов в
мясе и яйцах птицы, (ПДК мг/кг)
|
Показатели |
Мясо, в т.ч. полуфабрикаты, свежие, охлажденные, замороженные (все виды) |
Субпродукты птицы, охлажденные, замороженные |
Яйца и продукты их переработки (яйцо, меланж) |
Яичный порошок |
|
Кадмий |
0,05 |
0,3 |
0,01 |
0,1 |
|
Медь |
5,0 |
- |
3,0 |
15,0 |
|
Мышьяк |
0,1 |
1,0 |
0,1 |
0,6 |
|
Свинец |
0,5 |
0,6 |
0,3 |
3,0 |
|
Цинк |
70,0 |
70,0 |
50,0 |
200,0 |
Фтор попадает в корма через применение фосфорных удобрений, он в значительных количествах может присутствовать в кормовых фосфатах, мясокостной и рыбной муке, кормах микробиологического синтеза, при получении которых в состав питательной среды вводят суперфосфат. Токсичность фтора зависит от физико-химических свойств, прежде всего, растворимости в воде. Водорастворимые соединения имеют наибольшую токсичность, так как они полностью усваиваются организмом. При хронической интоксикации фтором у птицы возможны нарушения минерального обмена. Поэтому нужно контролировать минеральные корма, особенно известняки и фосфаты, корма микробиологического синтеза и воду на содержание этого элемента и своевременно их исключать или ограничивать ввод. Общее правило для любых отравлений - это замена кормов и воды, если таковы загрязнены, а также исключение лекарственных препаратов, содержащих те или иные соединения тяжелых металлов.
В комбикормах в повышенных количествах могут содержаться нитраты и нитриты. Токсичность воды и кормов с высоким содержанием нитратов и нитритов зависит от многих факторов. Основным следует считать дозу поступивших в организм нитратов и нитритов. Птица менее чувствительна к нитратам и переносит большие их дозы. Чувствительность птицы к нитратам и нитритам значительно повышается при голодании, ограниченном поении, заболевании колибактериозом и сальмонеллезом, одновременном применении нитрофурациновых лекарственных препаратов. У птицы характерным признаком хронической интоксикации является резкое снижение выводимости, кровяные пятна в яйцах, массовое появление яиц без скорлупы и аномалия органов у цыплят.В соответствии с ГОСТ 2874-82 «Вода питьевая» предельно допустимая концентрация (ПДК) нитратов в воде составляет 10 мг/л, нитритов - 1 мг/л.
Таблица 9
Нормы предельно допустимой концентрации (ПДК)
нитратов и нитритов в кормах для птицы (мг/кг)
|
Корма и сырье |
Нитраты NO3- |
Нитриты NO2- |
|
Комбикорм |
500 |
10 |
|
Зернофураж и продукты переработки зерна |
500 |
10 |
|
Жмыхи, шроты |
200 |
10 |
|
Сырье местного животного происхождения (мясо-костная и рыбная мука, сухое молоко) |
250 |
10 |
|
Дрожжи кормовые, гидролизные,БВК |
300 |
10 |
|
Травяная мука |
2000 |
10 |
|
Хвойная мука |
1000 |
10 |
|
Жом свекловичный |
800 |
10 |
При сложившейся структуре и традиционном кормлении птица испытывает дефицит в сере. В организме сера участвует в процессах обмена веще построения тканей в окислительной и восстановительной формах. Дефицит восстановленной серы обычно восполняется за счет добавок метионина или белковых кормов, тогда как дефицит в окислительной сере продолжает оставаться. Организм его восполняет путем окисления метионина. Таким образом, включение в рацион окисленной серы позволяет удовлетворять потребность «организма в этой форме и не отвлекать для этой цели серосодержащие аминокислоты. Для кормления птицы используют сульфат натрия согласно ГОСТ 6318-77, или второго сорта марки А. Может быть также использован сульфат марки Б, однако он гигроскопичен и при хранении слеживается. Сульфат натрия добавляют в комбикорма цыплятам-бройлерам с 7-го дня жизни и взрослым курам только в измельченном воде, по 2,5-3,0 кг на 1 т корма. Использование сульфата натрия исключает необходимость добавок поваренной соли. Скармливание птице кормов с добавкой сульфата натрия позволяет повыситъ на 2-3 % живую массу цыплят-бройлеров, на 1-2 % - эффективность использования ими корма и на 1,0-1,5 % - яйценоскость кур. Соль сульфатная кормовая предназначена для удовлетворения организма сельскохозяйственных животных в натрии и хлоре. Представляет собой однородный сыпучий мелкий кристаллический порошок белого цвета, соленого вкуса, без запаха, не горюч, не взрывоопасен, гидрофилен, устойчив при хранении как отдельно, так и в составе комбикормов. Слеживаемость средняя.
Таблица 10
Состав сульфатной кормовой соли
|
соединения |
процентный состав |
|
сульфат натрия Na2SO4 |
18-20% |
|
карбонат натрия Na2CO3 |
0,4-0,5% |
|
карбонат магния MgCO3 |
0,85-1,00% |
|
нерастворимый в соляной кислоте остаток |
0,5-1,5% |
|
хлорид натрия NaCl |
75-80% |
Сульфатная кормовая смесь используется в составе премиксов, комбикормов и других кормов, вводят в рацион для птицы в количестве от 0,1 до 0,5%. Соль сульфатную кормовую хранят в закрытых сухих складских помещениях. Срок хранения не ограничен. Производство и применение соли сульфатной кормовой регламентировано ГОСТом 18-87-85 Минхимпрома. [20] Для удовлетворения потребности птицы в марганце, цинке, железе используют, как правило, сернокислые и углекислые соли. Пиролюзит активированный технический (МnО2 Мn2О3) представляет cобой зернистый продукт черного цвета, полученный обжигом пиролюзита (марганцевой руды) с последующей обработкой серной кислотой по регламенту, утвержденному в установленном порядке. В процессе хранения стоек. Препарат содержит оксиды марганца четырехвалентного (МnО2) не менее 70 % и оксиды трехвалентного (Мn2О3) не более 15%. Примеси свинца Pb и мышьяка As отсутствуют. Для получения продукта с частицами требуемого размера его измельчают (0,3-0,5 мм). Продукты измельчения пиролюзита достаточно равномерно распределяются в различных наполнителях, не оказывают отрицательного влияния на сохранность витаминов в премиксах. Марганец углекислый основной неочищенный (МnСО3(ОН)2Н2О) представляет собой порошок от светло-коричневого до коричневого цвета с влажностью 30 %, слеживается. Содержит марганца не менее 42 %, свинца - не более 0,005 %, мышьяк отсутствует. Высушивание марганца углекислого основного неочищенного до влажности 10 % и менее способствует тому, что продукт приобретает технологические свойства: имеет высокодисперсную структуру, не слеживается. Двуоксид марганца (МnО2) — однородный сыпучий порошок черного цвета с влажностью 0,5 %, не слеживается, практически не гигроскопичен. Содержит оксида марганца не менее 75 %, свинца - не более 0,005 %. Отличается высокой распыляемостью из-за содержания большого количества (31,1 %) частиц малых размеров. В смеси с пшеничными отрубями и измельченными зерновыми культурами распределяется равномерно. Результаты определения физико- химических свойств, распределяемости и активности витаминов в премиксах с двуоксидом марганца позволяют рекомендовать ее для применения в комбикормовой промышленности без предварительной подготовки. Пероксидный концентрат представляет собой зернистый продукт черного цвета с содержанием влаги не более 8 %, гигроскопичен. Перед вводом в премиксы его необходимо измельчать. Содержание двуоксида марганца в пероксидном концентрате первого сорта 87 %, второго - 82 % и третьего сорта 72 %, содержание двуоксида кремния - не более 5, 8 и 10 % соответственно. Пероксидный концентрат не оказывает отрицательного влияния на сохранность витаминов в премиксах. Концентраты марганцевые, содержащие окисные и закисные соединения получают путем обогащения руд на горнообогатительных комбинатах (ГОК) и в рудоуправлениях (РУ) черной металлургии. Они должны представлять собой однородные сыпучие порошки коричневого до черного цвета, без запаха, с размером частиц до 0,1 мм, влажностью не более 1,5 % и содержанием марганца не менее 22,0 %. В марганцевых концентратах соединения ртути и кадмия отсутствуют, концентрация мышьяка и фтора не превышает 0,005 %, концентрация свинца - 0,0004 %. В процессе хранения они стойки, не слеживаются. В премиксах концентраты марганцевые распределяются равномерно и не оказывают отрицательного влияния на сохранность биологически активных веществ, легко усваиваются птицей и могут полностью заменить препараты марганца реактивной чистоты, не уступая последним по эффективности биологического действия.
Оксид цинка (ZnO) - аморфный, не растворимый в воде порошок белого или слегка желтоватого цвета, влажность его 0,2 %, он гигроскопичен, не слеживается. Содержит оксида цинка не менее 99 %, свинца - не более 0,005 %, мышьяка — не более 0,00005 %. Распределяется в смеси с пшеничными отрубями и измельченными зерновыми культурами достаточно равномерно. Результаты изучения технологических свойств препарата позволяют рекомендовать комбикормовой промышленности оксид цинка реактивной чистоты без предварительной подготовки. Препарат не оказывает отрицательного влияния на сохранность витаминов в премиксах.
Железо сернокислое техническое (FeS04 ·7H2O), или купорос железный. По внешнему виду это зеленовато-голубые кристаллы разных размеров, без видимых посторонних включений (механических примесей). Препарат гигроскопичен, слеживается. Содержит сернокислого железа 53-47 %, свинец и мышьяк отсутствуют. Выпускается Верх-Исетским металлургическим заводом (г. Екатеринбург) по ГОСТ 6991-75. Промышленное производство железа сернокислого технического в премиксах возможно только при его смешивании с наполнителем (отрубями пшечными) в соотношении 1:1 и последующем измельчении этой смеси. В составе премиксов препарат не оказывает отрицательного влияния на сохранность биологически активных веществ. Руда сидеритовая содержит железо в форме углекислых соединений. Для использования в птицеводстве рекомендуется руда сидеритовая Бакальского РУ (Челябинская область). Руда должна представлять собой сыпучий порошок серого цвета, без запаха, с размером частиц до 0,1 мм, влажностью - не более 0,1% и содержанием железа не менее 30 %. Вредные и ядовитые примеси могут находиться в следующих количествах, не более: свинец - 0,0001 %, ртуть –1,0005 %, мышьяк - 0,0007 %, фтор - 0,016 % и кадмий - 0,003 %. Распыляемость руды - 0,3%. В процессе хранения она не теряет активности, не слеживается и является доступным источником железа, заменяющим полностью препараты реактивной чистоты. Марганцевая руда содержит не менее 32 % марганца в форме углекислых соединений. Руда должна представлять собой однородный сыпучий порошок с размером частиц до 0,1мм. Содержание свинца и кадмия составляет по 0,02 %, ртуть и мышьяк не обнаружены. В составе премиксов не создает проблемы снижения стабильности витаминов. Смитсонит содержит не менее 34,5 % цинка в форме углекислых соединений, содержание свинца и кадмия не превышает 0,02 %, ртуть и мышьяк не обнаружены. Для птицеводства реализуется в форме порошка. Совместим с другими активными веществами в составе премиксов. Марганцевая руда и смитсонит были испытаны во ВНИТИП в комбикормах для бройлеров и кур при полной замене ими солей химического производства соответствующих микроэлементов. Полученные результаты позволяют рекомендовать включение этого сырья в премиксы для птицы. Нормирование новых источников микроэлементов следует проводить в расчете на чистый элемент.[19]
Препарат йодбелковый кормовой (ТУ-15-04-583-89) - порошок светло-серого или коричневого цвета, содержащий более 20 микроэлементов.
Таблица 11
Состав йодбелкового комбикорма. Микроэлементы
|
Микроэлементы
|
Процентный состав,% |
|
йод |
1,3 |
|
железо |
0,28 |
|
марганец |
0,04 |
|
медь |
0,038 |
|
кобальт |
0,007 |
|
цинк |
0,00097 |
Изготовлен из отходов агаровой промышленности. Препарат можно использовать в составе премиксов в количестве 0,01-0,04 %, заменяя полностью все соли микроэлементов. Концентрат микроэлементов водорослей (ТУ-15-04-582-89) - крупка темно-бурого или черного цвета, содержащая в своем составе свыше 20 микро элементов, в том числе (%): железа - 0,186; меди - 0,05; цинка - 0,0088 марганца - 0,275; йода - 2; кобальта 0,001.Сопоставление данных по содержанию лимитирующих микроэлементов в отходах агарового производства с содержанием их в рыбной муке, соевом и подсолнечном шротах свидетельствует, что новые продукты значительно превосходят традиционные кормовые средства по этим показателям, что позволяет использовать их для полной замены солей лимитирующих микроэлементов. Как и препарат йодбелковый кормовой, концентрат водорослевый может быть использован для замены солей микроэлементов в составе премиксов комбикормов для птицы в количестве 0,1-0,3 %. Что касается йода, то в данном случае его передозировки при использовании водорослевого концентрата микроэлементов и препарата йодбелкового кормового в комбикормах для бройлеров превышают норму добавок соответственно в 5,7-22,8 и 3,7-14,8 раза; Это превышение укладывается в максимально безопасный уровень йода для растущих цыплят, который составляет 50 мг/кг корма, что превышает норму потребности в 133 раза, а гарантийную норму добавки - в 71,4 раза. В комбикормах для кур-несушек при использовании отходов агарного производства превышение концентрации йода также укладывается в физиологически возможный предел. Из литературных источников известно, что максимально безопасный уровень йода для кур составляет 40 мг/кг, что превышает норму потребности в 133 раза, а существующую в нашей стране норму добавки — в 57 раз.[12]
Бишофит природный - комплекс магнийсодержащих солей и микроэлементов высокой гидрофильности (см. рис 7). Представляет собой прозрачную маслянистую жидкость. При плотности 1,326 г/см3 и рН4,9-5,2.
Таблица 12
Химический состав бишофита
|
Общий состав |
Состав микроэлементов |
||
|
Химические соединения |
Концентрация,г/л |
элементы |
Процентный состав, % |
|
хлористый магний |
446,25 |
железо |
0,002 |
|
бромистый магний |
2,96 |
медь |
0,0002 |
|
Хлористый кальций |
0,98 |
кремний |
0,004 |
|
хлористый калий |
0,76 |
кадмий |
0,0088 |
|
хлористый натрий |
0,46 |
висмут |
0,001 |
|
сернокислый кальций |
0,36 |
молибден |
0,001 |
|
кислый углекислый кальций |
0,23 |
литий |
0,0002 |
|
оксид бора |
0,01 |
рубидий |
0,0001 |
|
всего солей |
452,01 |
цезий |
0,0001 |
Хранить бишофит необходимо в стеклянной таре. Срок хранения не ограничен. Бишофит вводят в рацион птицы независимо от ее возраста в количестве от l до 2 мл, или от 400 до 800 мг сухого остатка в расчете на 1 кг корма. По данным Арькова А.А., введение в рацион бишофита стимулирует рост цыплят, способствует увеличению прироста живой массы на 5-7 % более, снижению затрат корма в расчете на 1 кг прироста живой массы на 10-14%, увеличению сохранности цыплят на 2—3 %. Обогащение рациона взрослых кур природным бишофитом в указанной дозировке положительно влияло на прочность скорлупы яиц (снижалось количество боя и насечки), способствовало увеличению яйценоскости на 2-5 % и сохранности птицы - на 1-%.

Рис.7. Бишофит
Вводить бишофит в комбикорм необходимо в составе премикса, который готовят следующим образом: сначала в смеситель подают наполнитель в количестве 90 % от массы премикса, а затем - бишофит, тщательно все перемешивая в течение 15 мин.
КОНТРОЛЬ ТОКСИЧНОСТИ КОРМОВ
При эксплуатации птицы современных кроссов, отличающихся уровнем обмена веществ, следует также предъявлять повышенные требования к качеству кормов и питьевой воды. По показателям безопасности питьевая вода, комбикорма и все компоненты для сельскохозяйственной птицы должны соответствовать ветеринарно-санитарным требованиям, утвержденным в установленном порядке.
Таблица 13
Предельно допустимые концентрации некоторых химических веществ в комбикормах, комбикормовом сырье, кормовых средствах, мг/кг
|
Корма |
Кадмий |
Свинец |
Мышьяк |
Медь |
Цинк |
Селен |
|
Комбикорма для птицы на откорме |
0,4 |
5,0 |
1,0 |
80,0 |
100 |
1,0 |
|
Комбикорма для яичной птицы |
0,3 |
3,0 |
0,5 |
80,0 |
50,0 |
0,5 |
|
Зерно и зернофураж |
0,3 |
5,0 |
0,5 |
30,0 |
50,0 |
0,5 |
|
Жмыхи и шроты |
0,1 |
0,5 |
0,5 |
30,0 |
50,0 |
0,5 |
|
Мука кормовая животного происхождения |
0,3 |
|
|
|
|
|
|
|
5,0 |
2,0 |
80,0 |
100,0 |
- |
|
|
Мука рыбная |
0,3 |
5,0 |
2,0 |
80,0 |
100,0 |
- |
|
Грубые и сочные корма |
0,3 |
5,0 |
0,5 |
30,0 |
50,0 |
1,0 |
|
Продукты микробного синтеза (дрожжи кормовые,белотин, биотрин) |
0,3 |
5,0 |
2,0 |
80,0 |
100,0 |
2,0 |
|
Минеральные кормовые добавки (в т.ч. цеолиты) |
0,4 |
50,0 |
2,0-60,0 |
500,0 |
1000 |
5,0 |
|
Масла растительные |
0,05 |
0,1 |
0,1 |
0,5 |
5,0 |
- |
Таблица 14
Гигиенические требования к качеству питьевой воды
|
Показатель |
Нормативы (ПДК),не более |
Показатель вредности |
Класс опасности |
|
Обобщенные показатели |
|||
|
Водородный показатель, ед. рН |
6-9 |
- |
- |
|
общая минерализация (сухой остаток), мг/л |
1000(1500) |
- |
- |
|
Жесткость общая, мг-экв./л |
7,0 (10) |
- |
- |
|
Неорганические вещества |
|
|
|
|
Железо (Fe, суммарно), мг/л |
0,3(1,0) |
орг. |
3 |
|
Кадмий (Cd, суммарно), мг/л |
0,001 |
С. -Т. |
2 |
|
Марганец (Мn, суммарно), мг/л |
0,1 (0,5) |
орг. |
3 |
|
Медь (Сu, суммарно), мг/л |
1,0 |
орг. |
3 |
|
Мышьяк (As, суммарно), мг/л |
0,05 |
с. -т. |
2 |
|
Нитраты (по NОз), мг/л |
45 |
с.-т. |
3 |
|
Свинец (РЬ, суммарно), мг/л |
0,03 |
с-т. |
2 |
|
Селен (Se, суммарно), мг/л |
0,01 |
с. -т. |
2 |
|
Сульфаты (SO42-), мг/л |
500 |
орг. |
4 |
|
Фториды(F), мг/л |
1,2; 1,5 |
с. -т. |
2 |
|
Хлориды(Сl-), мг/л |
350 |
орг. |
4 |
|
Хром (Сг6+), мг/л |
0,05 |
С.-т |
3 |
|
Цинк(Zn2+), мг/л |
5,0 |
орг. |
3 |
Примечание. «с. - т.» - санитарно-токсикологический норматив, орг. – органолептический норматив.
Таблица 16.Предельно допустимые концентрации химических веществ в питьевой воде, мг/л.
|
Химическое вещество |
ПДК |
|
Растворимые твердые вещества |
500,0 |
|
Соль поваренная (NaCl) |
250,0 |
|
Натрий сульфат |
250,0 |
|
Магний сульфат |
250,0 |
|
Магний |
200,0 |
|
Кальций |
75,0 |
|
Сера |
25,0 |
|
Нитраты (по азоту) |
10,0 |
|
Хром 3-валентный |
0,5 |
|
Медь |
0,3 |
|
Железо |
0,3 |
|
Хром 6-валентный |
0,1 |
|
Мышьяк |
0,05 |
|
Хлор |
0,05 |
|
Фтор |
0,02 |
|
Кадмий |
0,01 |
|
Свинец |
0,01 |
|
Нитриты |
0,0 |
|
Кислород (не менее) |
7,0-14,0 |
|
Коли бактерии (не более) |
500 шт |
В связи с развитием промышленности, увеличением масштабов рудных разработок в последние годы токсичные химические элементы (ртуть, кадмий, свинец, мышьяк, фтор и др.) нередко в значительных количествах загрязняют корма, служат причиной хронических интоксикаций сельскохозяйственных животных, снижения их воспроизводительных качеств, иммунного статуса. Попадая с кормом в организм, они могут ухудшать санитарное качество продуктов.
Большинство из этих элементов концентрируется в печени, почках, костях, в меньшей степени в мышечной ткани. Накапливаясь в печени и почках, токсичные элементы отрицательно влияют на их функцию, возможность обезвреживать и выводить различные вредные вещества, поступающие из пищеварительного тракта. Из химических элементов наибольшее токсикологическое и санитарное значение имеют тяжелые металлы (ртуть, кадмий, свинец и т.д.), а также металлоиды - мышьяк, фтор, сурьма, селен. На эти химические элементы установлены допустимые уровни в кормах. Предельно допустимые концентрации тяжелых металлов в кормах для птицы, по данным зарубежных и отечественных публикаций, представлены в таблицах.
Глава II. Методы качественного и количественного
анализа комбикормов
2.1. Методы определения кальция
КОМПЛЕКСОНОМЕТРИЧЕСКИЙ МЕТОД (основной)
Сущность метода заключается в образовании в щелочной среде малодиссоциированного комплексного соединения кальция с динатриевой солью этилендиамин -N', N', N', N' - тетрауксусной кислоты (трилон Б) и определении эквивалентной точки при титровании с использованием металл-индикаторов. Минерализацию проб проводят способом мокрого или сухого озоления.
1 Определение кальция в пробах, подготовленных способом мокрого озоления. Метод не распространяется на отходы рыбного и мясного производства.
1.1.1 Аппаратура, реактивы и материалы
Измельчитель проб растений марки ИПР-2 или других аналогичных марок, сушилка кормов СК-1 или шкаф сушильный лабораторный с погрешностью поддержания температуры не более 5°С, мельница лабораторная марки МРП-2 или других аналогичных марок, сито с отверстиями диаметром 1 мм, ножницы, ступка фарфоровая с пестиком, весы лабораторные 2-го класса точности с наибольшим пределом взвешивания 200 г по ГОСТ 24104, весы лабораторные 3-го класса точности с наибольшим пределом взвешивания 500 г по ГОСТ 24104, нагревательное устройство для пробирок, нагреватели для колб Кьельдаля, обеспечивающие нагрев 340—380 °С, пробирки из термостойкого стекла или колбы Кьельдаля вместимостью 50—100 см3, колбы конические с широким горлом вместимостью 100 и 250 см3 , колбы мерные 1(2) - 2 - 100(1000) по ГОСТ 1770, цилиндр мерный 1(2,3,4) — 2—100 по ГОСТ 1770, пипетки 1(2,3)- 1(2)- 1(2,5,10) по ГОСТ 29228 и 5-2-1(2,5,10) по ГОСТ 29230, бюретки 1(2) - 1(2) - 5 по ГОСТ 29252 и 2-1,5 по ГОСТ 29253, воронки стеклянные диаметром 36—56 мм по ГОСТ 25336, стакан фарфоровый вместимостью 1000 см3 по ГОСТ 9147, пробки стеклянные или резиновые, кислота серная, х.ч., ч.д.а., селен, перекись водорода, х.ч., ч.д.а., хромоген черный, хром темно-синий кислотный, эриохром сине-черный P(R), трилон Б [Этилендиамин - N', N', N', N'-тетрауксусной кислоты динатриевая соль, 2-водная по ГОСТ 10652, х.ч., ч.д.а. или стандарт титр трилона Б, раствор концентрации 0,01 моль/дм3 (0,02 н.)]. Калия гидроксид по ГОСТ 24363, х.ч., ч.д.а.Аммоний хлористый по ГОСТ 3773, х.ч., ч.д.а. Кальцеин (флуорексон), натрий лимонно-кислый трехзамещенный, 5,5-водный, по ГОСТ 22280, ч.д.а. Гидроксиламин гидрохлорид по ГОСТ 5456, ч.д.а. Триэтаноламин гидрохлорид, триэтаноламин. Кальций углекислый по ГОСТ 4530, х.ч., ч.д.а. Кальций хлористый по ГОСТ 4234, х.ч., ч.д.а. Вода дистиллированная. Соляная кислота х.ч., ч.д.а., концентрированная и разбавленная дистиллированной водой в два раза (1 + 1).
1.1.2 Подготовка к испытанию
1.1.2.1 Подготовка проб.
Среднюю пробу сена, силоса, сенажа или зеленых кормов измельчают на отрезки длиной 1—3 см, корнеплоды и клубнеплоды разрезают на пластинки (ломтики) толщиной до 0,8 см. Методом квартования выделяют часть пробы, масса которой после высушивания должна быть не менее 100 г. Высушивание проб проводят при температуре 60—65°С до постоянной массы (воздушно-сухое состояние). Затем пробу размалывают на лабораторной мельнице и просеивают через сито. Остаток на сите измельчают ножницами или в ступке, добавляют к просеянной части и тщательно перемешивают. Из средней пробы комбикормов или комбикормового сырья методом квартования выделяют около 100 г материала, размалывают без предварительного подсушивания и просеивают через сито. Остаток на сите измельчают и добавляют к пробе, затем перемешивают. Подготовленные пробы хранят в стеклянной или пластмассовой банке в сухом месте. Пробы жидких кормов анализируют без предварительной подготовки.
2.1.2.2 Приготовление растворов и реактивов.
Проверка качества воды: к 100 см3 дистиллированной воды приливают 1 см3 аммиачного буферного раствора и 5—6 капель индикатора хромогена черного. Голубая с сиреневым оттенком окраска раствора указывает на чистоту воды. Приготовление селенсодержащей серной кислоты
К 1000 см3 концентрированной серной кислоты добавляют 5 г селена и нагревают в колбе из термостойкого стекла до полного обесцвечивания раствора.
Приготовление индикаторов
1 г индикатора кальцеина (флуорексона) или эриохрома сине-черного, или хрома темно-синего кислотного смешивают со 100 г хлористого калия и растирают в ступке до однородного состояния. Хранят в сухом месте и в темной посуде с притертой пробкой. Приготовление раствора триэтаноламина гидрохлорида с массовой долей.25 %22,3 см3 триэтаноламина гидрохлорида растворяют в небольшом объеме дистиллированной воды и доводят объем до 100 см3. Раствор триэтаноламина готовят путем разбавления его дистиллированной водой в четыре раза (1+3).
Приготовление раствора углекислого кальция концентрации кальция 0,01 моль/дм31,001 г углекислого кальция, высушенного при температуре 105— 110 °С до постоянной массы, растворяют в 20 см3 разбавленной (1 + 1) соляной кислоты в мерной колбе вместимостью 1000 см3. Объем в колбе доводят до метки дистиллированной водой, тщательно перемешивают.
Приготовление раствора гидроксида калия с массовой долей 20 %
200 г гидроксида калия растворяют в 800 см3 дистиллированной воды. Вначале растворение проводят небольшими порциями при перемешивании в 300 см3 дистиллированной воды в фарфоровом стакане. После растворения щелочи и остывания раствора приливают оставшееся количество воды, перемешивают. Работу проводят в вытяжном шкафу.
Приготовление буферного раствора
20 г хлористого аммония смешивают со 100 см3 25%-ного водного раствора аммиака, после чего объем раствора доводят дистиллированной водой до 1000 см3, перемешивают.
Приготовление раствора трилона Б концентрации 0,01 моль/дм3
Раствор трилона Б готовят из стандарт-титра путем разбавления полученного 0,1 н. раствора дистиллированной водой в пять раз (1+4).При отсутствии стандарт-титра навеску массой 3,722 г растворяют в небольшом объеме дистиллированной воды в мерной колбе вместимостью 1000 см3 и доводят объем до метки дистиллированной водой. Если раствор мутный, его фильтруют. Раствор хранят в полиэтиленовых или стеклянных сосудах в темном месте в течение 6 мес.
Проверка молярной концентрации раствора трилона Б К 5 см3 раствора углекислого кальция добавляют 50 см3 дистиллированной воды, 5 см3 раствора гидроокиси калия, около 30 мг (на кончике скальпеля) одного из индикаторов. После добавления каждого реагента раствор перемешивают. Титруют раствором трилона Б до изменения окраски по п. 2.1.3. Титрование проводят дважды. За результат испытания принимают среднее арифметическое двух определений. Концентрацию (С) трилона Б, моль/дм3, рассчитывают по формуле
С=С1V1/V
где С1 —концентрация раствора углекислого кальция, моль/дм3;
V1 — объем раствора углекислого кальция, взятый для титрования, см3;
V— объем раствора трилона Б, израсходованный на титрование, см3.
2.1.3 Проведение испытания
В колбу или пробирку для сжигания отвешивают 0,2—0,3 г исследуемой пробы, добавляют 2 см3 перекиси водорода и через 1,5—2 мин 3 см3 селенсодержащей серной кислоты и слегка встряхивают. Затем колбы (пробирки) нагревают при температуре 340—380 °С до полного обесцвечивания растворов. Если через 30 мин в колбах и через 1,5 ч в пробирках не происходит обесцвечивания растворов, их охлаждают до 60—80 °С, добавляют 1 см3 перекиси водорода и снова озоляют в течение 30 мин. После обесцвечивания растворы охлаждают, количественно переносят в мерные колбы (или пробирки), доводят объем дистиллированной водой до метки 100 см3 и тщательно перемешивают. Одновременно проводят контрольный опыт через все стадии анализа, кроме взятия навески анализируемого материала. В коническую колбу вместимостью 250 см3 вносят в зависимости от содержания кальция от 5 до 50 см3 исследуемого раствора. Объем раствора доводят дистиллированной водой до 100 см3 (на колбах можно сделать метки и в дальнейшем доливать воду, не измеряя цилиндром). Затем в указанном порядке добавляют на кончике скальпеля (ножа) (около 30 мг) лимонно-кислый натрий, гидроксиламин и 10 см3 20%-ного раствора гидроксида калия (рН исследуемого раствора должен быть не ниже 12,5—13,5), а также около 30 мг одного из индикаторов. После добавления каждого реагента раствор перемешивают. Титруют не позднее чем через 10 мин раствором трилона Б концентрации 0,01 моль/дм3 в присутствии "свидетеля" до перехода окраски от красно-розовой в голубую при использовании эриохрома сине-черного P(R), желто-зеленой в розовую при использовании кальцеина, фиолетовой в синюю при использовании хрома кислотного темно-синего. В качестве "свидетеля" используют 100 см3 дистиллированной воды, в которую добавляют в тех же количествах вышеуказанные реактивы и несколько капель трилона Б. Допускается замена сухих солей лимонно-кислого натрия и гидроксиламина гидрохлорида на триэтаноламин, который вносят в количестве 3 см3.Параллельно проводят титрование контрольного опыта.
2.1.4 Обработка результатов
2.1.4.1 Массовую долю кальция в исследуемой пробе (Х1) в процентах рассчитывают по формуле
V2(V4-V3)×C ×0,040× 100
![]() X1=
X1=
V5 ×m
где V2- исходный объем исследуемого раствора, см3;
V3 -объем раствора трилона Б, израсходованный на титрование контрольного опыта, см3;
V4 -объем раствора трилона Б, израсходованный на титрование исследуемого раствора, см3;
С — концентрация раствора трилона Б;
0,040 — масса кальция, соответствующая 1 см3 раствора трилона Б с молярной концентрацией эквивалента 1 моль/дм3, г;
V5-объем исследуемого раствора, взятый для титрования, см3
m— масса навески, г; 100 — коэффициент пересчета в проценты.
Массовую долю кальция в сухом веществе (X1) в процентах рассчитывают по формуле
X1 100
![]() X2=
X2=
100-W
где X1-массовая доля кальция в исследуемой пробе, %; W — массовая доля воды в исследуемой пробе.
За окончательный результат испытания принимают среднее арифметическое двух параллельных определений. Результаты рассчитывают до третьего десятичного знака и округляют до второго десятичного знака.
2.1.4.2 Допускаемые расхождения между результатами двух параллельных определений (dабс) и между двумя результатами, полученными в разных условиях (Dабс) при доверительной вероятности Р = 0,95 не должны превышать следующих значений: dабс = 0,030 + 0,044 X;
Dабс= 0,06 + 0,14Х2,
где X— среднее арифметическое результатов двух параллельных определений, % ; Х2- среднее арифметическое результатов двух определений, выполненных в разных условиях, %.
![]() Предельную погрешность результата анализа ( å абс) при
односторонней доверительной вероятности Р = 0,95 рассчитывают по формуле
Предельную погрешность результата анализа ( å абс) при
односторонней доверительной вероятности Р = 0,95 рассчитывают по формуле
![]() åабс = 0,035+ 0,0821Х2 Предельная погрешность результата анализа используется
при оценке качества кормов. Допускается проведение анализа без параллельных
определений при наличии в партии исследуемых проб стандартных образцов (СО). В
этом случае (при обязательном проведении выборочного статистического контроля
сходимости параллельных определений) за результат испытания принимают
результат единичного определения, если разница между воспроизведенной и
аттестованной в СО массовой долей кальция не превышает D, рассчитанного по формуле
åабс = 0,035+ 0,0821Х2 Предельная погрешность результата анализа используется
при оценке качества кормов. Допускается проведение анализа без параллельных
определений при наличии в партии исследуемых проб стандартных образцов (СО). В
этом случае (при обязательном проведении выборочного статистического контроля
сходимости параллельных определений) за результат испытания принимают
результат единичного определения, если разница между воспроизведенной и
аттестованной в СО массовой долей кальция не превышает D, рассчитанного по формуле
D = 0,042 + 0,098 Xатг,
где D — допускаемое отклонение среднего результата анализа от аттестованного значения компонента, %; Хатт — аттестованное значение анализируемого компонента, взятое из свидетельства на СО.
2.2 Определение кальция в пробах, подготовленных способом сухого озоления
2.2.1 Аппаратура, реактивы и материалы
Для проведения испытания применяют аппаратуру, реактивы и материалы по п. 2.1.1 со следующим дополнением: перекись водорода по ГОСТ 10929, х.ч., ч.д.а. и разбавленная дистиллированной водой в десять раз (1 +9), печь муфельная с регулируемым нагревом, тигли фарфоровые № 3 или № 4. Щипцы для тиглей муфельные. Водяная баня. Азотная кислота по ГОСТ 4461, х.ч., ч.д.а. Соляная кислота по ГОСТ 3118, х.ч., ч.д.а., разбавленная дистиллированной водой в два раза (1 + 1).2.2.2 Подготовка к испытанию
2.2.2.1 Подготовка проб — по п. 2.1.2.1.
2.2.2.2 Приготовление реактивов и растворов — по п. 2.1.2.2.
2.2.2.3 Проведение испытания
Навеску исследуемой пробы массой 0,5—2,0 г (в зависимости от ожидаемого содержания кальция), взвешенную с точностью до 0,001 г, помещают в предварительно прокаленный и охлажденный тигель. Тигли помещают в холодную муфельную печь и повышают температуру до 200—250 °С. После прекращения выделения дыма температуру повышают до (525±25)°С и ведут прокаливание в течение 4—5 ч при указанной температуре. Равномерный серый цвет золы указывает на хорошее озоление. При наличии несгоревших частиц угля тигель с золой охлаждают на воздухе, прибавляют несколько капель дистиллированной воды и 1—2 см раствора перекиси водорода, разбавленной (1 +9). Содержимое тигля выпаривают (в сушильном шкафу, на электроплитке или другим способом), тигель снова помещают в муфельную печь и прокаливают при температуре (525±25)°С в течение одного часа. Тигель охлаждают и золу смачивают несколькими каплями дистиллированной воды, добавляют 2 см3 раствора соляной кислоты, разбавленной (1 + 1), и 5—10 см3 дистиллированной воды, перемешивают стеклянной палочкой и переносят раствор через воронку в мерную колбу вместимостью 100 см3.Для кормов с высоким содержанием золы добавляют 5 см3 раствора соляной кислоты и нагревают до кипения. При анализе проб костной, мясокостной, рыбной муки золу смачивают несколькими каплями дистиллированной воды, приливают 1 см3 азотной кислоты и 5 см3 соляной кислоты и доводят до кипения на водяной бане. Тигель и воронку тщательно обмывают дистиллированной водой и доводят раствор в колбе водой до метки, тщательно перемешивают, осадку дают отстояться. При анализе проб костной, мясокостной, рыбной муки, а также комбикормов с высоким содержанием кальция исходный раствор золы разбавляют дистиллированной водой в зависимости от ожидаемого содержания кальция в 5—10 раз. Одновременно проводят контрольный опыт через все стадии анализа, кроме взятия навески анализируемого материала. В зависимости от предполагаемого содержания кальция от 5 до 20 см3 исходного раствора золы переносят пипеткой или шприцем-дозатором в широкогорлые колбы вместимостью 250 см3, доводят объем раствора дистиллированной водой до 100 см3 (на колбах можно сделать метки и в дальнейшем доливать воду, не измеряя цилиндром). Сюда же добавляют на кончике ножа (около 30 мг) лимонно-кислый натрий, гидроксиламин и 10 см3 20%-ного раствора гидроксида калия, а также около 30 мг одного из индикаторов. После добавления каждого реагента раствор перемешивают. Титрование проводят раствором трилона Б концентрации 0,01 моль/дм3. В качестве "свидетеля" используют 100 см3 дистиллированной воды, в которую добавляют те же реактивы и несколько капель трилона Б. Допускается замена сухих солей лимонно-кислого натрия, гидроксиламина на раствор триэтаноламина, который приливают в количестве 3 см3.2.2.4 Обработка результатов Обработку результатов, расчет сходимости, воспроизводимости и других точностных нормативов проводят по пп. 2.1.4.1, 2.1.4.2. При вычислении массовой доли кальция учитывают разбавление раствора золы.
3. ПЛАМЕННО-ФОТОМЕТРИЧЕСКИЙ МЕТОД
Сущность метода заключается в сравнении интенсивности излучения кальция в пламени газ-воздух, при введении в него испытуемых растворов и растворов сравнения. Устранение влияния мешающих элементов при определении кальция в соляно-кислых растворах достигается добавлением в фотометрируемые растворы солей стронция при использовании воздушно-пропан-бутановой смеси газов или солей магния при использовании воздушно-ацетиленовой смеси газов.
3.1.Определение кальция в пробах, подготовленных способом сухого озоления
3.1.1 Аппаратура, реактивы и материалы
Весы лабораторные 2-го класса точности с наибольшим пределом взвешивания 200 г по ГОСТ 24104.Весы лабораторные 3-го и 4-го классов точности с наибольшим пределом взвешивания 500 г по ГОСТ 24104.Фотометр пламенный. Колбы мерные 1(2)-2-50 ( 100) 1000 по ГОСТ-1770.Пипетки — по 2.1.1. Бюретки — по 2.1.1.Печь муфельная с регулированием нагрева до 550 "С. Пропан-бутан (бытовой в баллоне или газ городской сети). Ацетилен растворенный технический по ГОСТ 5457.Соляная кислота по ГОСТ 3118, х.ч., ч.д.а., концентрированная и разбавленная дистиллированной водой в два раза (1 + 1) и в сто раз (1+99). Стронций хлористый 6-водный ч.д.а. Магний хлористый 6-водный х.ч., ч.д.а. Кальций углекислый х.ч., ч.д.а. Вода дистиллированная
3.1.2 Подготовка к испытанию
3.1.2.1 Подготовка проб по п. 2.1.2.1.Приготовление растворов и реактивов.
Приготовление раствора хлористого стронция концентрации 20 мг/см3
60,86 г хлористого стронция растворяют в дистиллированной воде, переносят в мерную колбу вместимостью 1000 см3 и доводят до метки дистиллированной водой, перемешивают. Раствор используют при работе на воздушно-пропановой смеси газов. Рабочие растворы хлористого стронция готовят следующим образом: для работы на приборах с дифракционной решеткой готовят раствор с концентрацией стронция 10 мг/см3 разбавлением исходного раствора дистиллированной водой (1 + 1). Для работы на приборах со светофильтрами готовят раствор с концентрацией стронция 2 мг/см3 разбавлением исходного раствора водой (1+9).
Приготовление раствора хлористого магния с концентрацией магния 22 мг/см3.
184 г хлористого магния растворяют в дистиллированной воде, переносят в мерную колбу вместимостью 1000 см3 и доводят водой до метки, тщательно перемешивают. Раствор используют при работе на воздушно-ацетиленовой смеси газов. Рабочие растворы с концентрацией 2,2 мг/см3 магния готовят разбавлением исходного раствора водой (1+9).
Приготовление основного раствора углекислого кальция с концентрацией кальция 1 мг/см3
2,497 г углекислого кальция (реактив предварительно высушивают при температуре 105—110 "С до постоянной массы) переносят в мерную колбу вместимостью 1000 см3, приливают 20 см3 разбавленного (1 + 1) раствора соляной кислоты и перемешивают до полного растворения соли. Затем доливают дистиллированной водой до метки и тщательно перемешивают.
Приготовление растворов сравнения.
В мерные колбы вместимостью 100 см3 отбирают пипеткой или бюреткой объем основного раствора, указанный в табл.1, доводят до метки дистиллированной водой и тщательно перемешивают. Растворы сравнения хранят в течение 1 мес.
3.1.3 Проведение испытания
Сухое озоление и приготовление исследуемых растворов проводят по п. 2.2.3.При фотометрировании в пламени пропан-бутан-воздух пипеткой или дозатором отбирают по 10 см3 испытуемых растворов золы и растворов сравнения в химические стаканы вместимостью 50 см3, приливают дозатором 10 см3 рабочего раствора хлористого стронция и хорошо перемешивают стеклянной палочкой. Фотометрирование проводят на аналитической линии 554 нм при использовании монохроматора или на аналитической линии 623,7 нм при использовании интерференционного светофильтра При фотометрировании в пламени ацетилен-воздух шприцем-дозатором или пипеткой отбирают по 5 см3 испытуемых растворов золы и растворов сравнения в химические стаканы вместимостью 100 см3, приливают дозатором 45 см3 рабочего раствора хлористого магния, хорошо перемешивают стеклянной палочкой и проводят Фотометрирование аналогично вышеуказанному на тех же аналитических линиях. Фотометрирование растворов сравнения проводят дважды в порядке возрастания концентрации кальция до и после фотометрирования испытуемых растворов. Проверку нулевого отсчета шкалы прибора проводят по нулевому раствору сравнения. По окончании фотометрирования строят градуировочный график, откладывая на оси абсцисс значения массы кальция в 100 см3 в миллиграммах, по оси ординат— показания шкалы прибора.Для построения каждой точки градуировочного графика вычисляют среднее арифметическое значение оптической плотности из двух отсчетов по шкале прибора. Если концентрация кальция в анализируемом растворе выходит за пределы градуировочного графика, определение повторяют, разбавив предварительно исходный раствор золы раствором соляной кислоты (1+99). Затем при фотометрировании в пламени ацетилен-воздух к 5 см3 разбавленного раствора приливают 45 см3 раствора хлористого магния, а при фотометрировании в пламени пропан-бутан-воздух к 10 см3 разбавленного раствора приливают 10 см3 раствора хлористого стронция и повторяют измерение. При таком же разбавлении проводят и контрольный опыт.3.1.4 Обработка результатов
Массовую долю кальция в исследуемой пробе (Х3) в процентах рассчитывают по формуле
С1 ×К ×100
![]() Х3=
Х3=
m
где C1 — масса кальция, найденная по градуировочному графику, мг в 100 см3;К— коэффициент разбавления исследуемого раствора золы; m масса навески, мг; 100— коэффициент пересчета в проценты. Массовую долю кальция в сухом веществе (Х4) в процентах рассчитывают по формуле
X3 100
![]() X4=
X4=
100-W
где X3— массовая доля кальция в исследуемой пробе, %; W— массовая доля воды в исследуемой пробе, %.
3.2 Определение кальция в пробах, подготовленных способом мокрого озоления
3.2.1 Аппаратура, реактивы и материалы
Для проведения испытания применяют аппаратуру, реактивы и материалы по п. 2.1.1.3.2.2 Подготовка к испытанию
3.2.2.1 Подготовка проб — по п. 2.1.2.1.
3.2.2.2 Приготовление растворов и реактивов.
Основной раствор углекислого кальция с концентрацией кальция 1 мг/см3 готовят по п. 3.1.2.2. Из основного раствора готовят рабочий раствор с концентрацией кальция 0,1 мг/см3 путем разбавления основного раствора в 10 раз дистиллированной водой (1+9). В мерные колбы вместимостью 100 см3 отбирают объемы рабочего раствора, указанные в табл.2, доливают до половины объема водой, добавляют 3 см3 селенсо-держащей серной кислоты, перемешивают, охлаждают, доводят объем раствора дистиллированной водой до метки и снова перемешивают. Если концентрация кальция в анализируемом растворе выходит за пределы градуировочного графика, определение повторяют, разбавив предварительно исходный раствор золы раствором соляной кислоты (1+99).
Таблица 17. Сравнение растворов
|
Номера растворов сравнения |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
Объем рабочего раствора, см3 |
0 |
0,5 |
1 |
2 |
5 |
10 |
20 |
30 |
|
Масса кальция в 100 см раствора сравнения, мг |
0 |
0,05 |
0,1 |
0,2 |
0,5 |
1,0 |
2,0 |
3,0 |
Мокрое озоление и приготовление зольных растворов проводят по п.2.1.3.
3.2.3 Проведение испытания
Зольные растворы и растворы сравнения вводят в пламя ацетилен-воздух и проводят фотометрирование. Фотометрирование растворов сравнения проводят дважды в порядке возрастания концентрации кальция. После каждого измерения проводят промывку системы подачи растворов водой. По результатам фотометрирования строят градуировочный график, как указано в п. 3.1.3.3.2.4 Обработка результатов
Массовую долю кальция в воздушно-сухой пробе и сухом веществе находят по формулам, указанным в п. 3.1.4.Точностные нормативы рассчитывают по п.2.1.4.2.
4. АТОМНО-АБСОРБЦИОННЫЙ МЕТОД ОПРЕДЕЛЕНИЯ КАЛЬЦИЯ
Метод основан на сравнении поглощения резонансного излучения свободными атомами кальция, образующимися в пламени при введении в него анализируемых растворов золы (минерализата) и растворов сравнения с известной концентрацией данного элемента.4.1 Определение кальция в пробах, подготовленных способом сухого озоления
4.1.1 Аппаратура, реактивы и материалы
Для проведения испытания применяют аппаратуру, реактивы и материалы по п. 2.1.1 со следующим дополнением.
Печь муфельная, обеспечивающая поддержание температуры (550±25)°С. Плитка электрическая. Щипцы муфельные. Атомно-абсорбционный спектрофотометр марки С-115 или аналогичных марок. Лампы с полым катодом Л СП-1.Компрессор воздушный мембранный типа СО-45.Тигли фарфоровые № 3—4.Пробирки вместимостью 20—25 см3.Штатив для пробирок. Шприц-дозатор для дозирования растворов в объемах 1 см3, 5 см3 или 10 см3 с погрешностью не более 1 %.Бюретки — по п. 2.1.1.Ацетилен растворенный технический по ГОСТ/5457 или пропан-бутан бытовой в баллоне. Кислота соляная, х.ч., ч.д.а., концентрированная и разбавленная дистиллированной водой в два раза (1 + 1) и в сто раз (1+99). Стронций хлористый 6-водный, ч.д.а. Перекись водорода 30%-ный водный раствор , х.ч., ч.д.а. и разбавленный дистиллированной водой в десять раз (1+9).
4.1.2 Подготовка к испытанию
4.1.2. Подготовка проб — по п. 2.1.2.1.Приготовление растворов и реактивов.
Приготовление раствора хлористого стронция с концентрацией стронция 10 мг/см3. 30,43 г 6-водного хлористого стронция растворяют примерно в 600 см3 дистиллированной воды, приливают 82 см3 концентрированной соляной кислоты, доводят до метки дистиллированной водой в мерной колбе вместимостью 1000 см3 и тщательно перемешивают.
Приготовление раствора хлористого стронция с концентрацией стронция 5,5 мг/см316,73 г 6-водного хлористого стронция растворяют примерно в 300 см3 дистиллированной воды, приливают 45 см3 концентрированной соляной кислоты, доводят до метки дистиллированной водой в мерной колбе вместимостью 1000 см3 и тщательно перемешивают. Приготовление основного раствора углекислого кальция с концентрацией кальция 0,2 мг/см3
0,499 г углекислого кальция (реактив предварительно высушивают при температуре 105—110 °С до постоянной массы) растворяют в 12,5 см3 разбавленной соляной кислоты (1 + 1), переносят в мерную колбу вместимостью 1000 см3, доливают до метки дистиллированной водой и перемешивают. Раствор хранят не более 3 мес. Приготовление растворов сравнения
В мерные колбы вместимостью 100 см3 из бюреток приливают указанные в табл.3 объемы основного раствора углекислого кальция, приготовленного по п. 4.1.2.2, доливают до метки соляной кислотой (1+99) и перемешивают. Растворы готовят в день проведения анализов и используют для градуирования атомно-абсорбционного спектрофотометра.
Таблица 18 Сравнение растворов
|
Номера колб |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Объем основного раствора, см3 |
0 |
5 |
10 |
20 |
30 |
40 |
50 |
|
Масса кальция в 100 см3 раствора сравнения, мг |
0 |
1,0 |
2,0 |
4,0 |
6,0 |
8,0 |
10,0 |
4.1.3 Проведение испытания Озоление проб проводят по п. 2.2.3.
4.1.3.1 Определение кальция с использованием воздушно-ацетиленового пламени.
Пипеткой или шприцем-дозатором отбирают в пробирки по 1 см3 растворов сравнения и раствора золы (минерализата), затем из бюретки или дозатором приливают по 10 см3 раствора хлористого стронция с концентрацией стронция 5,5 мг/см3 и перемешивают. Определение кальция проводят по аналитической линии 422.7 нм. Ширину щели монохроматора, расход газов, ток, питающий лампу с полым катодом, устанавливают в соответствии с инструкцией, прилагаемой к прибору и лампе. При использовании пламени ацетилен-воздух в него вводят вначале нулевой раствор сравнения, не содержащий кальция, и устанавливают начало отсчета. Затем вводят в пламя остальные растворы сравнения в порядке возрастания концентрации кальция и регистрируют соответствующие им показания измерительного прибора. Отградуировав прибор по растворам сравнения, в пламя вводят растворы минерализата и регистрируют соответствующие им показания прибора. Одновременно проводят контрольный опыт. Через каждые десять измерений в пламя вводят нулевой и четвертый растворы сравнения для проверки градуировочной характеристики прибора. Если обнаружится отклонение показаний прибора, корректируют его градуировку. Если показание прибора для раствора минерализата превышает показание седьмого раствора сравнения, определение повторяют, разбавив предварительно данный раствор минерализата соляной кислотой (1+99), при этом полученный результат увеличивают во столько раз, во сколько раз был разбавлен раствор минерализата. При таком же разбавлении проводят и контрольный опыт.4.1.3.2
Определение кальция с использованием воздушно-пропан-бутанового пламени.
При использовании пламени пропан-бутан-воздух бюреткой или дозатором приливают в пробирки по 5 см3 растворов сравнения и растворов минерализата, затем туда же приливают по 5 см3 раствора хлористого стронция с концентрацией стронция 10 мг/см3 и перемешивают. Анализируемые растворы вводят в окислительное воздушно-пропан-бутановое пламя и измеряют поглощение света по аналитической линии 422 нм. Градуировку прибора по растворам сравнения, а также разбавление растворов минерализата проводят по и.4.1.3.1.
4.1.3.3 Обработка результатов
Содержание кальция в исследуемой пробе (Х5) в процентах рассчитывают по формуле
(М1-М2) К 100
![]() Х5=
Х5=
m
где M1 — масса кальция в 100 см3 раствора минерализата (золы), мг;
M2 — среднее арифметическое значение массы кальция в100 см3 раствора контрольного опыта, мг; К— коэффициент разбавления анализируемых растворов минерализата; 100 — коэффициент пересчета в проценты;m — масса навески, мг. Массовую долю кальция в сухом веществе в процентах находят по п. 2.1.4.1.Результаты рассчитывают до третьего десятичного знака и округляют до второго десятичного знака. Точностные нормативы находят по п. 2.1.4.2.
5. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ ТИТРИМЕТРИЧЕСКИМ МЕТОДОМ
Метод применим для всех кормов, в которых содержание кальция превышает 1 г/кг. Сущность метода заключается в сжигании образца, обработке золы соляной кислотой и осаждении кальция в виде оксалата кальция, растворении осадка в серной кислоте и титровании стандартным титрованным раствором перманганата калия образующейся щавелевой кислоты.
Реактивы. Все реактивы должны быть аналитического качества, а применяемая вода должна быть дистиллированной. Соляная кислота, приблизительно, 30 % (по массе) Азотная кислота концентрированная Серная кислота, приблизительно 20 % (по массе) Раствор аммиака, приблизительно 33 % (по массе) Оксалат аммония, холодный и насыщенный раствор. Лимонная кислота, моногидрат, раствор концентрации 300 г/см3.
Хлористый аммоний, раствор концентрации 50 г/дм3.Перманганат калия, стандартный раствор, концентрации с (1/5 КМnО4) = 0,1 моль/дм3.
Аппаратура: электрическая муфельная печь с температурой нагрева (550±20)"С. Тигель для прокаливания из платины, кварца или фарфора. Стеклянный фильтр, степень пористости Р 16 (размер пор от 10 до 16 мкм). Кипящая водяная баня. Химический стакан вместимостью 250 см3. Мерная колба вместимостью 250 см3. Аналитические весы.
Методика определения
1.Навеска пробы Взвешивают около 5 г образца с точностью до 1 мг и помещают в тигель для прокаливания.
2. Проведение испытания Навеску сжигают в электрической муфельной печи при температуре (550±20)°С до полного разрушения всего органического вещества (обычно для этого достаточно 4 ч). Если осталось немного органического вещества (черные частицы), то добавляют несколько капель азотной кислоты (п. 6.4.2), выпаривают на горячей плитке и снова сжигают в муфельной печи при температуре (550±20)°С в течение 30 мин. Повторяют сжигание до тех пор, пока не будет разрушено все органическое вещество. Золу переносят в химический стакан вместимостью 250 см3 .Добавляют 40 см3 соляной кислоты , 60 см3 дистиллированной воды и несколько капель азотной кислоты. Доводят до кипения и кипятят в течение 30 мин. Охлаждают и переносят раствор в мерную колбу вместимостью 250 см3 . Доведя водой до метки, перемешивают и фильтруют. При этом получают исследуемый раствор. С помощью пипетки переносят аликвоту исследуемого раствора, содержащую от 10 до 40 мг кальция (в соответствии с ожидаемым содержанием), в химический стакан вместимостью 250 см3. Добавляют 1 см3 раствора лимонной кислоты и 5 см3 раствора хлористого аммония. Доводят объем водой примерно до 100 см3. Доводят до кипения, добавляют 10 капель бромкрезолового зеленого и 30 см3 теплого раствора оксалата аммония. Если образуется осадок, его растворяют, добавив несколько капель соляной кислоты. Нейтрализуют очень медленно раствором аммония при постоянном перемешивании до достижения рН 4,4—4,6 (то есть до изменения цвета индикатора). Помещают стакан на кипящую водяную баню и оставляют на 30 мин, чтобы осел образовавшийся осадок. Снимают стакан с водяной бани, дают раствору постоять 1 ч и фильтруют через стеклянный фильтр. Затем промывают стеклянный фильтр и стакан водой до полного удаления избытка оксалата аммония, о чем свидетельствует отсутствие хлора в промывной воде. Помещают стеклянный фильтр в стакан вместимостью 250 см3. Добавляют 80 см3 серной кислоты и нагревают до 70—80 "С для растворения осадка. Титруют горячий раствор стандартным раствором перманганата калия до появления розового окрашивания, не исчезающего в течение 1 мин.

Рис.8. Определение содержания кальция титриметрическим методом.
3. Обработка результатов. Формула для расчета. Массовую долю кальция (X7) в граммах на килограмм исследуемого продукта рассчитывают по формуле
20,04 V C 250
![]() Х7=
Х7=
mV1
где V— объем стандартного раствора перманганата калия, использованный на титрование, см3; С — точная концентрация стандартного титрованного раствора перманганата калия, моль/дм3; m — масса навески, г;V1— объем аликвоты исследуемого раствора. За результат анализа принимают среднее арифметическое значение двух определений при достаточной сходимости.
4.Сходимость Расхождения между двумя параллельными определениями не должны превышать: 1 г/кг (в абсолютных единицах) — при содержании кальция менее 50 г/кг; 2 % (относительная величина) — при среднем содержании кальция 50 г/кг и более.
5. Замечания по проведению испытания Если образец состоит исключительно из минеральных веществ, его растворяют в соляной кислоте без сжигания. В случае таких продуктов, как алюмокалиевые фосфаты, которые с трудом растворяются в кислотах, смешивают навеску в платиновой чашке с пятикратной массой смеси, содержащей равные части карбоната натрия и карбоната калия. Осторожно нагревают до полного плавления смеси. После охлаждения растворяют в соляной кислоте. Если содержание магния в образце превышает ожидаемое содержание кальция, проводят повторное осаждение оксалатом кальция. 6. Результаты
![]()
6. Методы определения содержания натрия и хлорида натрия
Ионометрический метод определения содержания натрия и хлорида натрия (основной)
Сущность метода состоит в экстракции хлорида натрия, содержащегося в пробе, буферным раствором гидроксида кальция и последующем определении натрия методом добавок с помощью стеклянного натрийселективного электрода ЭСЛ-51-07. Содержание натрия пересчитывают на хлорид натрия. Метод позволяет определять содержание натрия в комбикормах и комбикормовом сырье от 0,023 до 2,3 % и хлорида натрия — от 0,06 до 5,8 %.Аппаратура, материалы и реактивы: цифровой иономер типа И-130М или других марок с аналогичными параметрами; допускается использование стрелочных иономеров типа ЭВ-74 с дискретностью отсчета ±1 мВ; стеклянный натрийселективный электрод ЭСЛ-51-07; электрод сравнения хлорсеребряный насыщенный образцовый 2-го разряда по ГОСТ 17792; мешалка магнитную типа ММ-3; мельничка лабораторного типа МРП или других аналогичных марок; сито с отверстиями диаметром 1 мм; весы лабораторные 2-го класса точности наибольшим пределом взвешивания 200 г; шкаф сушильный температурой нагрева 120°С; аппарат для встряхивания жидкостей в емкостях типа АВУ-бс или других аналогичных марок; колбы конические вместимостью 500 см3 ;колбы мерные вместимостью 1000, 200, 100 и 50 см3 ;стаканы стеклянные вместимостью 100 см3 ;пипетки вместимостью 50; 20; 10; 5 и 1 см3 ;воронка стеклянная диаметром 6 см; натрия хлорид , х.ч.; кальция гидроксид, стандарт-титр, рН 12,45; бумага фильтровальная; вода дистиллированная.
Подготовка к проведению анализа Подготовка проб
Из средней пробы комбикорма или комбикормового сырья методом квартования выделяют около 100 г продукта, измельчают на лабораторной мельничке и просеивают через сито с отверстиями диаметром 1 мм. Подготовленные пробы хранят в стеклянных или пластмассовых емкостях с крышками в сухом месте.
Приготовление растворов Буферный раствор гидроксида кальция рН 12,45 готовят из стандарт-титра согласно прилагаемой к нему инструкции.
Приготовление раствора для экстракции хлорида натрия
20 см3 буферного раствора гидроксида кальция (рН 12,45), приготовленного согласно, переносят в мерную колбу вместимостью 200 см3, доводят до метки водой и тщательно перемешивают.
Приготовление раствора хлорида натрия молярной концентрации c(NaCl) 0,5 моль/дм3.
Навеску хлорида натрия 2,9222 г, предварительно высушенного при 120°С до постоянной массы, переносят в мерную колбу вместимостью 100 см3, растворяют при перемешивании в дистиллированной воде и доводят до метки. Содержимое колбы тщательно перемешивают.
Приготовление раствора хлорида натрия молярной концентрации c(NaCl) 0,05 моль/дм3
10 см3 раствора хлорида натрия молярной концентрации c(NaCl) = 0,5 моль/дм3 переносят в мерную колбу вместимостью 100 см3, доводят до метки дистиллированной водой и тщательно перемешивают.
Приготовление раствора хлорида натрия молярной концентрации c(NaCl) 0,001 моль/дм3
2 см3 раствора хлорида натрия молярной концентрации c(NaCl) = 0,5 моль/дм3 переносят в мерную колбу вместимостью 1000 см3 и доводят до метки дистиллированной водой. Содержимое колбы тщательно перемешивают.
Подготовка индикаторного натрийселективного электрода ЭСЛ-51-07Перед анализом каждой пробы электрод в течение 10 мин выдерживают при перемешивании в дистиллированной воде с ее двухразовой сменой, а затем в течение 5 мин в растворе хлорида натрия молярной концентрации c(NaCl) = 0,001 моль/дм3. После проведения анализа электродную пару тщательно промывают дистиллированной водой и протирают фильтровальной бумагой.
Порядок проведения анализа
Навеску пробы массой около 0,6; 6,0 и 30,0 г (при ожидаемом содержании хлорида натрия соответственно 3,0; 1,0 и 0,1 %) взвешивают с погрешностью не более 0,0002 г и переносят в коническую колбу вместимостью 500 см3 с притертой пробкой. Добавляют 200 см3 раствора, приготовленного согласно и взбалтывают в течение 10 мин.
5 см3 полученной суспензии переносят в мерную колбу вместимостью 50 см3, добавляют 0,5 см3 раствора хлорида натрия молярной концентрации c(NaCl) = 0,05 моль/дм3, 5 см3 буферного раствора гидроксида кальция и доводят водой до метки. Раствор перемешивают и количественно переносят в первый стакан, куда опускают электродную пару и магнитную вертушку. Измеряют ЭДС цепи до постоянного значения потенциала. Электродную пару опускают во второй стакан с 50 см3 полученной суспензии и измеряют ЭДС цепи. После установления постоянного значения потенциала к суспензии добавляют 0,5 см3 раствора хлорида натрия молярной концентрации c(NaCl) = 0,5 моль/дм3 и снова измеряют ЭДС до постоянного значения потенциала. Полученные значения потенциалов фиксируют в лабораторном журнале.
Расчет результатов анализа
Массовую долю натрия в пробе Х1 %, рассчитывают по формуле
2,2990
![]() Х1=
Х1=
(10 Е3-Е2/S-1)m
где 2,2990 — содержание натрия в 200 см3 раствора хлорида натрия молярной концентрации c(NaCl) = 0,5 моль/дм3, г; Е3-Е2— изменение потенциала, мВ; S = Е3-Е2 — крутизна электродной функции, Na+ мВ/р; т — масса навески, г.За конечный результат анализа принимают среднеарифметическое результатов двух параллельных определений. Результаты округляют до второго десятичного знака при содержании натрия более 0,1 % и до третьего — при содержании менее 0,1 %.Массовую долю натрия в сухом веществе Х2 %, рассчитывают по формулеХ1 100
![]() Х2=
Х2=
100-W
где W— влажность пробы, %/Массовую долю хлорида натрия в пробе Х3, %, рассчитывают по формулеХ3 = 2,54 ×X1,где 2,54 — коэффициент пересчета натрия на хлорид натрия. Массовую долю хлорида натрия в сухом веществе Х4, %, рассчитывают по формулеX4=2,54 X2Показатели точности анализа Допустимые расхождения между результатами двух параллельных определений (dабс.) и между двумя результатами, полученными в разных лабораториях (Dабс.) при доверительной вероятности Р = 0,95 не должны превышать следующих значений:d абс= 0,061 Х=1+0,011,Dабс. = 0,084 Х2= 1+0,051,где X— среднее арифметическое результатов двух параллельных определений, %; X2— среднее арифметическое результатов двух определений, выполненных в разных лабораториях, %; 0,061; 0,084; 0,011; 0,051 — коэффициенты регрессии.
![]() Предельную погрешность
результата анализа ( абс.) при доверительной вероятности Р = 0,95
определяют по формуле
Предельную погрешность
результата анализа ( абс.) при доверительной вероятности Р = 0,95
определяют по формуле
![]() абс. = 0,05X+0,03, где 0,05;
0,03 — коэффициенты регрессии.Допускается проведение анализа без параллельных
определений при наличии в партии испытуемых проб стандартных образцов. За
результат испытания принимают результат единичного определения, если разница
между воспроизведенным и аттестованным значениями содержания натрия в стандартном
образце не превышает следующего значения:D= 0,059 Xат.+
0,036
абс. = 0,05X+0,03, где 0,05;
0,03 — коэффициенты регрессии.Допускается проведение анализа без параллельных
определений при наличии в партии испытуемых проб стандартных образцов. За
результат испытания принимают результат единичного определения, если разница
между воспроизведенным и аттестованным значениями содержания натрия в стандартном
образце не превышает следующего значения:D= 0,059 Xат.+
0,036
где D — допустимое отклонение среднего результата анализа стандартного образца от его аттестованного значения, %;Хат — аттестованное значение массовой доли натрия, взятое из свидетельства, %; 0,059; 0,036 — коэффициенты регрессии. Контрольные анализы образцов и анализ стандартных образцов проводят в двух параллельных определениях.
Аргентометрический метод определения содержания хлоридов и хлорида натрия (арбитражный)
Сущность метода состоит в растворении хлоридов пробы в воде, осветлении раствора, слабом окислении азотной кислотой, осаждении хлоридов в виде хлорида серебра с помощью стандартного титрованного раствора нитрата серебра и титровании избытка нитрата серебра стандартным титрованным раствором роданида калия или роданида аммония.
Аппаратура, материалы и реактивы: весы лабораторные 2-го класса точности наибольшим пределом взвешивания 200 г; аппарат для взбалтывания жидкостей в емкостях типа АВУ-бс или других аналогичных марок; колбы мерные вместимостью 1000; 500; 200; 100 см3;колбы конические вместимостью 250; 100 и 50 см3;пипетки вместимостью 100, 50, 25, 20, 5 и 2 см3;бюретки вместимостью 25, 10 и 5 см3;цилиндры вместимостью 500 и 100 см3;бумага фильтровальная; уголь активированный, не содержащий и не сорбирующий хлориды; кислоту азотную; квасцы железоаммонийные; цинка ацетат; натрия хлорид по ГОСТ 4233 или стандарт-титр; калия хромат, раствор массовой долей 10 %; кислоту уксусную ледяную; калия феррицианид (II);калия роданид или аммония роданид; серебра нитрат ; ацетон; гексан; вода дистиллированная.
Подготовка к проведению анализа.Подготовка проб
Приготовление раствора Карреза-121,9 г ацетата цинка растворяют в мерной колбе вместимостью 100 см3 в небольшом объеме дистиллированной воды, добавляют 3 см3 ледяной уксусной кислоты и доводят водой до метки.
Приготовление раствора Карреза-20,6 г феррицианида (II) калия растворяют в мерной колбе вместимостью 100 см3 в небольшом объеме дистиллированной воды и доводят водой до метки.
Приготовление насыщенного раствора железоаммонийных квасцов.500 г измельченных квасцов растворяют в 1000 см3 кипящей дистиллированной воды. Раствор охлаждают, помещая колбу в холодную воду. Образовавшиеся кристаллы отделяют декантацией или фильтрованием. К полученному раствору при перемешивании добавляют небольшими порциями концентрированную азотную кислоту до тех пор, пока раствор не станет прозрачным (около 40 см3)
Приготовление раствора хлорида натрия молярной концентрации c(NaCl) 0,1 моль/дм3 5,8454 г хлорида натрия, предварительно высушенного при 120 °С до постоянной массы, количественно переносят в мерную колбу вместимостью 1000 см, растворяют в небольшом объеме дистиллированной воды и доводят до метки. Допускается приготовление раствора из фиксанала.
Приготовление раствора нитрата серебра молярной концентрации c(AgNО3) = 0,1 моль/дм3 17,00 г нитрата серебра переносят в мерную колбу вместимостью 1000 см, растворяют в небольшом объеме дистиллированной воды и доводят до метки. Раствор хранят в банке из темного стекла.
Определение коэффициента поправки раствора азотнокислого серебра
В коническую колбу вместимостью 100 см3 отмеряют 20 см3 раствора хлорида натрия молярной концентрации 0,1 моль/дм3, добавляют 4 капли раствора хромата калия массовой долей 10 % и титруют раствором нитрата серебра при постоянном перемешивании до изменения окраски раствора от лимонной до слабо-оранжевой. Коэффициент поправки к раствору нитрата серебра К1рассчитывают по формулеК1=VK/V1где V— объем раствора хлорида натрия, см3;К— коэффициент поправки раствора хлорида натрия, равный 1;V1 — объем раствора нитрата серебра, израсходованный на титрование, см3.Молярную концентрацию раствора нитрата серебра C1, моль/дм3, рассчитывают по формуле С1= СК1 где С— заданная молярная концентрация нитрата серебра в растворе, равная 0,1 моль/дм3; К1 — коэффициент поправки к раствору нитрата серебра.
Приготовление раствора роданида калия или роданида аммония молярной концентрации c(KSCN) или c(NH4SCN) = 0,1 моль/дм3
9,72 г роданида калия или 8,00 г роданида аммония переносят в мерную колбу вместимостью 1000 см3, растворяют в небольшом объеме дистиллированной воды и доводят до метки. Раствор хранят в банке из темного стекла. Допускается приготовление раствора из фиксанала.
Определение коэффициента поправки раствора роданида калия или роданида аммония
В коническую колбу вместимостью 250 см3 отмеряют 25 см3 раствора нитрата серебра, добавляют 2 см3 насыщенного раствора железоаммонийных квасцов, 50 — 100 см3 дистиллированной воды и титруют раствором роданида калия или роданида аммония до неисчезающей слабооранжевой окраски.
Коэффициент поправки раствора роданида калия или роданида аммония (К2) рассчитывают по формуле К2=V2 K1/V3где V2— объем раствора нитрата серебра, см3;К2 — коэффициент поправки раствора нитрата серебра;V3 — объем раствора роданида калия или роданида аммония, израсходованный на титрование, см3.Точную концентрацию раствора роданида калия или роданида аммония С2, моль/дм3, рассчитывают по формулеC2=C3K2где с3 — заданная молярная концентрация раствора роданида калия или роданида аммония, равная 0,1 моль/дм3; К2 — коэффициент поправки к раствору роданида калия или роданида аммония.
Порядок проведения анализа
Навеску исследуемого продукта массой около 5 г взвешивают с погрешностью не более 0,0002 г. переносят в мерную колбу вместимостью 500 см3, добавляют 400 см3 дистиллированной воды, 5 см3 раствора Карреза-1, перемешивают и добавляют 5 см3 раствора Карреза-2. Содержимое колбы взбалтывают на аппарате для взбалтывания в течение 30 мин, доводят дистиллированной водой до метки, перемешивают и фильтруют. Для получения неокрашенных и прозрачных вытяжек в колбу с навеской добавляют 1 г активированного угля. Для кормов с высоким содержанием коллоидных веществ, жмыхов, зерна, подвергнутых гидротермической обработке, анализ проводят, как описано выше, но не фильтруют. 100 см3 вытяжки переносят в мерную колбу вместимостью 200 см3 и доводят до метки ацетоном. Раствор перемешивают и фильтруют. В коническую колбу переносят аликвотную часть (25—100 см3) фильтрата соответственно ожидаемому содержанию хлоридов. Аликвотная часть должна содержать не более 150 мг хлорида. Раствор доводят дистиллированной водой до объема не менее 50 см3, добавляют 5 см3 концентрированной азотной кислоты, 2 см3 насыщенного раствора железоаммонийных квасцов и 2 капли раствора роданида калия или роданида аммония из бюретки, заполненной до нулевой отметки, (остаток раствора используется потом для титрования избытка нитрата серебра). Потом добавляют раствор нитрата серебра из бюретки или пипетки до исчезновения красной окраски и некоторый его избыток (для комбикормов и сырья в зависимости от ожидаемого содержания хлоридов общий объем добавленного нитрата серебра составляет от 2 до 5 см3, для контрольного опыта — от 0,5 до 2 см3). При добавлении нитрата серебра содержимое колбы энергично взбалтывают для коагуляции выпадающего осадка. Для обеспечения лучшей коагуляции осадка добавляют 5 см3 гексана. Опыт выполняют в вытяжном шкафу. Потом титруют избыток нитрата серебра раствором роданида калия или роданида аммония до появления красновато-коричневой окраски, не исчезающей в течение 30с.Одновременно проводят контрольный опыт, используя все указанные реактивы. Вместо исследуемой вытяжки берут такой же объем дистиллированной воды.
Расчет результатов анализа
Массовую долю в пробе хлорида натрия X, %, рассчитывают по формуле
5,845[(V5-V5¢) ×C1-(V6-V6¢)C2] ×500
![]() X=
X=
M×V4
где 5,845 — коэффициент для пересчета результата в виде процентного содержания хлорида натрия; К5 — объем раствора нитрата серебра, добавленный в исследуемую пробу, см3; V'5 — объем раствора нитрата серебра, добавленный в контрольный опыт, см3; c1 — точная молярная концентрация раствора нитрата серебра, моль/дм3; V6 — объем раствора роданида калия или роданида аммония, использованный на титрование исследуемой пробы, см3; V'6 — объем раствора роданида калия или роданида аммония, использованный на титрование контрольного опыта, см3;
с2 — точная молярная концентрация раствора роданида калия или роданида аммония, моль/дм3; 500 — общий объем водной вытяжки, см3; т — масса навески, г; V4 — объем аликвотной части фильтрата, использованный для анализа, см3.
Показатели точности анализа
Допустимые расхождения между результатами параллельных определений не должны превышать 0,05 % при содержании хлорида натрия менее 1 %. При содержании хлорида натрия более 1 % предельно допустимые расхождения между результатами параллельных определений не должны превышать 5 %.
Оформление результата анализа
|
Дата |
Проба комбикорма или комбикормового сырья |
Массовая доля натрия, X1% |
Массовая доля хлорида натрия, Х3, % |
|
|
|
29.01.2008 |
№16 |
7% |
19% |
||
|
16.02.2009 |
№4 |
12% |
26% |
||
|
03.06.2009 |
№21 |
10% |
20% |
||
ФОТОМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ФОСФОРА
Сущность метода заключается в минерализации пробы способом сухого или мокрого озоления с образованием солей ортофосфорной кислоты и последующем фотометрическом определении фосфора в виде окрашенного в желтый цвет соединения — гетерополикислоты, образующегося в кислой среде в присутствии ванадат- и молибдатионов.
Аппаратура, материалы и реактивы для определения содержания фосфора после сухого озоления пробы:
Измельчитель проб растений ИПР-2..
Мельница лабораторная МРП-2.
Сушилка проб кормов СК-1 или шкаф сушильный лабораторный с погрешностью не более ±2 °С.
Сито с отверстиями диаметром 1 мм.
Ножницы.
Весы лабораторные 2-го класса точности с наибольшим пределом взвешивания 200 г по ГОСТ 24104.
Мезгообразователь МЛ-1.
Весы лабораторные 3-го и 4-го классов точности с наибольшим пределом взвешивания 500 г по ГОСТ 24104.
Спектрофотометр или фотоэлектроколориметр с максимумом светопропускания в области 440—465 нм.
Печь муфельная электрическая типа ПМ-8 или МР-64-0215 по ГОСТ 9736 или других аналогичных типов.
Щипцы для тиглей муфельные.
Ступка фарфоровая с пестиком по ГОСТ 9147.
Тигли фарфоровые № 3, № 4 по ГОСТ 9147.
Плитка электрическая с закрытой спиралью по ГОСТ 14919 .или других аналогичных типов.
Эксикатор по ГОСТ 25336.
Пипетки градуированные 1(2,4,5,6)-2-1(5,10,20) по ГОСТ 29169, ГОСТ 29227, ГОСТ 29228, ГОСТ 29229, ГОСТ 29230 или дозаторы с той же вместимостью с погрешностью дозирования не более 5 %.
Воронки стеклянные диаметром 36—56 мм по ГОСТ 25336.
Цилиндр мерный 1(2,3,4)-2-500 по ГОСТ 1770. ГОСТ 26657-97
Стаканы или колбочки химические 1(2)-2-50(100) по ГОСТ 25336.
Колбы мерные 1(2)-2-50(100,500,1000) по ГОСТ 1770.
Бюретки 1(2,3,6)-2-25(50) по ГОСТ 29252, ГОСТ 29253.
Стеклянные или пластмассовые банки вместимостью 250 см3 с плотно закрывающимися пробками или крышками.
Аммоний молибденовокислый по ГОСТ 3765, х. ч., ч. д. а.
Аммоний ванадиевокислый мета по ГОСТ 9336, х. ч., ч. д. а.
Кислота азотная по ГОСТ 4461, х. ч., ч. д. а., концентрированная и разбавленная дистиллированной водой (но объему) 1:2.
Вода дистиллированная по ГОСТ 6709.
Кислота соляная по ГОСТ 3118, х. ч., ч. д. а., концентрированная и разбавленная дистиллированной водой 1:1.
Калий фосфорнокислый однозамещенный по ГОСТ 4198, х. ч.
Перекись водорода по ГОСТ 10929, х. ч., ч. д. а., раствор с массовой долей 30 % и раствор, разбавленный дистиллированной водой 1:9.
Кальций хлористый технический по ГОСТ 450, прокаленный при температуре 250—300 °С в течение 2 ч.
Подготовка к испытанию
Подготовка проб
Среднюю пробу сена, соломы, сенной резки, силоса, сенажа, зеленых кормов измельчают на отрезки длиной 1—3 см, корнеплоды и клубнеплоды разрезают на пластинки (ломтики) толщиной до 0,8 см или измельчают на мезгообразователе. Измельченную пробу тщательно перемешивают и методом квартования выделяют часть средней пробы, масса которой после высушивания должна быть не менее 150 г. Высушивание проб проводят в сушильном шкафу при температуре 60—65 "С до воздушно-сухого состояния. Воздушно-сухую пробу размалывают на лабораторной мельнице и просеивают через сито. Остаток на сите измельчают ножницами или в ступке, добавляют к просеянной части и тщательно перемешивают.
Из средней пробы комбикормов, травяной муки, брикетов, гранул, жмыхов, шротов методом квартования выделяют не менее 150 г материала, размалывают без предварительного подсушивания и просеивают через сито. Остаток на сите измельчают ножницами или в ступке, добавляют к просеянной части и тщательно перемешивают.
Объединенную пробу мухи животного происхождения массой не менее 1,5 кг тщательно перемешивают. Для химического анализа муки в лаборатории из объединенной пробы отбирают 0,5 кг, тщательно перемешивают, высыпают на бумагу и разравнивают тонким слоем. Затем методом квартования выделяют пробу массой около 150 г, размалывают без предварительного подсушивания, просеивают через сито. Остаток на сите измельчают, добавляют к пробе и снова перемешивают. Пробы хранят в сухом месте в чистой стеклянной или пластмассовой банке с плотно закрывающейся крышкой или пробкой.
Приготовление растворов
Приготовление раствора азотной кислоты (раствор № 1):
один объем концентрированной азотной кислоты разводят двумя объемами дистиллированной воды, перемешивают.
Приготовление аммония ванадиевокислого мета (раствор № 2):
2,5 г ванадиевокислого аммония растворяют в нагретой до кипения дистиллированной воде, охлаждают, добавляют 20 см3 концентрированной азотной кислоты и доводят объем раствора дистиллированной водой до 1000 см3, перемешивают.
Приготовление раствора молибденовокислого аммония (раствор № 3):
50 г молибденовокислого аммония растворяют в горячей (свыше 75 °С) воде, охлаждают и доводят объем раствора дистиллированной водой до 1000 см3, перемешивают.
Приготовление окрашивающей смеси (раствор № 4):
равные объемы растворов № 1, 2, 3 последовательно смешивают и в случае появления мути отфильтровывают. Смесь хранят в темном месте при температуре 15—28 ºС не более 6 мес.
Приготовление стандартного раствора фосфата:
4,393 г однозамещенного фосфорнокислого калия, высушенного при температуре 100—105 ºС в течение 1 ч, растворяют в стакане или колбочке вместимостью 50—100 см3, затем содержимое тщательно переносят в мерную колбу вместимостью 1000 см3, объем раствора доводят дистиллированной водой до метки, перемешивают и хранят в склянке с притертой пробкой в течение одного года. В 1 см3 основного раствора содержится 1 мг фосфора.
Приготовление растворов сравнения:
в мерные колбы вместимостью 500 см3 из бюретки вместимостью 50 см' приливают стандартный раствор фосфата в объемах, указанных в таблице 1. В каждую колбу добавляют 5 см3 разбавленного (1:1) раствора соляной кислоты, доводят дистиллированной водой до метки перемешивают
При приготовлении растворов сравнения при анализе кормов животного происхождения в мерные колбы вместимостью 500 см3 приливают основной раствор фосфорнокислого калия в объемах, указанных в таблице 1. В каждую колбу добавляют 5 см3 концентрированной азотной кислоты, 25 см 3 разбавленной (1:1) соляной кислоты, доводят дистиллированной водой до метки и перемешивают.
|
Таблица19 |
||
|
Номер колбы |
Объем стандартного раствора фосфора, см3 |
Масса фосфора в 100 см3 растворов сравнения, мг |
|
1 |
0 |
0 |
|
2 |
3 |
0,6 |
|
3 |
5 |
1,0 |
|
4 |
10 |
2,0 |
|
5 |
20 |
4,0 |
|
6 |
30 |
6,0 |
|
7 |
40 |
8,0 |
|
8 |
50 |
10,0 |
Проведение испытания
В предварительно охлажденный в эксикаторе и взвешенный с погрешностью не более 0,001 г тигель берут навеску испытуемой пробы, приготовленной, массой 0,5-2,0 г (для кормов животного происхождения берут навеску массой 0,3-0,4 г), в зависимости от ожидаемого содержания фосфора. Тигель помещают в холодную муфельную печь и повышают температуру до 200-250 ºС, до появления дыма. Допускается предварительное сжигание пробы на электрической плитке или газовой горелке, при этом следует избегать воспламенения пробы, помещая тигли на асбестовую сетку.
После прекращения выделения дыма температуру в печи увеличивают до (525±25) ºС и ведут прокаливание 4-5 ч затем тигли с золой охлаждают. Отсутствие несгоревших частиц угля и равномерный светло-серый (иногда розовый, зеленоватый или голубоватый) цвет золы указывает на полное озоление навески. В противном случае золу осторожно смачивают несколькими каплями дистиллированной воды приливают 1-2 см3 перекиси водорода (1:9) и содержимое тигля выпаривают (в сушильном шкафу, на электроплитке или другим способом) и затем тигли с золой снова помещают в печь, прокаливают при температуре (525±25) ºС еще в течение одного часа. Затем тигли охлаждают, золу смачивают несколькими каплями дистиллированной воды, добавляют 1 см3 соляной кислоты (1:1) и 5-10 см3 дистиллированной воды, тщательно перемешивают стеклянной палочкой и переносят не фильтруя, через воронку в мерную колбу вместимостью 100 см3 Тигель и воронку тщательно обмывают водой, доводят раствор водой до метки, перемешивают и дают осадку отстояться. Аликвоту для анализа берут, не взмучивая осадка. Подготовка контрольного раствора (холостое определение) включает все стадии анализа, кроме взятия навески.

Рис.8 определение содержание фосфора. Подготовка пробы.
Золу, полученную при сжигании костной, мясокостной или рыбной муки, смачивают несколькими каплями дистиллированной воды, приливают 1 см3 концентрированной азотной кислоты, затем 5см3 разбавленного (1:1) раствора соляной кислоты, доводят до кипения, охлаждают и содержимое тигля переносят, не фильтруя через воронку в колбу вместимостью 100 см3, доводят дистиллированной водой до метки, перемешивают.
Из растворов озолята анализируемых проб пипеткой берут по 10 см3 раствора и переносят в .мерную колбу вместимостью 50 см3 добавляют 5 см3 раствора азотной кислоты раствор № 1) и 15 см3 окрашивающего раствора № 4, доводят дистиллированной водой до метки. После каждого добавления растворов и воды растворы тщательно перемешивают.
Через 30 мин окрашенные растворы сравнения фотометрируют против нулевого раствора шкалы (раствор № 1), не содержащего фосфор, а испытуемые зольные растворы анализируемых образцов - относительно контрольного (холостого) раствора. Фотометрирование проводят в кюветах с толщиной просвечиваемого слоя 5-20 мм, используя синий светофильтр с максимумом светопропускания в области-440-465 нм. Если оптическая плотность испытуемого раствора превышает оптическую плотность раствора сравнения, анализируемый раствор разбавляют нулевым раствором шкалы до оптимальной для фотометрирования концентрации (оптическая плотность 0,2— 0,8) и повторяют описанные выше операции в том же порядке. Полученный результат увеличивают во столько раз, во сколько раз был разбавлен раствор анализируемой пробы.
Построение градуированного графика
По результатам фотометрирования растворов сравнения строят градуировочный график, откладывая на оси абсцисс — содержание фосфора в 100 см3 растворов сравнения в миллиграммах, на оси ординат — соответствующее значение оптической плотности.
Для построения каждой точки градуировочного графика вычисляют среднее арифметическое значение оптической плотности двух отсчетов на приборе.
Обработка результатов
Массовую долю фосфора (Л), %, вычисляют по формуле
m1 100
![]() X=
X=
m
где т{ — масса фосфора в навеске, найденная по графику, мг; т — масса навески, мг;
100 — коэффициент пересчета в проценты.
-Массовую долю фосфора в пересчете на абсолютно сухое вещество, %, вычисляют по формуле
X=X 100\100-W
где X— массовая доля фосфора в испытуемой пробе, %;
W— массовая доля влаги в испытуемой пробе, %, определяется по ГОСТ 27548;
100 — коэффициент пересчета в проценты.
За окончательный результат испытания принимают среднее арифметическое результатов двух параллельных определений.
Результаты вычисляют до третьего десятичного знака и округляют до второго десятичного знака.
Допускаемые расхождения между результатами двух параллельных определений (dбс) и между двумя результатами, полученными в разных лабораториях (Da6c) при доверительной вероятности Р = 0,95, не должны превышать следующих значений:
dабс=0,091X+0,01
Da6c=0,28X+0,01
X— среднее арифметическое результатов двух параллельных определений, %; X — среднее арифметическое результатов двух испытаний, выполненных в разных лабораториях, %. Допустимую предельную погрешность результата анализа (Da6c) для односторонней доверительной вероятности Р= 0,95 вычисляют по формуле
Az абс = 0,1641+0,007
Допускается проведение анализа без параллельных определений при наличии в партии испытуемых проб стандартных образцов (СО), если разница между воспроизведенной и аттестованной в СО массовой долей фосфора не превышает D.
D=0,20X+0,007
где D — допускаемое отклонение среднего результата анализа стандартного образца от его аттестованного значения, указанного в свидетельстве, %; Х — аттестованное значение анализируемого компонента, взятое из свидетельства.
В этом случае (при обязательном проведении выборочного статистического контроля сходимости параллельных определений) за результат испытания принимают результат единичного определения.
Контрольные анализы образцов испытуемой пробы и анализы СО проводят в двух параллельных определениях.
Аппаратура, материалы и реактивы для определения содержания фосфора после мокрого озоления
Весы лабораторные 2-го класса точности с наибольшим пределом взвешивания 200 г по ГОСТ 24104.
Весы лабораторные 3-го и 4-го классов точности с наибольшим пределом взвешивания 500 г
Спектрофотометр или фотоэлектроколориметор с максимумом светопропускания 440-465 нм
Нагревательное устройство для пробирок или колб с температурой нагрева до 380 ºС (допускается применение электроплиток, покрытых асбестовой)
Бюретки 1(2,3,б)-2-50 по ГОСТ 29252 и ГОСТ 29251
Колбы мерные 1(2)-2-100(!000) по ГОСТ 1770
Стаканы или колбы 1(2)-2-50(100) по ГОСТ 25336
Аммоний молибденовокислый по ГОСТ 3765 х ч ,ч д.а.
Аммоний ванадиевокислый мета по ГОСТ 9336 х ч ,ч д.а.
Азотная кислота по ГОСТ 4461, х. ч., ч д а,концентрированная и разбавленная водой (по объему) 1:2
Серная кислота по ГОСТ 4204 х ч ч д а, концентрированная
Калий фосфорнокислый однозамещедный
Селен аморфный по ГОСТ 10298, ч.
Перекись водорода по ГОСТ 10929, х ч ч д а, раствор с массовой долей 30%
Дистиллированная вода по ГОСТ 6709
Примечание - Допускается использовать другую аппаратуру, мерную посуду, имеющие такие же или лучшие метрологические, а также реактивы по квалификации не ниже отечественных.
Подготовка к испытанию
Подготовка проб
Приготовление растворов
Приготовление раствора серной кислоты, содержащей селен
Аморфный селен растворяют при нагревании в колбе из термостойкого стекла в концентрированной серной кислоте до его обесцвечивания из расчета 5 г селена на 1000 см3 кислоты. Эту смесь используют для озоления испытуемых проб при определении азота, фосфора, калия из одной навески и при приготовлении шкалы образцовых растворов.
Приготовление раствора аммония ванадиевокислого мета
Приготовление раствора аммония молибденовокислого
Приготовление окрашивающей смеси: смешивают равные объемы растворов №2, №3 и дистиллированной воды, перемешивают.
Приготовление основного раствора фосфата.
Приготовление растворов сравнения:
В мерные колбы вместимостью 1000 см3 из бюретки вместимостью 50 см3 вносят стандартный раствор фосфата в объемах, указанных в таблице 20. В каждую колбу наливают до половины дистилированную воду добавляют 30см3 концентрированной серной кислоты, содержащей селен. Растворы охлаждают и доводят дистиллированной водой до метки ( после прибавления каждого из указанных реактивов растворы перемешивают)
При температуре 15-28 °С растворы хранят не более 3 мес в местах, защищенных от прямых солнечных лучей.
Таблица 20
|
Номер колбы |
Объем стандартного раствора фосфора, см3 |
Масса фосфора в 100 см3 растворов сравнения, мг |
|
1 |
0 |
0 |
|
2 |
2 |
0,2 |
|
3 |
5 |
0,5 |
|
4 |
10 |
1,0 |
|
5 |
15 |
1,5 |
|
6 |
20 |
2,0 |
|
7 |
25 |
2,5 |
|
8 |
30 |
3,0 |
|
9 |
35 |
3,5 |
Спирт этиловый ректификованный технический по ГОСТ 18300
Вода дистиллированная по ГОСТ 6709. 5. 2
Подготовка к испытанию
Подготовка проб
Приготовление растворов
Приготовление раствора молибденовокислого аммония
90 г молибденовокислого аммония, взвешенного с погешностью не более 0,01 г, растворяют в теплой дистиллированной воде. После охлаждения к раствору приливают аммиак до слабощелочной реакции, затем доводят листиллированной водой до 1000 см3 и через 12 ч. фильтруют.
Приготовление азотной кислоты с массовой долей 1 %
11 см3 концентрированной азотной кислоты (d=1, 40 г\см3) растворяют в дистилированной воде -в мерной колбе вместимостью 1000 см3, объем раствора доводят до метки дистиллированной водой, перемешивают. Приготовление 1 % спиртового раствора фенолфталеина
1 г фенолфталеина, взвешенный с погрешностью не более 0,01г,растворяют в этиловом спирте в мерной колбе вместимостью 100 см3
Приготовление 0,1 % спиртового раствора метил-рота
0,1 г. метил-рота (метиловый красный), взвешенного не более 0,001 г, растворяют при нагревании в 95%-ном этиловом спирте в мерной колбе вместимостью 100 см3, перемешивают.
Проведение испытания
Навеску рыбной или крилевой муки массой 0,3—0,5 г взвешивают с погрешностью не более 0,001 г, помещают в колбу Кьельдаля вместимостью 100 см3, приливают 5 см3 концентрированной серной кислоты. Колбу с содержимым осторожно нагревают так, чтобы избежать сильного вспенивания. Для ускорения процесса озоления пробы в колбу, после ее охлаждения, приливают 2 см3 азотной кислоты и снова нагревают
После обесцвечивания раствор охлаждают и приливают 5 см3 дистилированной воды, затем осторожно кипятят для удаления оксидов азота (до исчезновения бурой окраски паров оксидов азота)
Охлажденный раствор переносят в мерную колбу вместимостью 100 см3 многократным смыванием дистилированной водой и после охлаждения объем раствора доводят до метки, перемешивают.
В химический стакан или коническую колбу вместимостью 300-400 см3 отбирают 25 см3 раствора, добавляют 2 капли индикатора метилового красного, нейтрализуют аммиаком до перехода красной окраски в желтую, добавляют 5 см3 азотной кислоты, 10 см3 насыщенного раствора азотнокислого аммония и доводят объем дистилированной водой до 60-80 см3 .Раствор подогревают до 30-40 ºС и при перемешивании приливают 10 см3 раствора молибденовокислого аммония, дают постоять 1-2 мин и снова приливают при перемешивании 5 см3 раствора молибденовокислого аммония. Смесь перемешивают в течение 5-10 мин и оставляют на 1 ч. После этого фильтруют через плотный бумажный фильтр, стараясь оставить осадок в колбе. Осадок тщательно промывают один раз раствором азотной кислоты с массовой долей 1%, а затем охлажденной дистилированной водой до нейтральной реакции на лакмус промывных вод.
Обработка результатов
Массовую долю фосфора Х2, %, вычисляют по формуле
X2=(VK1-V1K2) V2 100 0,0001348\m25
Где V- объем раствора гидроксида натрия 0,1 моль\дм3, добавленный для растворения осадка, см3.
K1 – коэффициент пересчета на раствор гидроксида натрия точной концентрации 0,1 моль\дм3.
V1- объем раствора серной кислоты точной концентрации 0,05 моль/дм3; израсходованной на титрование избытка щелочи, см3.
K2 - коэффициент пересчета на раствор серной кислоты точной концентрации 0,05 моль/дм3.
V2 – конечный объем раствора минерализованной пробы, см3.
100 — коэффициент пересчета в проценты.
0,0001348 — количество фосфора, соответствующее 1см3 раствора концентрацией 0,1 моль/дм3 гидрокисида натрия, г;
m — масса навески, г;
25 — объем испытуемого раствора, взятый для определения, см3.
За результат испытания принимают среднее арифметическое значение результатов двух параллельных определений. Результаты вычисляют до третьего десятичного знака и округляют до второго десятичного знака.
Допускаемые расхождения между результатами двух параллельных определений при доверительной вероятности Р=0,95 не должны превышать:
d = 0,05 абс. %
между результатами, полученными в разных лабораториях,
D = 0,10 абс. %.
Предельная погрешность результата анализа при односторонней доверительной вероятности P= 0,95 не должна превышать
Az = 0,06 абс. %.
Допускается проведение анализов без параллельных определений при наличии в партии испытуемых проб стандартных образцов (СО), если разница между воспроизведенной и аттестованной в СО массовой долей фосфора не превышает D
D = 0,07 абс. %
где D — допускаемое отклонение среднего результата анализа СО от его аттестованного значения, указанного в свидетельстве, абс. %.
При обязательном проведении выборочного статистического контроля сходимости параллельных определений за результат испытания принимают результат единичного определения.
Контрольные анализы образцов испытуемой пробы и анализы СО проводят в двух параллельных определениях.
Определение сырой клетчатки
Принцип метода состоит в обработке испытуемого продукта смесью концентрированной азотной и 80%-ной уксусной кислоты, промывании остатка водой, спиртом, эфиром и последующем высушивании.
Приборы, материалы, реактивы: весы аналитические, сушильный шкаф, насос вакуумный, плитка электрическая, холодильник воздушный обратный со шлифом, колба Бунзена вместимостью 1 л., воронка Бюхнера №4 или 5, цилиндры мерные на 50 и 100 мл, эксикатор, пинцет, промывалка, колбы конические плоскодонные со шлифом вместимостью 100 мл, кислота азотная и уксусная.
Для приготовления 80%-ного раствора уксусной кислоты 800 мл ледяной уксусной кислоты переносят в мерную колбу вместимостью 1 л. и доводят дистилированной водой до метки. Для приготовления реакционной смеси смешивают 2 объема азотной кислоты с 9 объемами 80-ной уксусной кислоты.
Проведение анализа. Навеску массой 1 г. взвешивают с погрешностью не более 0,0002 г., переносят в коническую колбу на 100 мл и осторожно, по стенкам, приливают 40 мл реакционной смеси. Затем присоединяют к колбе воздушный холодильник со шлифом и ставят на электроплитку. Гидролиз осуществляется под вытяжным шкафом при слабом равномерном кипении смеси в течение 30 минут, считая от момента закипания. При сильном кипении под колбу подкладывают слой асбеста. По окончании гидролиза холодильник отсоединяют от колбы, а ее содержимое в горячем состоянии фильтруют через бумажный фильтр, помещенный в воронку Бюхнера. Фильтр с бюксой должен быть заранее просушен при температуре 160ºС в течение 10 мин и взвешен. Колбу промывают 3-4 раза горячей водой, перенося смывы на фильтр. Для удаления остатка реакционной смеси осадок на фильтре промывают 10 мл спирта и 10 мл. эфира и выключают насос. Фильтр с клетчаткой захватывают пинцетом, складывают, переносят в бюксу, подсушивают на воздухе и сушат в сушильном шкафу при температуре 160ºС в течение 15 минут. Высушенную бюксу с клетчаткой охлаждают в эксикаторе и взвешивают. Содержание сырой клетчатки вычисляют по формуле:
М1-М2
![]() Х= ·100,
Х= ·100,
М
Где Х-содержание клетчатки,%; М1 – масса бюксы с клетчаткой и фильтром, г; М2 –масса бюксы с фильтром,г; М-масса навески,г.
Определение сырого жира
Сущность метода заключается в определении количества жира, экстрагированного из навески корма этиловым эфиром.
Приборы, материалы, реактивы: весы аналитические, аппарат Сокслета, водяная баня с терморегулятором, сушильный шкаф, фильтровальная бумага, эфир этиловый.
Проведение анализа: из листа фильтровальной бумаги размером 6·7 см делают пакет (завертывают, как в аптеке при изготовлении порошков) и высушивают при температуре 105 ºС до постоянной массы. В высушенный и взвешенный пакет отвешивают 1,0-2,0 г. испытуемой пробы с погрешностью не более 0,001 г. Пакетик закрывают, помещают в ту же бюксу и высушивают в сушильном шкафу при температуре 105 ºС до постоянной массы. Затем охлаждают в эксикаторе и взвешивают. Приготовленных таким образом 8-12 пакетиков помещают в экстрактор аппарата Сокслета. Затем в экстрактор наливают эфир до тех пор, пока он не потечет в колбу и не заполнит ее на 2\3. После этого в экстрактор вставляют холодильник и через него пускают воду, а колбочку нагревают на водяной бане при температуре около 50 ºС. При этом пары эфира поднимаются в холодильник, где эфир конденсируется, стекает в экстрактор, смачивает пакетик с веществом и извлекает из него жир. Когда уровень эфира поднимается несколько выше колена сифонной трубки, он вместе с извлеченным из вещества жиром стекает в колбу, откуда снова испаряется, оставляя в колбе жир, попадает в холодильник, оттуда – снова в экстрактор. Таким образом происходит постепенное извлечение жира из вещества. Надо следить за тем, чтобы водяная баня не нагревалась сильно и чтобы эфир не кипел бурно, так как при этом он не сможет полностью охлаждаться в холодильнике и частично будет улетучиваться. При равномерной экстракции происходит 4-5 сливаний в течение 1 часа. Экстрагирование продолжается несколько часов. Для проверки степени извлечения жира смачивают коней полоски фильтровальной бумаги эфиром из экстрактора. Если после испарения эфира на фильтровальной бумаге не останется жирного пятна, экстрагирование считается законченным. После окончания экстракции пакетик с обезжиренным остатком вынимают, просушивают в вытяжном шкафу на часовом стекле, а затем помещают в сухой предварительно взвешенный стаканчик с притертой пробкой и высушивают при температуре 105 ºС до постоянной массы. Зная массу пакета и массу пакета с веществом до и после экстрагирования, определяют количество жира во взятой навеске по формуле:
Б-В
![]() Х= Б-А ·100,
Х= Б-А ·100,
Где Х- количество жира, %; Б – масса пакета с веществом до экстрагирования и В – после экстрагирования, г; А- масса пакета без вещества, г.
РЕЗУЛЬТАТЫ ПРОВЕДЕННЫХ ИССЛЕДОВАНИЙ
|
Порядковый номер опыта |
Протеин, мг\т |
Сырая клетчатка,мг/т |
Обмен ная энергия, ккал |
Кальций доля |
Фосфор доля |
Хлорид натрия доля |
Сырой жир,мг |
Кислотность, рН |
Натрийдоля |
|
1 |
22,0 |
4,05 |
308 |
0,95 |
0,65 |
0,36 |
7,17 |
4,4 |
0,12 |
|
2 |
21,0 |
5,1 |
315 |
0,90 |
0,59 |
0,36 |
11,05 |
3,8 |
0,16 |
|
3 |
18,5 |
6,7 |
318 |
0,88 |
0,72 |
0,42 |
|
3,2 |
0,16 |
|
4 |
23,5 |
3,2 |
300 |
0,96 |
0,67 |
0,34 |
4,41 |
5,2 |
0,14 |
|
5 |
21,0 |
5,1 |
315 |
0,90 |
0,59 |
0,36 |
11,12 |
2,8 |
0,16 |
|
6 |
18,5 |
6,4 |
318 |
0,88 |
0,72 |
0,42 |
13,51 |
4,0 |
0,14 |
|
7 |
18,5 |
6,4 |
318 |
0,88 |
0,72 |
0,34 |
|
;.4 |
0,16 |
|
8 |
22,0 |
4,6 |
308 |
0,95 |
0,74 |
0,34 |
|
4,0 |
0,12 |
|
9 |
23,5 |
3,2 |
300 |
0,96 |
0,67 |
0,36 |
3,86 |
5,2 |
0,10 |
|
10 |
19,0 |
6,5 |
320 |
0,88 |
0,60 |
0,36 |
14,20 |
3,8 |
0,12 |
|
11 |
21,0 |
5,1 |
315 |
0,90 |
0,59 |
0,36 |
11,12 |
4,0 |
0,14 |
|
12 |
19,0 |
6,5 |
320 |
0,88 |
0,60 |
0,34 |
12,86 |
4,0 |
0,10 |
|
13 |
22,0 |
4,1 |
308 |
0,95 |
0,65 |
0,36 |
7,72 |
5,2 |
0,12 |
|
14 |
19,0 |
6,6 |
320 |
0,88 |
0,60 |
0,34 |
13,02 |
4,0 |
0,12 |
|
15 |
22,0 |
4,1 |
308 |
0,95 |
0,59 |
0,36 |
7,20 |
5,2 |
0,12 |
|
16 |
21,0 |
5,1 |
315 |
0,90 |
0,60 |
0,36 |
10,68 |
4,0 |
0,10 |
|
17 |
19,0 |
6,5 |
320 |
0,88 |
0,60 |
0,36 |
13,26 |
4,0 |
0,12 |
|
18 |
19,0 |
6,6 |
320 |
0,88 |
0,60 |
0,36 |
13,00 |
3,6 |
0,12 |
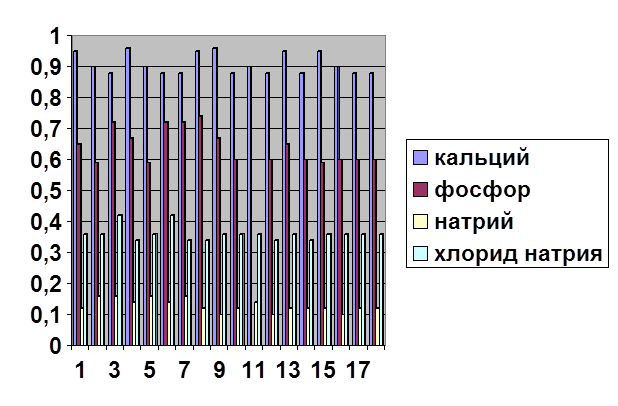
Таким образом, в ходе проведенных исследований было установлено, что оптимальное количество фосфора, кальция, хлорида натрия в комбикормах соответственно составляет примерно 0,70 долей, 0,90 долей, 0,36 долей. Мы поставили также опыт на определение влияния состава комбикормов на рост, развитие птицы. В качестве объектов были выбраны группы птиц 1 корпуса, примерно одного возраста.
Одной группе птиц мы давали корм, в котором отсутствовал кальций,
второй группе птиц предлагался корм, в котором был дефицит фосфора,
третья группа птиц получала сбалансированный корм, в котором содержалось необходимое количество макро- и микроэлементов, витаминов. Результаты опытов оказались следующие:
1 группа птиц отставала в росте, у особей обнаружены остеопороз, рахит.

У второй группы обнаружены: искривление позвоночника, ребер,
трубчатых костей и клюва у птиц. 
У третьей группы отклонений от нормы не выявлено.

Заключение
Живой организм- это вся периодическая система Д.И. Менделеева, собранная воедино. Одни элементы присутствуют в большем количестве, другие - в меньшем. Химические элементы входят в состав клеток органов и тканей, с их участием происходят процессы кроветворения, секреции, мышечного сокращения, нервной проводимости, внутритканевого дыхания.
В данной работе мы рассмотрели как основные химические элементы влияют на работу живого организма, и как питание оказывает влияние на жизнедеятельность систем на примере организации питания кур. В соответствии с поставленными целями, задачами, гипотезой была проведена следующая работа и сделаны соответствующие выводы:
1) установлено, каждый химический элемент, как опытный работник, знает свою функцию: кальций является основным компонентом костной ткани, и прочность костей зависит преимущественно от него; магний необходим для нормального функционирования нервной системы, это антистрессовый элемент; железо поддерживает иммунитет; марганец стимулирует рост организма; хром стабилизирует уровень сахара и нормализует обмен веществ; недостаток селена вызывает катаракту, мускульную дистрофию, рак; меди - врожденные болезни сердца; фосфора – рахит; бора, серы, олова – глухоту; ванадия и цинка – диабет, гипогликемию (понижение сахара в крови); висмута – язву желудка и двенадцатиперстной кишки. Поэтому при организации питания птиц в искусственных условиях, с применением комбикормов, специалисты учитывают влияние каждого компонента на живой организм, исключают попадание токсических элементов с пищей, с водой. Для этого хорошо изучаются суточные потребности в каждом из химических элементов, а нормирование состава комбикормов проводится на основе лабораторных анализов.
2) для каждого химического элемента существуют свои методы качественного и количественного анализов. Так, например, для кальция разработаны комплексонометрический метод, пламенно-фотометрический, атомно-абсорбционный, титриметрический методы; для натрия и хлорида натрия – ионометрический метод, аргентометрический метод. После проведения лабораторных анализов результаты опытов сравниваются с показателями предельно-допустимой концентрации и устанавливается пригодность комбикорма к применению.
3)проведена экспериментальная работа, позволяющая оценить влияние организации питания в искусственных условиях на увеличение привеса птицы.
В дальнейшем изучение данного вопроса можно продолжить в направлении разработок методик организации питания в птицеводстве и внедрение нетрадиционных кормов: марикультур (морских водорослей), муки из клеток крови свиней, кукурузной барды (зерна кукурузы при производстве этилового спирта), амаранта (зерновая культура), сухой молочной сыворотки (побочный продукт при изготовлении творога и сыров) и др.
Литература
1.Воложин А.И., Субботин Ю.К. Путь к здоровью. М.: Знание, 1999. – 160 с.
2.Ершов Ю.А., Попков В.А., Берлянд А.С. и др.; под ред. Ю.А. Ершова. Общая химия. Химия биогенных элементов: учеб. для студ. вузов, обуч. по мед., биол.. агроном.. ветеринар., эколог. спец. – М: Высшая школа, 2007. - 169 с.
3. Журавлев Е.М. Руководство по зоотехническому анализу кормов. – М: Сельхозиздат, 1993. – 295 с
4.Земляной В.А. Практические советы по организации производства комбикормов. Новосибирск изд.Север,- 2000.- 476 с.
5. Имангулов Ш.А. Рекомендации по кормлению сельскохозяйственной птицы. Сергиев Посад, ВНИТИП – 2004.- 243 с.
6. Кожевников Е.М. , Войтов Л.И., Ефимова М.Н. Гиповитаминозы у кур (диагностика, профилактика). – Кишинев: Картя Молдовеняскэ, 2006. – 52 с.
7.Ленинджер А.Биохимия.-М.:Мир,1976. – 687 с.
8. Лидин Р.А., Алиакберова Л.Ю. Химия. Справочник для старшеклассников и поступающих в вузы. М.: АСТ-Пресс Школа, 2005. – 325 с.
9.Майстренко В.Н. Эколого-аналитический мониторинг стойких органических загрязнений: уч. Пособие для вузов – М: бином. Лаборатория знаний, 2004. – 374 с.
10. Маслиева О.И. Анализ качества кормов и продуктов птицеводства. – М:Колос, 1997. – 176 с.
11. Методические рекомендации для зоотехнических лабораторий птицеводческих предприятий/ подгот. П.Н. Паньков, В.А. Агеев, Н. В. Лобин и др. – Загорск, 1999. – 45с.
12. Методы анализа кормов и продуктов птицеводства: Метод. рекомендации\ Укр. Н.-и. Ин-т птицеводства; Разраб. П.Ф. Сурай и И.А. ионов. – Харьков. 1999. – 95 с.
13.Миркин Б.М., Наумова Л.Г. Экология Башкортостана. Уфа: Китап, 1995.-144 с.
14 Наука и жизнь №1 2009 с 26-29. Петрухина А. «из чего мы состоим? Из того, что мы едим…»
15. Наука и жизнь №.7 2008 с. 132-137 Клевцова М. «Пища, дети, аллергия»
16. Наука и жизнь №.8 1999 Прозоровский В. «пища и лекарства-звенья одной цепи»
17.Немцов В.И. Основы питания. М.: Диля, 2006.- 143 с.
18. Околелова Т. М. Кормление птицы. Сергиев Посад, ВНИТИП,1996. – 62 с.
19.Околелова Т.М., Румянцев С.Д. Корма и биологически активные добавки для птицы. М.:Колос, 1999. – 163 с.
20. И.Г. Панин Компоненты комбикормов.М.:Сергиев Посад,ВНИТИП,2008. –210 с.
21.Разумов В.А. Массовый анализ кормов – Справочник. – М.:Колос, 1992.- 176 с.
22. Скурихин В.Н. , Шабаев С.В. методы анализа витаминов А, Е, D и каротина в кормах, биологических объектах и продуктах животноводства/ справочное издание. – М.: Химия, 1996. – 96 с.
23.Тюкавкина Н.А.Биоорганическая химия:Учебник для вузов.- М:Дрофа,2004.- 326 с.
24.Уайт А. И др.Основы биохимии.-М.:Мир,1981. – 254 с.
25.Филипович Ю.Б., Егорова Т.Д., Севастянова Г.А. Практикум по общей биохимии.- М.:Просвещение,1982. – 362 с.
26. Филипович Ю.Б Основы биохимии.- М.:Высшая школа,1985. – 165 с.
27. Филипович Ю.Б. биохимические основы жизнедеятельности человека.-М.: Владос,2005. – 268 с.
28.Фисинин В.И., Егоров И.А. Нетрадиционные корма в рационах птицы. Сергиев Посад, ВНИТИП, 2005.- 42 с.
29. Фисинин В.И., Околелова Т.М. Ферменты в кормлении птицы. Сергиев Посад, ВНИТИП,2005. – 153 с.
30.Фисинин В.И., Тишенков А.Н. Оценка качества кормов, органов, тканей, яиц и мяса птицы. Сергиев Посад, ВНИТИП, 2004. – 112 с.
31.Фисинин В.И., Егоров И.А. Кормление сельскохозяйственной птицы. Сергиев Посад, ВНИТИП, 2004.- 325 с.
32. Фисинин В.И., Околелова Т.М. Рекомендации по анализу комбикормов. М.: Знание, 1997. – 37 с.
33. Фисинин В.И. Химический анализ комбикормов. Сергиев Посад, ВНИТИП, 2000.- 157 с.
34. Хомов Р.Б. Академия хорошего здоровья. Том1. Кострома: Северная неделя,2006. – 210 с.
35. Хомов Р.Б. Академия хорошего здоровья. Том 2. Кострома: Северная неделя,2006. – 185 с.
36.Шамарин П.И. Здоровье, болезнь и медицина. Саратов: Приволжское книжное изд., 1993. – 241 с.
37. Шеко Т.С. Корма, комбикорма, комбикормовое сырье. М.: изд. Стандартов, 1996. – 115 с.
38.Шашина Т.П. Комбикорма, комбикормовое сырье. М.: изд. Стандартов, 1999. - 87 с.
39. Экология и жизнь №3 2007.Кузнецов И. « Поговорим о микроэлементах»
40.Япанов Р.А., Зинин О.Л. Норматирование макроэлементов в комбикормовой промышленности. М.: Наука, 2000.- 66 с.
41.Япанов Р.А. Анализ кормов. М.: Наука, 1996.- 202 с.
Скачано с www.znanio.ru
Материалы на данной страницы взяты из открытых источников либо размещены пользователем в соответствии с договором-офертой сайта. Вы можете сообщить о нарушении.